1 Veteriner İç Hastalıkları Laboratuvarı, Veteriner Fakültesi, Konkuk Üniversitesi, Seul, Güney Kore,
Düzenleyen: Davis Seelig, Minnesota Twin Cities Üniversitesi, Birleşik Devletler
İnceleyen: Valeria Martini, Milano Üniversitesi, İtalya
Kun Ho Song, Chungnam Ulusal Üniversitesi, Güney Kore
*İlgili yazar: Hee-Myung Park parkhee@konkuk.ac.kr
Uzmanlık bölümü: Bu makale Frontiers in Veterinary Science dergisinin bir bölümü olan Veteriner Deneysel ve Tanısal Patoloji’ye gönderilmiştir.
Sunum Tarihi: 17 Kasım 2020 Kabul Tarihi: 20 Aralık 2021 Yayın Tarihi:17Ocak 2022
Bu makaleye atıfta bulunmak için: Lee G-W, Kang M-H, Jeon J-H, Song D-W, Ro W-B, Kim H-S and Park H-M (2022) Case Report: Long-Term Survival of a Dog With Chronic Lymphocytic Leukemia Treated With Chlorambucil, Prednisolone, and Imatinib. Front. Vet. Sci. 8:625527. doi: 10.3389/fvets.2021.625527
2 Biyo-Hayvan Bakımı Bölümü, Jangan Üniversitesi, Hwaseong, Güney Kore
Yedi yaşında kısırlaştırılmış erkek Poodle cinsi köpek kronik progresif lenfositoz nedeniyle kliniğe getirildi. Hematolojik ve periferik kan yayma bulguları, iyi diferansiye küçük lenfositlerle belirgin lenfositoz göstermekteydi. Kemik iliği aspiratının sitolojisi, tüm çekirdekli hücrelerin %45’ini oluşturan küçük olgun lenfositlerin infiltrasyonu ile hipersellüler bütünlük gösterdi. Kan ve ilik örneklerinin akış sitometrisi, ağırlıklı olarak CD21 molekülünü eksprese eden neoplastik lenfositleri ortaya çıkardı. İmmünofenotipik analiz sonucunda B hücreli kronik lenfositik lösemi (KLL) tanısı konmuştur. Prednizolon ve klorambusil tedavileri başlatıldı ancak yanıt belirgin değildi. Bu nedenle, KLL ile ilişkili hematolojik anormallikleri gideren imatinib ile ek tedavi verilmiştir. Akış sitometrisi ∼1 yıllık tedaviden sonra CD21 yönünden pozitif lenfosit sayısının normalleştiğini ve hematolojik lenfositozun giderildiğini göstermiştir. Köpek 2 yıl boyunca takip edildi ve herhangi bir ciddi yan etki görülmedi. Bu vaka, tedaviye yanıt vermeyen köpeklerde KLL tedavisinde imatinibin prednizolon ve klorambusil tedavisine ek tedavi olarak iyi bir seçenek olabileceğini göstermiştir.
Anahtar Kelimeler: klorambusil, kronik lenfositik lösemi, köpek, akış sitometrisi, imatinib, lenfositoz GİRİŞ
Kronik lenfositik lösemi (KLL), kemik iliğinde küçük lenfositlerin neoplastik klonal proliferasyonu ile karakterize, daha önce tanımlandığı gibi 3 aydan uzun süre kalıcı ve belirgin periferik lenfositoz şeklinde ortaya çıkan lenfoproliferatif bir hastalıktır (1, 2). KLL’deki lösemik hücreler morfolojik olarak olgun lenfositlere benzer. Kan ve dokular boyunca yayılırlar (3). KLL, yaşlı insanlarda (4) ve köpeklerde (5) görülen indolent bir hastalıktır ve KLL’li köpekler üzerinde yapılan birkaç çalışma, ortalama hastalık başlangıç yaşının ∼10 yıl olduğunu ve 1,5-15 yıl arasında değiştiğini göstermektedir (1, 2, 6). Daha önce yayınlanan bir raporda (2, 5), KLL’nin köpeklerde cinsiyet eğilimi göstermediği ve akut lenfoblastik lösemiye (ALL) kıyasla daha az, miyeloproliferatif bozukluklara kıyasla ise daha sık görüldüğü belirtilmiştir. KLL’nin nedeni hala bilinmemektedir, ancak genetik risk taşıdığı tespit edilmiştir (1, 5). Klinik bulgular spesifik değildir ve bunlar arasında letarji, inappetans, pireksi, kilo kaybı, kusma ve hafif splenomegali/lenfadenopati bulunmaktadır (3). Moleküler genetik analizde klonalitenin görülmesi neoplazi tanısına işaret edebilir.
Akış sitometrisi ile immünofenotipleme kesin tanıya ulaşmak için yararlıdır ve B ve T lenfositlerinin proliferasyonlarını tespit edebilir (2, 6).
ALL ve lösemik lenfomanın aksine KLL, tedavi gerektirmeyen uzun bir subklinik dönemle karakterize yavaş ilerleyen bir hastalık şeklinde tanımlanmaktadır (2). Hayvanda klinik belirtiler ortaya çıktığında, anemik veya trombositopenik hale geldiğinde, lenfadenopati veya hepatosplenomegali olduğunda veya 60.000/μL’nin üzerinde aşırı yüksek lenfosit sayısına sahip olduğunda KLL’nin tedavi edilmesi gerekir (7). KLL’li köpekler için en etkili ilaçlar yakın zamana kadar klorambusil ve prednizolondu. Ancak KLL hala tedavi edilememektedir (8, 9). Vinkristin tedaviye eklenebilir ve klorambusil siklofosfamid ile değiştirilebilir (2). Melfalan ve prednizolon tedavisi, daha önce açıklandığı gibi 8-210 gün boyunca klinik iyileşme gösteren KLL’li köpeklere uygulanabilir (3).
Beşeri tıpta, klorambusil veya anti-CD20 antikorları ile kemoterapi KLL için standart tedavidir (4). İnsan KLL’si için yeni hedefe yönelik tedaviler arasında B-hücresi reseptör inhibitörleri, fosfatidilinositol-4,5-bisfosfat 3- kinaz inhibitörleri, anti-CD20 monoklonal antikorlar ve Bcl-2 antagonistleri bulunmaktadır (4, 10, 11), ancak yakın zamana kadar köpek KLL’sinde kemoimmünoterapi rapor edilmemiştir.
Bu raporda ilk olarak, imatinib ile birlikte klorambusil ve
ve uzun süreli sonuçları açıklanmaktadır.
VAKAYA DAİR BİLGİLER
Vaka Sunumu ve Tanıya Yönelik
İncelemeler
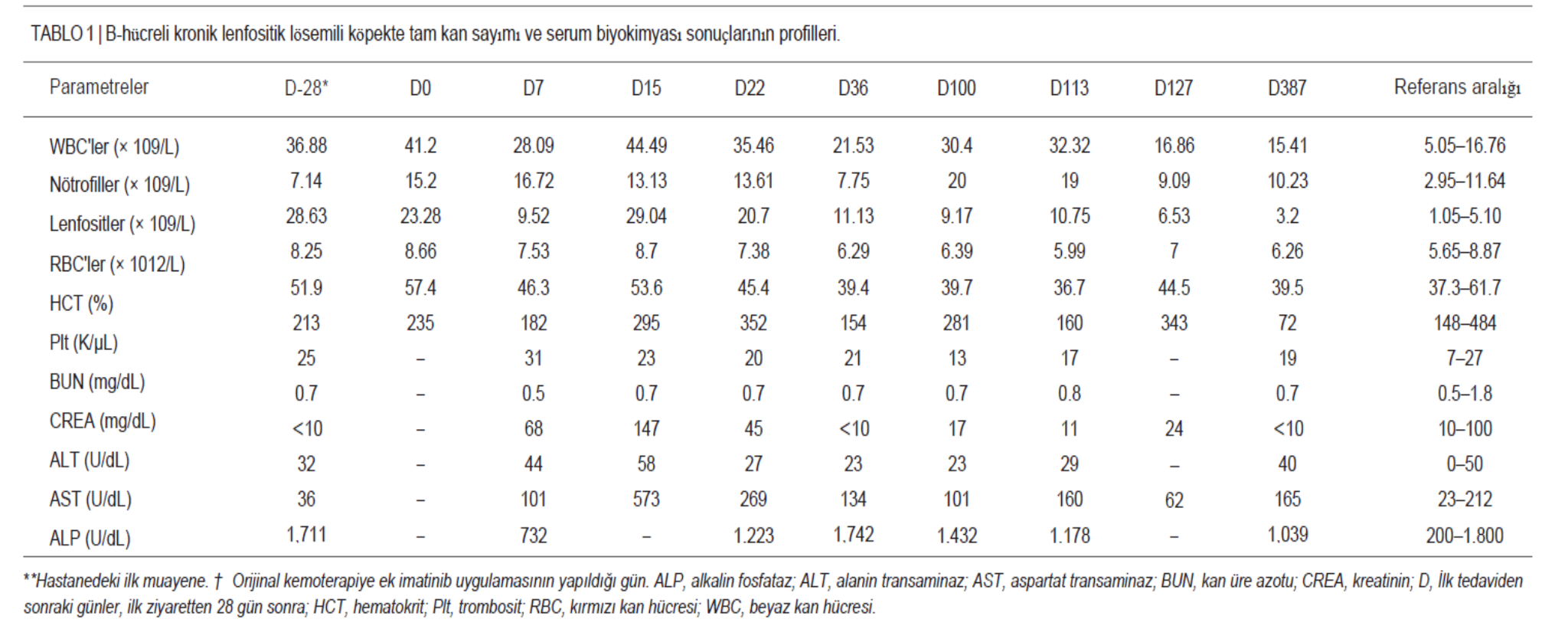
7 yaşındaki kısırlaştırılmış erkek Poodle cinsi köpek, 20 aydan uzun süredir devam eden ve giderek kötüleşen inatçı lenfositoz nedeniyle değerlendirilmek üzere sevk edilmiştir. Muayene öncesinde kalp kurdu, Lyme, Ehrlichia canis ve Anaplasma phagocytophilum için köpek SNAP 4Dx (IDEXX Laboratories, Westbrook, ME) testleri negatif çıktığı için spesifik enfeksiyonlar ekarte edilmiştir. Fizik muayenede köpekte hipertermi (rektal vücut ısısı: 39,4◦C) ve taşipne vardı. Palpasyonda yüzeysel lenf düğümlerinin boyutu normal bulundu. Hematolojik bulgular lökositoz, lenfositoz ve nötropeniyi içeriyordu (Tablo 1, Gün -28). Periferik kan yaymasında iyi diferansiye küçük lenfositler içeren lenfositoz ve nötropeni saptandı (Şekil 1A). Serum biyokimya sonuçları normal sınırlardaydı. Abdominal ultrasonografide hepatosplenomegali görüldü. Öncelikle kalıcı lenfositoza neden olabilecek kronik inflamasyon ve immün aracılı hastalıklar dışlandı ve lenfoproliferatif hastalıktan şüphelenildi. Bu nedenle, ilik infiltrasyonunu tanımlamak ve hematopoetik hücrelerin sitolojik tiplerini ve oranlarını değerlendirmek için kemik iliği aspirasyonu yapıldı. Kemik iliği aspirat sitolojisi hipersellülarite ve küçük boyutlu olgun lenfositlerle infiltrasyon gösterdi (Şekil 1B); lenfoid hücrelerin yüzdesi %45 idi. Kemik iliğinde lenfositoz için ayırıcı tanı ALL, KLL ve V. evre lenfoma olmuştur. Bunlar arasında, yukarıda belirtilen klinik muayene sonuçlarına dayanarak köpeğe KLL teşhisi konuldu.
Akış sitometrisi ile immünofenotipin değerlendirilmesi için hem kan hem de ilik örnekleri aşağıdaki T-lenfosit belirteçlerine özgü bir antiserum paneli ile boyanmıştır: [CD3
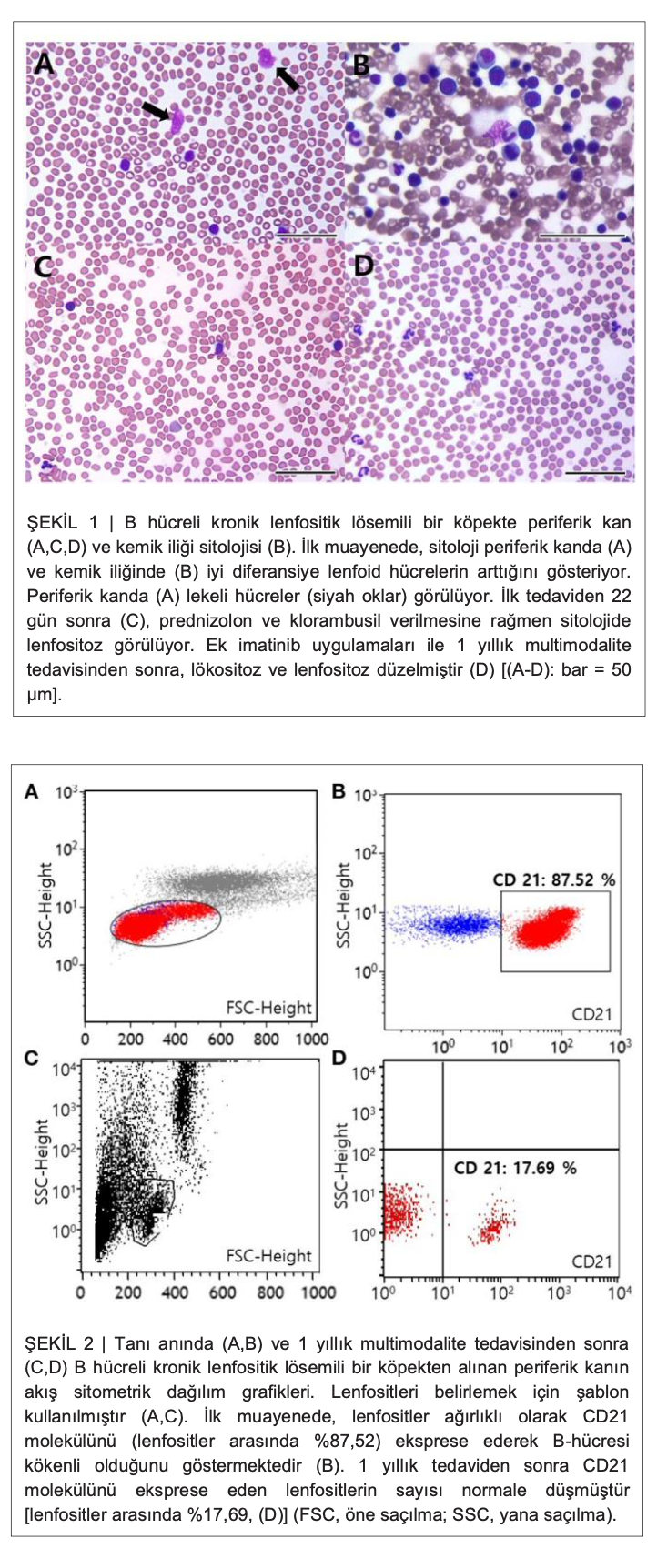
(CA17.2A12; Serotec Inc, Raleigh, NC, ABD), CD5 (YKIX322.3; Serotec Inc, Raleigh, NC, ABD), CD4 (YKIX302.9; Serotec Inc, Raleigh, NC, ABD) ve CD8 (YCATE55. 9; Serotec Inc, Raleigh, NC, ABD)], B-lenfosit belirteci CD21 (CA2.1D6; Serotec Inc, Raleigh, NC, ABD) ve öncü hücre belirteci CD34 (1H6; B- D Biosciences, San Jose, CA, ABD) (Colorado Eyalet Üniversitesi, Fort Collins, CO, ABD). Propidium iyodür boyamasıyla ölü hücrelerin ekarte edilmesinden sonra, lenfosit popülasyonları öne saçılma ve log yan saçılma grafikleri üzerinden değerlendirilmiştir (12). Neoplastik lenfositler ağırlıklı olarak CD21+ hücrelerden oluşmaktaydı ve sırasıyla kan örneğindeki tüm çekirdekli hücrelerin %66,73’ünü ve kemik iliği örneğindeki tüm çekirdekli hücrelerin %31,71’ini oluşturmaktaydı. Lenfositler arasında CD21 ekspresyonu olan hücreler sırasıyla kanda %87,52 ve kemik iliğinde %75,60 idi. Bu sonuçlar B hücreli KLL’ye işaret eden B hücresi kökenini ortaya koymuştur (Şekil 2A,B). Yukarıda bahsedildiği gibi diğer belirteçlerin ekspresyonu belirgin değildi. Ayrıca, yeniden düzenlenmiş antijen reseptör genlerini tespit ederek klonaliteyi saptamak amacıyla kan örnekleri kullanılarak antijen reseptör yeniden düzenlemeleri için polimeraz zincir reaksiyonu (PARR) analizi gerçekleştirilmiştir (Colorado Eyalet Üniversitesi, Fort Collins, CO, ABD). DNA kandan ekstrakte edilmiş ve antijen reseptörü hipervariable bölgesinin boyutu, B hücreleri için immünoglobulin ve T hücreleri için T-hücre reseptörü γ sekanslarının amplifikasyonu ile PCR yoluyla tespit edilmiştir (12). Köpeğin PARR sonuçları, belli başlı bantlarla immünoglobulin dizisine karşı pozitif reaksiyon gösterirken, B hücresi klonalitesini gösteren klonal bantlar olmaksızın T hücresi reseptörü γ dizisine karşı negatif reaksiyon göstermiştir.
Tedavi ve sonuç
Tedaviye ilk hasta kabulünden 28 gün sonra klorambusil (0.2 mg/kg, PO, QOD; Excella GmbH, Almanya) ve prednizolon (30 mg/m2 yüzey alanı, PO, SID; Daesung, Kore) ile başlanmıştır (Tablo 1, 0. Gün). Bir hafta sonra, klorambusil dozu 0.1 mg/kg’a (PO, QOD) ve prednizolon dozu 20 mg/m2’ye (PO, SID)düşürüldü. Bir hafta sonra, klorambusil dozu 0,1 mg/kg’a (PO, EOD) ve prednizolon dozu 10 mg/m2’ye (PO, EOD) düşürülmüştür. Ayrıca, yüksek karaciğer enzimlerinin kontrol altına alınması için karaciğer destek ilaçları (Zentonil; 0,1 T/kg, PO, bölünmüş; Vetoquinol, ABD.) ve ursodeoksikolik asit (10 mg/kg, PO, BID; Daewoong, Kore) içeren ek ilaçlar reçete edilmiştir.
Köpeğin lökosit ve lenfosit sayıları 3 haftalık klorambusil ve prednizolon kemoterapisinden sonra kayda değer bir şekilde düzelmedi (Şekil 1C). Ayrıca hipertermi, taşipne ve hepatosplenomegali gibi klinik bulgular da iyileşmedi. Bu nedenle, asıl tedaviye ek olarak imatinib (10 mg/kg, PO, SID; Novartis, İsviçre) uygulandı (Tablo 1, Gün 22). Kombine tedaviden iki hafta sonra, beyaz kan hücresi (WBC) sayısı 35,46 × 109/L’den 21,53 × 109/L’ye düşmüş ve miyelosupresyonu önlemek için imatinib dozu günde bir kezden gün aşırıya düşürülmüştür. Ayrıca, hipertermi düzelmiş ve köpek normal vücut sıcaklığına kavuşmuştur (rektal sıcaklık: 38,9◦C). Ancak, 9 hafta sonra WBC sayısı 30,4 × 109/L’ye yükselmiştir (Tablo 1, 100. Gün).
Bu nedenle imatinib dozu günde bir defaya çıkarılmıştır. 2 hafta sonra, WBC sayısı 30.4 × 109/L’den 32.32 × 109/L’ye yükselmiş ve miyelosupresyonun yan etkisi olarak hafif anemi (HCT %36.7; referans aralığı, %37.3-61.7) ortaya çıkmıştır. Yan etkinin kötüleşmesi göz önünde bulundurularak, imatinib dozu günde bir kezden 3 günlük döngü halinde 2 gün başlama ve 1 gün bırakma şeklinde değiştirilmiştir. Ayrıca, ek imatinib uygulamasından 18 gün sonra, c-kit geninde tespit edilen mutasyonları kontrol etmek için kan örneğinde c-kit mutasyonu testi yapıldı (Colorado Eyalet Üniversitesi, Fort Collins, CO, ABD). Köpekte c-kit mutasyonu olmadığını gösteren c-kit ekzon 8 ve 11’de dahili tandem duplikasyon yoktu. 2 hafta sonra, WBC sayısı dramatik bir şekilde 16,86 × 109/L’ye düşmüş ve anemi iyileşmiştir (Tablo 1, 127. Gün). Bu köpeğin WBC ve lenfosit sayısı mevcut tedavi rejimi ile gayet iyi şekilde kontrol altına alınmıştır. 386. günde, WBC sayısı normal aralıktaydı (15,41 × 109/L; referans aralığı, 5,05-16,76 × 109/L) ve lenfosit sayısı da normal aralıktaydı (3,2 × 109/L; referans aralığı, 1,05-5,1 × 109/L; Şekil 1D).
Tedaviye başladıktan yaklaşık 1 yıl sonra, güncel tedavi yanıtını değerlendirmek için akış sitometrisi yeniden ölçülmüştür (Şekil 2C). CD21 molekülünü eksprese eden hücrelerin sayısı ilk hasta kabul tarihinde 24.678/μL iken 704/μL’ye (referans aralığı, 85-350) düşerek ilaç tedavisine son derece olumlu yanıt verdiğini kanıtlamıştır (Şekil 2D). Köpek 2 yıl boyunca klorambusil, prednizolon ve imatinib ile tedaviye iyi yanıt vermiş ve klinik bakımdan iyi durumda seyretmiştir.
TARTIŞMA
Prednizon, klorambusil ve vinkristin ile tedavi edilen 17 KLL’li köpek arasında KLL’li köpekler için ortalama sağkalım süresi ∼1 yıl şeklinde rapor edilmiştir (13) ve başka bir raporda B hücreli KLL’li 17 köpeğin ortalama genel sağkalım süresinin 480 gün olduğu belirtilmiştir (9). KLL’nin kötü prognostik faktörleri arasında büyük B hücre tipi, <8 yaşındaki genç köpekler, Richter sendromu gelişimi, immün aracılı hemolitik anemi ve saf kırmızı hücre aplazisi gibi paraneoplastik sendromlar ve CD8+ fenotipinde 30.000 lenfosit/μL’den fazla lenfositoz yer almaktadır (1, 9, 12, 14). Bu vakadaki köpek, <8 yaş dahil olmak üzere kötü prognostik faktörler taşıyordu, ancak klorambusil, prednizolon ve imatinib kombinasyon tedavisine verdiği klinik yanıt, ciddi yan etkiler olmaksızın 2 yıllık takip süresi boyunca mükemmeldi.
Küçük moleküllü tirozin kinaz inhibitörü olan imatinib, başlangıçta insan kronik miyeloid lösemisinin tedavisi için geliştirilmiştir ve mast hücre tümörleri gibi neoplazmları olan köpek ve kedilerde endikasyon dışı kullanılmaktadır (15). İmatinib, tirozin kinaz mutasyonları olan köpek ve kedilerde faydalı olabilir çünkü imatinibin terapötik etkisi KIT’in aktivasyonuna bağlıdır (15). İmatinibin KLL hücrelerini klorambusilin sitotoksik etkilerine karşı hassaslaştırabildiği ve in vitro KLL hücrelerinde apoptozu indükleyebildiği rapor edilmiştir (16). İmatinib, c-ABL kinaz aktivitesini inhibe ederek Rad51 fosforilasyonunda azalmaya neden olur ve klorambusil
kaynaklı DNA hasarının onarılmasını sağlar (16). KLL hastalarının insanlarda c-ABL artışı görülme olasılığı daha yüksektir (17, 18). Ayrıca, insanlarda yapılan bir vaka çalışmasında, imatinibin KLL ve kronik miyelojenöz lösemi tedavisinde etkili bir şekilde kullanıldığı ve periferik kan KLL hücrelerinde azalma görüldüğü bildirilmiştir (19). Veteriner hekimlikte imatinib ile tedavi edilen köpeklerde KLL’nin klinik yanıtını gösteren herhangi bir çalışma olmamasına rağmen, imatinibin KLL’li insanlarda klinik etkinliğinin kanıtlanmış olması ve imatinibin in vivo klorambusilin sitotoksik etkisini sinerjik olarak indükleme yeteneğine sahip olması nedeniyle imatinibin köpeklerde de benzer etkinlik göstereceğini varsaydık. Bu nedenle, bu vakada prednizolon ve klorambusil içeren asıl tedaviye imatinib eklenmiş ve KLL, WBC seviyelerinin normalleşmesiyle birlikte gayet iyi kontrol altına alınmıştır. Bu vakadaki köpekte c-kit ekzon 8 ve 11’de internal tandem duplikasyon olmamasına rağmen, bu durum c-kit mutasyonu olmadığını göstermektedir, köpeğin tedavi sonucu olumludur. Bu nedenle, klorambusile kötü yanıt veren KLL’li köpekler için, c-kit mutasyonuna bakılmaksızın ek olarak imatinib uygulanabilir. Ayrıca, imatinib ile kombinasyon halinde klorambusil tedavisinin maliyeti, sistemik parenteral kemoterapiye kıyasla pratikte daha uygundur.
Bu köpekte ilk muayenede lenfositozu karakterize etmek ve 1 yıl sonra multimodalite tedavi yanıtını değerlendirmek amacıyla iki kez akış sitometrik analiz yapılmıştır. Ağırlıklı olarak CD21 molekülünü eksprese eden lenfositlerin sayısı 1 yıllık tedavinin ardından belirgin şekilde normale düşmüştür.
Sonuç olarak, bu vaka raporu imatinib ile birlikte klorambusil ve prednizolon ile tedavi edilen KLL’li köpeklerin tedavi sonrası klinik yanıtını ortaya koymaktadır. Yazarların bildiği kadarıyla, bu multimodalite ilaçla tedavi edilen köpeklerde KLL’nin klinik sonuçlarını gösteren herhangi bir çalışma bulunmamaktadır. Bu vaka raporu, bu kombinasyonun iyi tolere edildiğini ve tedavi dozajının WBC sayısına göre uygun şekilde ayarlanması halinde köpek KLL’sinde olumlu yönde antikanser etki gösterebileceğini ortaya koymaktadır.
VERİ ERİŞİM BEYANI
Çalışmada yer alan ve sunulan özgün katkılar makale/ek materyalde yer almaktadır, daha detaylı bilgi için ilgili yazar/yazarlara başvurulabilir.
ETİK İNCELEME VE ONAY BEYANI
Hayvan üzerinde yapılan çalışma için etik inceleme ve onay gerekmemiştir çünkü bu vaka raporunun ve eşlik eden görsellerin yayınlanması için köpeğin gerçek sahibinden bilgilendirilmiş onam alınmıştır.
KATKIDA BULUNAN YAZARLAR
G-WL vaka analizinde yer almış ve makalenin yazımından sorumlu olmuştur. M-HK ve J-HJ taslağın hazırlanmasında ve vaka analizinde yer almıştır. D-WS, W-BR ve H-SK vaka
analizinde ve makalenin gözden geçirilmesinde yer almıştır. H-MP vakanın koordinasyonunda yer almış ve sonuçların yorumlanmasından sorumlu olmuştur. Tüm yazarlar makaleye katkıda bulunmuş ve sunulan versiyonu onaylamıştır.
TEŞEKKÜRLER
Yazarlar Klinik İmmünoloji Laboratuvarı’na (Colorado Eyalet Üniversitesi, Fort Collins, CO, ABD) hasta kabulündeki sitometri grafiklerinin hazırlanması için teşekkür etmeyi bir borç bilirler.
KAYNAKÇA
- Workman HC Vernau W. Chronic lymphocytic leukemia in dogs and cats: the veterinary perspective. Vet Clin North Am Small Anim Pract. (2003) 33:1379–99. doi: 10.1016/S0195-5616(03)00120-7
- Kleiter M, Hirt R, Kirtz G, Day M. Hypercalcaemia associated with chronic lymphocytic leukaemia in a giant schnauzer. Aust Vet J. (2001) 79:335– 8. doi: 10.1111/j.1751-0813.2001.tb12007.x
- Fujino Y, Sawamura S, Kurakawa N, Hisasue M, Masuda K, Ohno K, et al. Treatment of chronic lymphocytic leukaemia in three dogs with melphalan and prednisolone. J Small Anim Pract. (2004) 45:298– 303. doi: 10.1111/j.1748-5827.2004.tb00239.x
- Hallek M, Shanafelt TD, Eichhorst B. Chronic lymphocytic leukaemia. Lancet. (2018) 391:1524–37. doi: 10.1016/S0140-6736(18)30422-7
- Bromberek J, Rout E, Agnew M, Yoshimoto J, Morley P, Avery A. Breed distribution and clinical characteristics of B cell chronic lymphocytic leukemia in dogs. J Vet Intern Med. (2016) 30:215–22. doi: 10.1111/jvim.13814
- Vernau W Moore PF. An immunophenotypic study of canine leukemias and preliminary assessment of clonality by polymerase chain reaction. V et Immunol Immunopathol. (1999) 69:145– 64. doi: 10.1016/S0165-2427(99)00051-3
- Withrow SJ, Vail DM, Page R. Withrow and MacEwen’s Small Animal Clinical Oncology-E-Book. St. Louis, MS: Elsevier Health Sciences (2013).
- Giantin M, Aresu L, Arico A, Gelain M, Riondato F, Martini V, et al. Evaluation of tyrosine-kinase receptor c-KIT (c-KIT) mutations, mRNA and protein expression in canine leukemia: might c-KIT represent a therapeutic target? Vet Immunol Immunopathol. (2013) 152:325– 32. doi: 10.1016/j.vetimm.2013.01.003
- Comazzi S, Gelain M, Martini V, Riondato F, Miniscalco B, Marconato L, et al. Immunophenotype predicts survival time in dogs with chronic lymphocytic leukemia. J Vet Intern Med. (2011) 25:100– 6. doi: 10.1111/j.1939-1676.2010.0640.x
- Jain N O’Brien S. Targeted therapies for CLL: practical issues with the changing treatment paradigm. Blood Rev. (2016) 30:233– 44. doi: 10.1016/j.blre.2015.12.002
- Awan FT Byrd JC. New strategies in chronic lymphocytic leukemia: shifting treatment paradigms. Clin Cancer Res. (2014) 20:5869– 74. doi: 10.1158/1078-0432.CCR-14-1889
- Williams M, Avery A, Lana S, Hillers K, Bachand A, Avery P. Canine lymphoproliferative disease characterized by lymphocytosis: immunophenotypic markers of prognosis. J Vet Intern Med. (2008) 22:596– 601. doi: 10.1111/j.1939-1676.2008.0041.x
- Leifer C Matus R. Chronic lymphocytic leukemia in the dog: 22 cases (1974- 1984). J Am Vet Med Assoc. (1986) 189:214–7.
- Comazzi S, Martini V, Riondato F, Poggi A, Stefanello D, Marconato L, et al. Chronic lymphocytic leukemia transformation into high- grade lymphoma: a description of richter’s syndrome in eight
dogs. V et Comp Oncol. (2017) 15:366–73. doi: 10.1111/vco.1 2172
- Bonkobara M. Dysregulation of tyrosine kinases and use of imatinib in small animal practice. Vet J. (2015) 205:180–8. doi: 10.1016/j.tvjl.2014.12.015
- Aloyz R, Grzywacz K, Xu Z-Y, Loignon M, Alaoui-Jamali
MA, Panasci L. Imatinib sensitizes CLL lymphocytes to chlorambucil. Leukemia. (2004) 18:409–14. doi: 10.1038/sj.leu.240 3247
- Lin K, Glenn MA, Harris RJ, Duckworth AD, Dennett S, Cawley JC, et al. c-Abl expression in chronic lymphocytic leukemia cells: clinical and therapeutic implications. Cancer Res. (2006) 66:7801– 9. doi: 10.1158/0008-5472.CAN-05-3901
- Giannopoulos K, Karczmarczyk A, Karp M, Bojarska-Junak A, Kosior K, Kowal M, et al. In vivo, ex vivo and in vitro dasatinib activity in chronic lymphocytic leukemia. Oncol Lett. (2021) 21:285. doi: 10.3892/ol.2021.12546
- Yoon JY, Kumar R, Aloyz R, Johnston JB. Response of concomitant chronic myelogenous leukemia and chronic lymphocytic leukemia to imatinib mesylate. Leuk Res. (2011) 35:e179–80. doi: 10.1016/j.leukres.2011.06.007
Çıkar Çatışması Beyanı: Yazarlar, araştırmanın herhangi bir ticari veya finansal çıkar çatışması olarak yorumlanabilecek herhangi bir ilişki olmaksızın yürütüldüğünü beyan etmişlerdir.
Yayıncının Notu: Bu makalede ifade edilen tüm iddialar yalnızca yazarlara aittir ve bağlı oldukları kuruluşların veya yayıncının, editörlerin ve hakemlerin görüşlerini temsil etmeyebilir. Bu makalede değerlendirilebilecek herhangi bir ürün veya üreticisi tarafından ileri sürülebilecek herhangi bir iddia, yayıncı tarafından onaylanmamış veya herhangi bir garanti verilmemiştir.
Telif Hakkı © 2022 Lee, Kang, Jeon, Song, Ro, Kim ve Park. Bu, Creative Commons Attribution License (CC BY) koşulları altında dağıtılan açık erişimli bir makaledir. Orijinal yazar(lar)a ve telif hakkı sahip(ler)ine atıfta bulunulması ve bu dergideki orijinal yayına atıfta bulunulması koşuluyla, kabul görmüş akademik uygulamalara uygun olarak diğer forumlarda kullanılmasına, dağıtılmasına veya çoğaltılmasına izin verilir. Bu şartlara uymayan hiçbir kullanım, dağıtım veya çoğaltmaya izin verilmez.