| AÇIK ERİŞİM Makaleye atıfta bulunmak için: London CA, Gardner HL, Mathie T, Stingle N, Portela R, Pennell ML, et al. (2015) Impact of Toceranib/Piroxicam/Cyclophosphamide Maintenance Therapy on Outcome of Dogs with Appendicular Osteosarcoma following Amputation and Carboplatin Chemotherapy: A Multi-Institutional Study. PLoS ONE 10(4): e0124889. doi:10.1371/journal.pone.0124889 Akademik Editor: Daniel Bouvard, Institut Albert Bonniot-INSERMU823, FRANSA Telif Hakkı: © 2015 London et al. Bu makale, orijinal yazar ve kaynağa atıfta bulunulması koşuluyla, herhangi bir ortamda sınırsız kullanım, dağıtım ve çoğaltmaya izin veren Creative Commons Attribution License koşulları altında dağıtılan açık erişimli bir makaledir. Veri Erişim Beyanı: İlgili tüm veriler makalede ve Ek Bilgi dosyasında yer almaktadır. Finansman: Bu proje aşağıdaki fonlar ile desteklenmiştir: Translasyonel Bilimleri Geliştirme Ulusal Merkezi’nden UL1TR001070 ve Ulusal Kanser Enstitüsü’nden Ohio Eyalet Üniversitesi’ne P30CA016058. Bu klinik çalışma ve tedavi edilen köpekler için toceranib finansmanı Zoetis tarafından sağlanmıştır |
| 1 Veteriner Biyobilimleri ve Veteriner Klinik Bilimleri Bölümleri, Veteriner Hekimliği Fakültesi, Ohio Eyalet Üniversitesi, Columbus, Ohio, Amerika Birleşik Devletleri, 2 Veteriner Klinik Tıp Bölümü, Urbana-Champaign’deki Illinois Üniversitesi, Veteriner Fakültesi, Champaign, Illinois, Amerika Birleşik Devletleri, 3 Biyoistatistik Bölümü, Halk Sağlığı Fakültesi, Ohio Eyalet Üniversitesi, Columbus, Ohio, Amerika Birleşik Devletleri, 4 Hope Veteriner Hekimleri, Malvern, Pennsylvania, Amerika Birleşik Devletleri, 5 Veteriner Kanser Derneği, Tustin, Kaliforniya, Amerika Birleşik Devletleri, 6 Tıp Bilimleri Bölümü, Veteriner Hekimliği Fakültesi, Wisconsin Üniversitesi, Madison, Madison, Wisconsin, Amerika Birleşik Devletleri, 7 Klinik Bilimler Bölümü, Veteriner Hekimliği Fakültesi, Kuzey Carolina Eyalet Üniversitesi, Raleigh, Kuzey Carolina, Amerika Birleşik Devletleri, 8 New England Veteriner Onkoloji Grubu, Waltham, Massachusetts, Amerika Birleşik Devletleri, 9 Küçük Hayvan Klinik Bilimleri Bölümü, Veteriner Hekimliği Fakültesi, Teksas A&M Üniversitesi, Üniversite Kampüsü, Teksas, Amerika Birleşik Devletleri, 10 Veteriner Hekimliği Klinik Bilimleri Bölümü, Minnesota Üniversitesi Veteriner Hekimliği Fakültesi, St. Paul, Minnesota, Amerika Birleşik Devletleri, 11 Veteriner Hekimliği ve Cerrahisi Bölümü, Veteriner Hekimliği Fakültesi, Missouri Üniversitesi, Columbia, Missouri, Amerika Birleşik Devletleri, 12 Oradell Hayvan Hastanesi, Paramus, New Jersey, Amerika Birleşik Devletleri, 13 Güneydoğu Veteriner Onkolojisi ve Tıbbı, Orange Park, Florida, Amerika Birleşik Devletleri, 14 Küçük Hayvan Hekimliği ve Cerrahisi Bölümü, Georgia Üniversitesi, Veteriner Hekimliği Fakültesi, Atina, Georgia, Amerika Birleşik Devletleri, 15 Sage Veterinerlik Uzmanlık ve Acil Bakım Merkezleri, Concord, Kaliforniya, Amerika Birleşik Devletleri, 16 VCA Katonah Bedford Veteriner Kliniği, Bedford Hill, New York, Amerika Birleşik Devletleri, 17 Güneybatı Veteriner Onkolojisi, Tucson, Arizona, Amerika Birleşik Devletleri, 18 Veterinerlik İhtisas Hastanesi Carolinas, Cary, Kuzey Carolina, Amerika Birleşik Devletleri, 19 Klinik Bilimler Bölümü, Veteriner Hekimliği ve Biyomedikal Bilimler Fakültesi, Colorado Eyalet Üniversitesi, Fort Collins, Colorado, Amerika Birleşik Devletleri, 20 Veterinerlik İhtisas Hastanesi, San Diego, Kaliforniya, Amerika Birleşik Devletleri, 21 Veteriner Kanser Merkezi, Norwalk, Connecticut, Amerika Birleşik Devletleri
☯ Söz konusu yazarlar bu çalışmaya eşit oranda katkıda bulunmuşlardır. |
ÖzetGerekli BilgilerAmputasyon ve karboplatin kemoterapisini takiben apendiküler osteosarkomlu (OSA) köpeklerde metronomik siklofosfamid/piroksikam tedavisine toceranib eklenmesinin hastalıksız geçen süreyi (DFI) ve genel sağkalımı (OS) önemli ölçüde iyileştireceği varsayılmıştır. Metod ve BulgularBu çalışma, ağır metastatik hastalığı olmayan OSA’lı köpeklerin (n = 126) amputasyonu takiben karboplatin kemoterapisi (4 doz) aldığı randomize, prospektif bir klinik çalışmadır. Çalışmaya girişte, köpekler kemoterapiyi tamamladıktan sonra toceranib ile birlikte veya toceranib olmadan piroksikam/siklofosfamid (n = her biri 63) almak üzere randomize edilmiştir. Hasta demografik özellikleri her iki grup arasında istatistiksel olarak anlamlı farklılık göstermemiştir. Karboplatin kemoterapisi sırasında veya hemen sonrasında 32 köpekte (n = 13 toceranib; n = 19 kontrol) metastatik hastalık gelişmiş ve 13 köpek diğer tıbbi durumlar veya hasta sahibinin tercihi nedeniyle çalışmadan ayrılmıştır. Karboplatin kemoterapisinin ardından 81 köpek (n = 46 toceranib; n = 35 kontrol) metronomik tedavi almış; 35 köpekte (n = 20 toceranib; n = 15 kontrol) idame tedavisi sırasında metastatik hastalık gelişmiş ve 26 köpek diğer tıbbi durumlar veya hasta sahibinin tercihi nedeniyle çalışmadan ayrılmıştır. Dokuz toceranib ile tedavi edilen ve 11 kontrol köpeği amputasyondan 1 yıl sonra metastatik hastalık kanıtı olmadan çalışmayı tamamlamıştır. Toceranib ile tedavi edilen köpeklerde kontrol köpeklerine kıyasla daha fazla ishal, nötropeni ve kilo kaybı vakası görülmüştür, ancak bu toksisiteler düşük dereceli olup tipik olarak destekleyici bakım ile düzelmiştir. Kontrol köpeklerine (n = 1) kıyasla daha fazla toceranib ile tedavi edilen köpek (n = 8) tedaviyle ilişkili yan etkiler nedeniyle çalışmadan çıkarılmıştır. Kontrol grubu ve toceranib ile tedavi edilen köpekler için ortalama hastalıksız geçen süre (DFI) sırasıyla 215 ve 233 gün (p = 0,274); kontrol grubu ve toceranib ile tedavi edilen köpekler için ortalama genel sağkalım (OS) sırasıyla 242 ve 318 gün (p = 0,08) olmuştur. Kontrol grubu köpekler için bir yıllık sağkalım oranı %35 iken, toceranib alan köpekler için bu oran %38’dir. SonuçAmputasyon ve karboplatin kemoterapisini takiben metronomik piroksikam/siklofosfamid tedavisine toceranib eklenmesi, OSA’lı köpeklerde ortalama DFI, OS veya 1 yıllık sağkalım oranını iyileştirmemiştir. |
GirişOsteosarkom (OSA) köpeklerde en sık görülen primer kemik tümörüdür ve rapor edilen tüm kemik neoplazilerinin %85’ini oluşturmaktadır [1]. Yalnızca amputasyon ile ortalama sağkalım süreleri 4-5 aya yaklaşırken, adjuvan kemoterapi ile ortalama sağkalım süreleri 8-12 aya çıkmaktadır [2]. Çeşitli kemoterapi protokollerinin ve yeni tedavi yaklaşımlarının kullanılmasına rağmen, sağkalımda klinik olarak anlamlı iyileşmeler sağlanamamıştır ve köpeklerin %90’ı tedaviden sonraki 2 yıl içinde metastatik hastalık nedeniyle ölmektedir [3-8]. OSA’lı köpeklerin çoğunun başlangıçta mikroskobik metastatik hastalığa sahip olduğu göz önüne alındığında, terapötik gelişimin bir diğer amacı da metastatik tümör hücrelerinin büyümesi için kritik olan tümör mikro-çevresindeki faktörleri etkilemek olmuştur. Özellikle, standart sitotoksik tedavi yaklaşımlarına alternatif olarak bağışıklık tepkilerinin modüle edilmesi ve tümörün kan kaynağı gibi kritik unsurlara erişiminin değiştirilmesi yönünde çabalar sarf edilmiştir. Veteriner hekimlikte, metronomik kemoterapi tipik olarak piroksikam ve düşük doz siklofosfamidden oluşmaktadır ve çeşitli yayınlar bu yaklaşımla hem tümör mikroçevresinin hem de immün yanıtın modülasyonunu ortaya koymuştur [9-11]. Hem veteriner hekimliğinde hem de insan tıbbında, metronomik siklofosfamidin CD4+ Treg’leri aşağı regüle ettiği görülmüştür [11,12]. Yumuşak doku sarkomu olan köpeklerde 15 mg/m2/gün dozunda uygulanan metronomik siklofosfamid de tümör mikrodamar yoğunluğunda azalma ile ilişkilendirilmiştir [11]. Ayrıca, metronomik siklofosfamidin dolaşımdaki endotel öncüllerinin (CEP’ler) mobilizasyonunu ve canlılığını azalttığı görülmüştür [13,14]. NSAİİ’ler çoğu insan metronomik kemoterapi protokolünde yer almazken, piroksikam veteriner hekimlikte sıklıkla kullanılmaktadır, çünkü CEP’lerde COX- 2 ekspresyonunun hayatta kalmaları için önemli olduğu öne sürülmüştür. Bu nedenle COX-2 inhibisyonu, CEP’lerin tümör mikroçevresinde hayatta kalma ve çoğalma yeteneğini azaltabilir [15]. Köpek melanom kseno-greftleri olan farelerde metronomik siklofosfamid ile piroksikam kombinasyonu, tümör mikrodamar yoğunluğunda azalma, VEGF sekresyonunda azalma ve TSP-1 sekresyonunda artış ile sonuçlanmış ve metronomik kemoterapi ile NSAID’lerin eş zamanlı kullanılmasına yönelik görüşleri desteklemiştir [16]. Tümör anjiyogenezi ile ilgili olarak, vasküler endotelyal büyüme faktörü (VEGF) ve reseptörünün (VEGFR) bu süreçte kritik rol oynadığı bilinmektedir. Endotel hücrelerinde VEGFR’nin aktivasyonu, endotel hücre sağkalımını, vasküler geçirgenliğin artmasını ve CEP’lerin mobilizasyonunu teşvik eden çoklu sinyal yollarını uyarır. Tümör hücreleri VEGF üretimi yoluyla VEGFR2 eksprese eden CEP’lerin kemik iliğinden tümör mikroçevresine göçünü sağlayabilir ve anti-VEGF/VEGFR tedavisinin sağkalım sinyalini ve CEP’lerin tümör büyüme bölgesine mobilizasyonunu azalttığı görülmüştür [17-20]. VEGF hem insan hem de köpek OSA’sında tespit edilebilir ve bu durum, malign potansiyelin artması ve kötü prognoz ile ilişkilendirilmiştir [21-25]. İnsan kanser tedavisinde, küçük moleküller sunitinib, sorafenib ve pazopanib ve monoklonal antikor bevacizumab dahil olmak üzere VEGF/VEGFR sinyal ekseninin birkaç onaylı inhibitörü mevcuttur. Bu ilaçlar fare modellerinde kayda değer aktivite gösterirken, insanlarda anjiyogenez ve tümör progresyonu üzerindeki etkileri tartışmaya açıktır [26-29]. OSA ile ilgili olarak, birkaç çok hedefli VEGF inhibitörü OSA’nın murin ksenograft modellerinde değerlendirilmiş ve antitümör aktivite göstermiştir [30,31]. Ayrıca, gefitinib ile kombine edilen cediranib, OSA’lı bir hasta da dahil olmak üzere solid tümörlü hastalarda antitümör aktivite ve VEGF ve VEGFR2 seviyelerinde değişiklikler sergilemiştir [32]. Toceranib phosphate (toceranib; Palladia), VEGFR, PDGFR, KIT ve FLT-3 dahil olmak üzere çeşitli reseptör tirozin kinazların (RTK’lar) çok hedefli küçük moleküllü bir inhibitörüdür ve oral yoldan biyolojik olarak kullanılabilir bir anti-anjiyojenik ajan olarak geliştirilmiştir [33-35]. Tseranib, KIT inhibisyonu sayesinde köpek mast hücre tümörlerinin tedavisi için onaylanmış olsa da, muhtemelen toceranib tarafından inhibe edilen diğer RTK’ların düzensizliği nedeniyle köpeklerde de çeşitli tümörlere karşı aktivite görülmüştür [33,36]. Daha önce yayınlanan veriler, gün aşırı verilen 2,4-2,75 mg/kg toceranib dozlarının VEGFR2 inhibisyonunun taşıyıcı biyobelirteci olan plazma VEGF’de istatistiksel olarak anlamlı artışlar ile sonuçlandığını göstermektedir [37]. Bu nedenle, şu anda çeşitli tümörler için köpekleri tedavi etmek amacıyla kullanılan toceranib dozlarının da buna benzer bir etkiye sahip olması beklenmektedir. Metastatik OSA ortamında, retrospektif bir çalışma, toceranib tedavisini takiben köpeklerin yaklaşık %48’inin klinik fayda (esas olarak stabil hastalıktan meydana gelen) gördüğünü göstermiştir [38]. Bu çalışmada, köpeklerin çoğu toceranib ile birlikte metronomik siklofosfamid ve/veya bir NSAID ile de tedavi edilmiştir. Daha yakın zamanda, toceranibin kanserli köpeklerde dolaşım halindeki düzenleyici T hücrelerinin seviyelerini düşürdüğü görülmüştür, bu da tümörler üzerindeki etkilerinin bir kısmının immünomodülasyon yoluyla ortaya çıkabileceğini düşündürmektedir [39]. Metronomik kemoterapi ve VEGF/ VEGFR inhibitörlerinin potansiyel tamamlayıcı etkileri göz önüne alındığında, insan tıbbında farklı sonuçlarla kombine edilmişlerdir [26,40-42]. Bununla birlikte, ileri evre meme kanseri olan kadınlarda, kapesitabin veya metotreksat ile bevasizumb ve siklofosfamid kombinasyonları kullanılarak kayda değer sayıda hastada (%63,6-68) klinik fayda sağlandığı kanıtlanmıştır [26,42]. Bu veriler, anti-anjiyojenik hedefe yönelik tedavilerle birlikte sürekli düşük doz metronomik kemoterapi uygulanmasının mikroskobik metastatik hastalığı ele almak için geçerli bir strateji olabileceğini göstermektedir. Bu nedenle, bu klinik çalışmanın amacı, amputasyon ve karboplatin kemoterapisini takiben apendiküler OSA’lı köpeklerde metronomik siklofosfamid ve piroksikam ile kombine edilen toceranib fosfatın hastalıksız aralık (DFI) ve genel sağkalım (OS) üzerindeki etkisini değerlendirmektir. |
Materyal ve MetodUygunluk ve Etik Beyan Ohio Eyalet Üniversitesi Veteriner Hekimliği Fakültesi Klinik Araştırma ve Danışma Komitesi ve Ohio Eyalet Üniversitesi Kurumsal Hayvan Bakım ve Kullanım Komitesi (IACUC) bu çalışmayı onaylamıştır. IACUC onayı ayrıca Wisconsin-Madison Üniversitesi, North Carolina Eyalet Üniversitesi, Texas A&M Üniversitesi, Minnesota Üniversitesi, Missouri Üniversitesi, Georgia Üniversitesi ve Colorado Eyalet Üniversitesi’nden de alınmıştır. Bu klinik araştırmaya katılan özel uzmanlık uygulamaları IACUC onayı gerektirmemektedir; klinik araştırmaya katılım, bu çalışma sahalarında baş araştırmacı olarak belirlenen Veteriner Tıbbi Onkoloğun takdirine bağlıydı (Hope Veteriner Uzmanları, Malvern, PA; Veteriner Kanser Topluluğu, Tustin, CA; New England Veteriner Onkoloji Topluluğu, Waltham, MA; Oradell Hayvan Hastanesi, Paramus, NJ; Güneydoğu Veteriner Onkoloji ve Tıp, Orange Park, FL; Sage Veteriner Uzmanlık ve Acil Bakım Merkezleri, Concord, CA; VCA Katonah Bedford Veteriner Merkezi, Bedford Hill, NY; Güneybatı Veteriner Onkoloji, Tuc- son, AZ; Carolinas Veteriner Uzmanlık Hastanesi, Cary, NC; Veteriner Uzmanlık Hastanesi, San Diego, CA; Veteriner Kanser Merkezi, Norwalk, CT). Çalışmaya katılmadan önce tüm hasta sahiplerinden bilgilendirilmiş onam alınmıştır. Histolojik olarak doğrulanmış apendiküler osteosarkomu olan ve amputasyon geçirmiş gros metastatik hastalığı olmayan köpeklerin kayıtları kabul edilmiştir. Sadece uzun kemikleri içeren apendiküler bölgeler çalışmaya dahil edilmiştir. Kayıt öncesinde köpeklere torasik radyografiler, tam kan sayımı (CBC), serum biyokimya profili ve idrar tahlili gibi tanısal testler uygulanmıştır. Daha önce radyoterapi veya kemoterapi tedavisi görmüş veya karboplatin kemoterapisine başladıktan sonraki 72 saat içinde non-steroid anti-enflamatuar (NSAID) ilaçlar almış olan köpekler çalışmaya dahil edilmemiştir. |
Çalışma TasarımıAmputasyon sonrası histolojik olarak doğrulanmış apendiküler osteosarkomu olan ve gross metastatik hastalık kanıtı bulunmayan toplam 126 köpek bu çalışmaya dahil edilmiştir. Çalışmaya başlamadan önce bilgisayar ortamında oluşturulmuş randomizasyon tablosu hazırlanmış ve hastalar kaydedildikçe çalışma grubu atamaları bu tabloya göre yapılmıştır. Kayıt sonrasında, köpekler karboplatin kemoterapisini tamamladıktan sonra toceranib (Zoetis, Florham Park, NJ tarafından sağlanmıştır) içeren veya içermeyen piroksikam/siklofosfamid almak üzere randomize edilmiştir. Tüm köpekler amputasyondan sonraki 14 gün içinde her üç haftada bir 4 kür tek ajan karboplatin (300 mg/m2 IV) ile tedaviye başlamıştır. Dördüncü karboplatin tedavisinden önce köpekler toraks radyografileri ile yeniden değerlendirilmiştir. Pulmoner metastatik hastalık kanıtı olmayan köpekler 0,3 mg/kg PO EOD piroksikam ve 10 mg/m2 PO EOD siklofosfamid (toceranib ile dönüşümlü dozlama günü) ile birlikte veya toceranib olmadan 2,75 mg/kg PO gün aşırı (EOD) oral idame tedavisine başlamıştır; oral tedaviye dördüncü karboplatin tedavisinin tamamlanmasından 3 hafta sonra başlanmıştır. Oral idame tedavisinin başlangıcında tüm köpeklere her 12 saatte bir 0,5 mg/kg PO famotidin verilmiştir. Klorambusil, steril hemorajik sistit durumunda siklofosfamid yerine 5 mg/m2 PO EOD olarak uygulanmıştır. Köpekler oral idame tedavisine başladıktan 2 hafta sonra, sonraki 8 ay boyunca veya progresif hastalık kaydedilene kadar her 4 haftada bir değerlendirildi. CBC ve biyokimya profili her 4 haftada bir yapıldı; idrar tahlili oral idame tedavisine başladıktan sonra her 16 haftada bir alındı. Her 8 haftada bir toraks radyografileri ile yeniden görüntüleme yapıldı. |
İlaç Çeşitleri ve Eşlik Eden İlaçlarSiklofosfamid ve piroksikam, Apothecary Shoppe (şimdi Avella Specialty Pharmacy, Columbus, OH) tarafından birleştirilmiş ve doğrudan sahiplerine postalanmıştır. Apothecary Shoppe, Eczane Bileşim Akreditasyon Kurulu (PCAB) tarafından onaylanmıştır ve yanlış dozlama olasılığını azaltmak için kullanılmıştır. Klorambusil, Diamondback Drugs (Phoenix Arizona) tarafından siklofosfamid ile sistit/gastroenterit görülen 8 köpek için bileşik haline getirilmiştir. Toceranib, Pfizer Animal Heath (şimdi Zoetis) tarafından 10 mg, 15 mg ve 50 mg boyutlarında tabletler halinde sağlanmıştır. Yan etkiler kaydedilmiş ve VCOG-CTCAE [43] kullanılarak derecelendirilmiştir. İlaca bağlı toksisiteleri önlemek ve/veya tedavi etmek için eşlik eden ilaçlar, ilgili klinisyenin takdirine bağlı olarak kullanıldı ve şunları içeriyordu: antibiyotikler (siprofloksasin, sefazolin, sefaleksin, amoksisilin klavulanik asit, trimetoprim-sülfametoksazol, enrofloksasin, marbofloksasin), anti-emetikler (ondansetron, maropitant, metoklopramid), gastrointestinal koruyucular (omeprazol, famotidin, sukralfat, pantoprazol, misoprostol, ranitidin), ishal önleyici (loperamid, metronidazol, Pepto-Bismol, probiyotikler) ve ağrı kesici (tramadol, gabapentin, buprenorfin, fentanil), proteinüri/hipertansiyon (benazepril, enalapril), karaciğer transaminazlarında artış meydana geldiğinde (Denamarin, SAMe). |
İstatistiksel AnalizÇalışmanın örneklem büyüklüğü hesaplamalarını yapmak için, amputasyon ve karboplatin kemoterapisi ile tedavi edilen osteosarkomlu 48 ve 155 köpekten oluşan iki önceki çalışmadan tarihsel kontrol grupları alınmıştır. Bu iki popülasyonda bildirilen 1 yıllık sağkalım oranı %35’tir [3,7]. 80 güç ve %95 güven varsayıldığında, tarihsel kontrol popülasyonunda bildirilen 1 yıllık sağkalım oranında %50 artış göstermek için her grupta 47 köpek gerekliydi. Yüksek yıpranma oranı nedeniyle, 32 ilave köpek (grup başına toplam 63 köpek) toplam 126 köpek olarak kaydedilmiştir. Hasta özellikleri tedavi grubuna göre özetlenmiştir (sürekli değişkenler için ortalama ± standart sapma (SD) ve kategorik değişkenler için frekans (%)). Amputasyon tarihi ile tespit edilebilir metastatik hastalık gelişimi arasındaki süre hastalıksız geçen süre (DFI) şeklinde tanımlanmıştır. Ölüm veya son takip sırasında belgelenmiş metastatik hastalığı olmayan köpekler DFI analizinden sansürlenmiştir. Nekropsi incelemesi gerekli değildi, ancak hastalığın ilerlediğine dair radyografik, sitolojik/histopatolojik kanıtları olan köpekler DFI analizine dahil edildi. Genel sağkalım (OS), amputasyondan ölüm veya ötenazi tarihine kadar geçen süre olarak tanımlanmıştır. Köpekler son takip tarihinde hayattaysa veya takibi kaybedilmişse sağkalım analizinden sansürlenmiştir. Kaplan-Meier eğrileri her grup için DFI ve OS’yi tanımlamak için kullanılmış ve Cox regresyonu, başlangıçta gruplara göre farklılık gösterdiği tespit edilen özelliklere göre ayarlanarak DFI veya OS’de herhangi bir fark olup olmadığını test etmek için kullanılmıştır. Hastalığa özgü ölümlerin eksik raporlanmasını önlemek için hastalığa özgü sağkalım yerine OS seçilmiştir. Cox regresyonunun orantılı tehlikeler (PH) varsayımının ihlal edilip edilmediğini belirlemek için Schoenfeld Artıklarının [44,45] grafikleri ve zamanla etkileşim testleri (log dönüştürülmüş) kullanılmıştır. |
| PH ihlal edilmiş ise, zaman ile etkileşim korunmuş ve tehlike oranları; 100 gün (kabaca idame tedavisinin başladığı zaman), iki grubun tehlikelerinin birbirine yaklaştığı zaman, 100 gün ile yakınsama zamanı arasında bir zaman dilimi ve yakınsama zamanı ile maksimum takip süresi arasında son bir zaman dilimi şeklinde olmak üzere dört farklı zamanda tahmin edilmiştir. DFI için tedavi amaçlı analiz ve uyum analizi olmak üzere iki tür analiz gerçekleştirilmiştir. Her iki analizde de köpekler metastatik hastalığa dair kanıt yoksa sansürlenmiştir. Tedaviye yönelik analizde, metastatik hastalığı olmayan köpekler, metastatik hastalık olmadan hayatta kaldıkları bilinen son tarihte sansürlenmiştir. Bağlılık analizi için, hasta sahibinin tercihi veya başka bir tıbbi durum nedeniyle metastatik hastalık gelişmeden önce çalışmadan ayrılan köpekler, çalışmadan çekildikleri tarihte sansürlenmiştir. Uyum analizinde kalan köpekler metastatik hastalık olmadan bilinen son tarihte sansürlenmiştir. Birçok hasta, çalışmaya devam eden hastalara kıyasla daha fazla ölüm riski taşıyan tıbbi sorunlar nedeniyle tedaviden çekildiği için OS için bir uyum analizi yapılmamıştır; bu hastalar analize dahil edilmiş olsaydı Kaplan-Meier hesaplayıcısının ve Cox regresyonunun bağımsız sansürleme varsayımı ihlal edilmiş olacaktı. Sağkalım sonuçları ayrıca tedavi grupları arasında tümörün yerleşim yerinin sonucu etkileyip etkilemediğini değerlendirmek için tümörün yerine göre (proksimal humerusa karşı diğer tüm yerleşim yerleri) karşılaştırılmıştır. En az beş hastada ve tedavi grubu başına en az iki hastada görülen yan etkiler için, vaka oranları Genelleştirilmiş Tahmin Denklemleri (GEE) kullanılarak tahmin edilen sağlam standart hatalarla Poisson regresyonu kullanılarak tedavi grupları arasında karşılaştırılmıştır. Sadece bir tedavi grubunda meydana gelen yan etkiler nadirdi ve sadece istatistiksel olarak karşılaştırılabilecek kadar yaygın olanlar bu analize dahil edildi. Sağkalım analizleri Inter-cooled Stata 11 (StataCorp, College Station, TX) kullanılarak gerçekleştirilmiştir. Poisson regresyonu SAS sürüm 9.2’deki PROC GENMOD kullanılarak gerçekleştirilmiştir (SAS Inc., Cary, NC). |
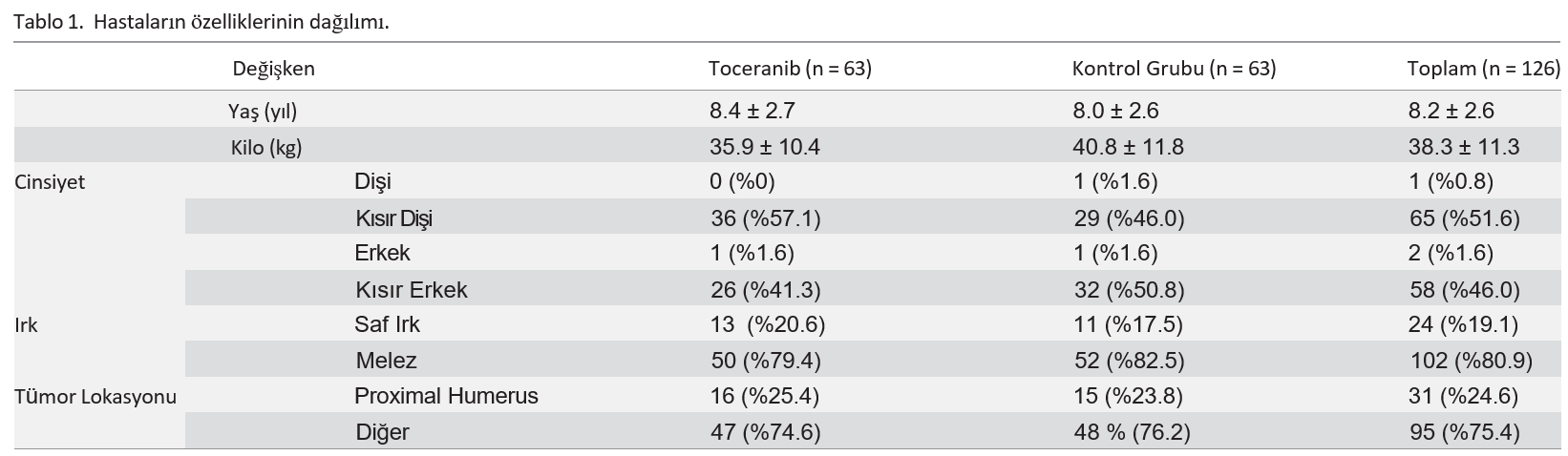
SonuçlarHasta Demografik Özellikleri Bu çalışma, Eylül 2010’dan Ağustos 2012’ye kadar toplam 126 köpeğin (63 toceranib ile tedavi edilen, 63 kontrol) kaydedildiği çok kurumlu bir çalışmadır. Kontrol grubundaki hastalar daha ağırdı ve erkek olma olasılıkları daha yüksekti (Tablo 1). Bu nedenle, Cox regresyon analizlerinde hasta ağırlığı ve cinsiyeti (kısırlaştırılmış erkek/kısırlaştırılmış dişi durumu göz ardı ederek erkek, dişi) için ayarlamalar yapılmıştır. Dozaj ve İlaç DeğişiklikleriTüm köpekler için başlangıç karboplatin dozu 300 mg/m2 idi. Çalışma sırasında uygulanan ortalama karboplatin dozu 300 mg/m2 idi. On dokuz köpekte doz ayarlaması yapılmıştır (aralık: 250-290 mg/m2). Dört köpekte birden fazla doz ayarlaması yapılmıştır. Yan etkiler nedeniyle karboplatin dozunda 33 köpekte gecikme meydana gelmiştir. Uygulanan ortalama toceranib dozu 2,73 mg/kg EOD idi. Yirmi yedi köpekte toceranib doz azaltımı yapılmıştır. Ayrıca, 10 köpekte yan etkiler nedeniyle tedaviye yeniden başlanmadan önce geçici olarak toceranib kesilmiştir. İlaç kesintisi genellikle 1 hafta sürmüştür. Siklofosfamid kaynaklı sistit, 7 köpeğin siklofosfamidden 5 mg/m2 EOD’de klorambusile geçmesine neden olmuştur. Gastrointestinal yan etkiler nedeniyle 1 köpekte siklofosfamid yerine klorambusil kullanılmıştır. |
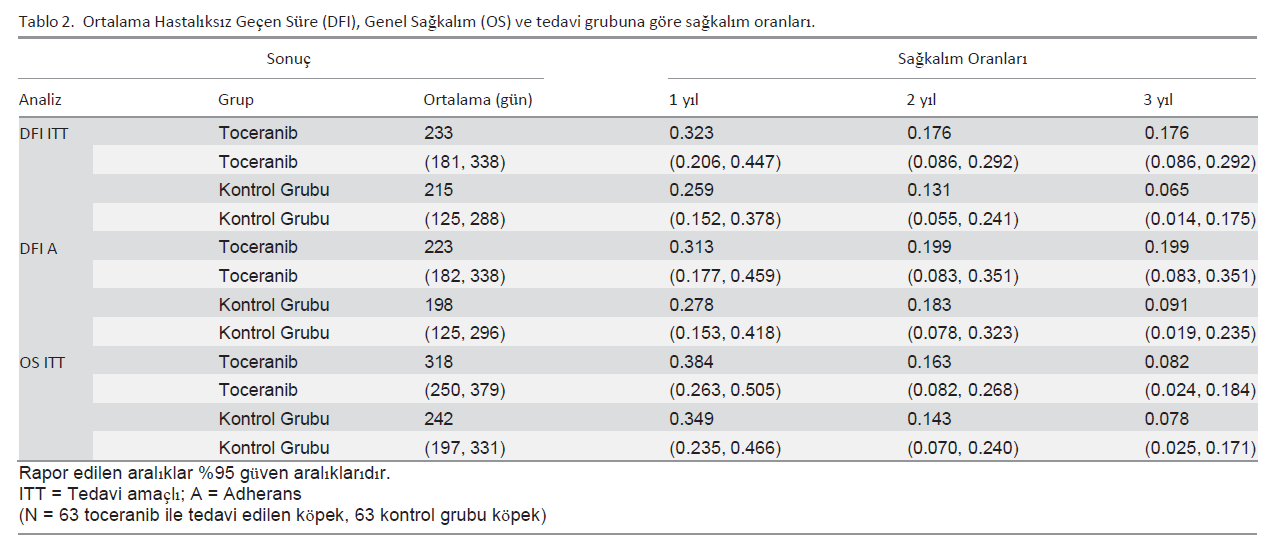
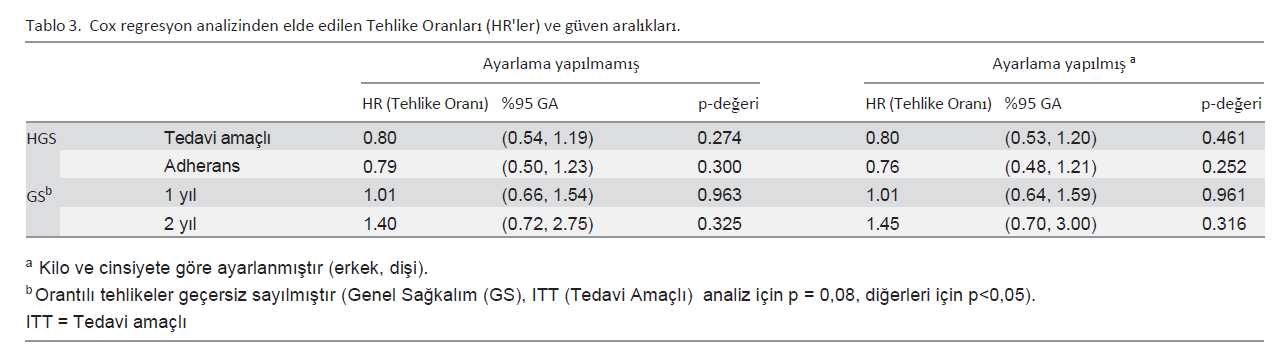
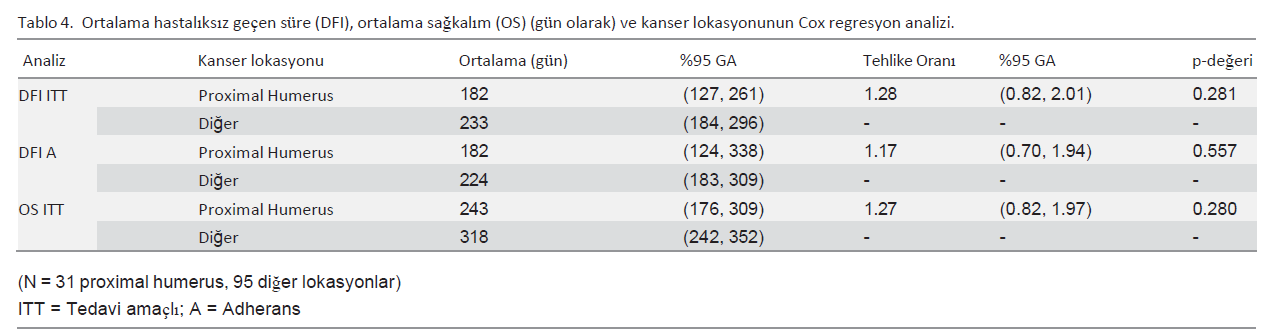
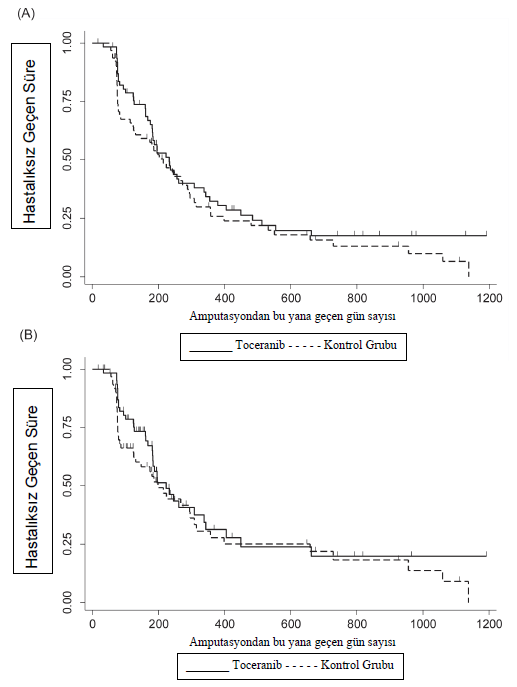
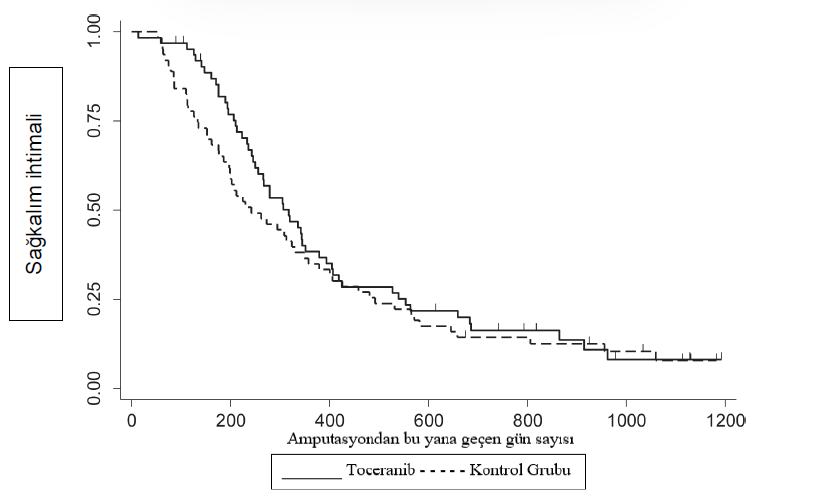
Hastalara İlişkin SonuçlarOtuz iki köpekte (%25) 14. haftada oral tedaviye başlamadan önce ilerleyici hastalık gelişmiştir ve bunların 12’sinde pulmoner parankim dışında metastatik lezyonlar gelişmiştir. Bu durum, apendiküler OSA’lı köpeklerde karboplatin kemoterapisi ile ilgili önceki raporlarla tutarlılık göstermektedir. On üç köpek oral idame tedavisine başlamadan önce sahibinin tedaviye uyumsuzluğu veya diğer tedaviyle ilgisi olmayan tıbbi durumlar nedeniyle tedaviden çekilmiştir. Çalışmaya dahil edilen 126 köpekten 81’i (%64) metronomik tedavi almıştır. Toceranib ile oral tedavi alan 46 köpekten 9’u çalışma protokolünü tamamlamış, 20’si metastatik hastalık geliştiği için, 17’si ise sahibinin tedaviye uymaması veya diğer tedaviyle ilgisi olmayan tıbbi durumlar nedeniyle tedaviden çekilmiştir. Toceranib olmadan oral tedavi alan kontrol grubundaki 35 köpekten 11’i çalışma protokolünü tamamlamış, 15’i metastatik hastalık gelişimi nedeniyle geri çekilmiş ve 9’u da sahibinin uyumsuzluğu veya diğer ilgisiz tıbbi durumlar nedeniyle geri çekilmiştir. Tedavi amaçlı analizde rapor edilen ortalama DFI, toceranib ile tedavi edilen köpekler için 233 gün ve kontrol köpekleri için 215 gündü (p = 0.274, Şekil 1A, Tablo 2 ve 3). Bağlılık analizinde bildirilen ortalama DFI, toceranib ile tedavi edilen köpekler için 223 gün ve kontrol köpekleri için 198 gündü (p = 0.3, Şekil 1B, Tablo 2 ve 3). Ortalama OS, toceranib ile tedavi edilen ve kontrol köpekleri için sırasıyla 318 gün ve 242 gündü (p = 0,08) (Şekil 2, Tablo 2 ve 3). DFI tedavi grupları arasında benzerdi, ancak kısa vadeli mortalite riskinde zamana bağlı bir fark vardı (Şekil 2 ve Tablo 3). Başlangıçta, mortalite tehlikesi kontrol hastaları arasında daha fazlaydı, ancak yaklaşık 400 günde riskler birbirine yaklaştı ve bir yıl (p = 0.961) ve iki yılda (p = 0.316) önemli bir fark göstermedi. Toceranib ile tedavi edilen grubun 1 ve 2 yıllık sağkalım oranları kontrol grubununkilerden belirgin şekilde farklı değildi (sırasıyla p = 0,963 ve 0,325) (Tablo 2). Kanseri proksimal humerus yerleşimli hastalarda ortalama DFI (182 gün, p = 0.281) ve OS (243 gün, p = 0.28) daha kısaydı, ancak bu fark istatistiksel olarak anlamlı değildi (Tablo 4). Ayrıca, proksimal humerus yerleşimi tedavi grupları arasındaki farkları etkilememiştir (her bir sağkalım sonucu için p > 0.28). |
Yan EtkilerYan etkiler daha önce karboplatin ve toceranib için rapor edilenlere benzerdi. Grade 1 (n = 77) ve 2 (n = 18) nötropeni ve grade 1 trombositopeni (n = 26) karboplatin kemoterapisi sırasında gözlenen en yaygın hematolojik yan etkilerdi. Grade 1 diyare (n = 31), letarji (n = 22) ve kusma (n = 18) da karboplatin uygulaması sırasında yaygın olarak bildirilmiştir. Oral tedavi sırasında gözlenen başlıca toksisiteler gastrointestinal ve hematolojiktir. S1 Tablosu Poisson regresyonu kullanılarak modellenebilecek kadar yaygın olan tüm olaylar için yan etki oranlarını göstermektedir. Toceranib’e randomize edilen hastalar, kontrole randomize edilen hastalara göre daha fazla diyare, nötropeni ve kilo kaybı atakları yaşamıştır, ancak bu toksisiteler düşük derecelidir ve tipik olarak destekleyici bakım ve doz modifikasyonları ile düzelmiştir. Yan etkiler nedeniyle ilacın geçici olarak kesilmesi genellikle 1 hafta sürmüştür. İlacın 2 haftadan daha uzun süre kesilmesini gerektiren köpekler çalışmadan çıkarılmıştır. |
| Kontrol köpeklerine (n = 1) kıyasla daha fazla toceranib ile tedavi edilen köpek (n = 8) tedaviyle ilişkili yan etkiler nedeniyle çalışmadan çıkarılmıştır. Yedi köpekte siklofosfamide bağlı sistit gelişmiştir (n = 2 kontrol; n = 5 toceranib ile tedavi edilen), bu da siklofosfamidin klorambusil ile değiştirilmesine neden olmuştur. Toceranib ile tedavi edilen bir köpekte görülen gastrointestinal yan etkiler siklofosfamidden klorambusile geçişe neden olmuştur. Gastrointestinal. On üç köpek toceranib kullanırken grade 1 kusma yaşamış, bunlardan ikisi birden fazla atak geçirmiştir. Toceranib ile tedavi edilen bir köpekte pankreatit ile birlikte grade 4 kusma ve ishal gelişmiştir. Kusma ve ishal destek tedavisiyle ve ilacın geçici olarak kesilmesiyle düzelmiştir. On kontrol köpeğinde grade 1 kusma görülmüş, 3 köpekte birden fazla atak yaşanmıştır. On yedi toceranib ile tedavi edilen köpekte grade 1 diyare gelişmiş ve 12 köpekte 1’den fazla atak görülmüştür. On altı köpekte toceranib kullanırken grade 2 diyare gelişmiştir ve 6 köpekte 1’den fazla atak görülmüştür. Toceranib ile tedavi edilen iki köpekte grade 3 diyare gelişmiş, bir köpekte 3 diyare epizodu görülmüştür. Grade 3 diyaresi olan her iki köpek de gastrointestinal yan etkiler nedeniyle çalışmadan çıkarılmıştır. |
| Toceranib almayan yedi köpekte grade 1 diyare gelişmiş, bir köpekte ise 2 diyare epizodu görülmüştür. Anoreksi genellikle hafifti ve çalışmanın her iki kolunda da grade 1 ve 2 yan etkilerle sınırlıydı. Hematolojik. Grade 1 nötropeni, toceranib ile tedavi edilen köpeklerde en sık görülen hematolojik yan etkiydi ve 14 köpekte geçici nötropeni görüldü. Geçici düşük gradeli hematolojik toksisite nedeniyle doz ayarlaması veya ilacın geçici olarak kesilmesi gerekmemiştir. Toceranib alan altı köpekte ve 8 kontrol köpeğinde grade 1 trombositopeni görülmüştür. Bir köpekte yaygın metastatik hastalık ortamında meydana gelen grade 5 trombositopeni görülmüştür. |
| Biyokimyasal. Karaciğer transaminazlarındaki yükselmelerin çoğu grade 1 ve 2 idi. Toceranib alan iki köpekte grade 3 ALT yükselmesi görülmüş ve bu durum toceranibin geçici olarak kesilmesi ve destekleyici tedaviyle düzelmiştir. Bir kontrol grubu köpeğinde sırasıyla grade 3 ve 4 ALT ve ALP yüksekliği görülmüş ve bu durum oral tedavinin geçici olarak kesilmesiyle düzelmiştir. Nöromasküler. Toceranib ile tedavi edilen 4 köpekte ve 3 kontrol grubunda grade 1 ve 2 halsizlik görülmüştür. Toceranib alan iki köpekte grade 3 halsizlik gelişmiştir ve 1 köpekte üç ayrı atak meydana gelmiştir. Her iki köpekte de her bir epizod toceranibin geçici olarak kesilmesiyle düzelmiştir. Toceranib ile tedavi edilen 8 köpekte ve 5 kontrol köpeğinde ilerleyici hastalık olmaksızın düşük dereceli kas-iskelet ağrısı/zayıflığı kaydedilmiştir. Diğer. Bu çalışmaya dahil edilen köpeklerde gözlenen diğer yan etkiler şunlardır: yüksek kreatinin kinaz; otitis media; ateş; idrar yolu enfeksiyonu; epistaksis; strangüri; hiperglisemi; hipoglisemi; indolent oküler ülser; nöbet; titreme/panting; deri eritemi; piyoderma; hiperkalemi; hipokalemi; hipoalbuminemi; hiperkalsemi; ataksi; motor nöropati; duyusal nöropati. Bu yan etkilerin toceranib/oral tedavi ile ilişkili olmadığı ve muhtemelen hastalığın ilerlemesini veya diğer komorbid durumları temsil ettiği düşünülmektedir. TartışmaOSA’lı köpekler için amputasyon ve adjuvan kemoterapinin faydaları veteriner hekimlikte kabul görmüştür, ancak çoğu köpek amputasyon ve adjuvan kemoterapiden sonraki 1 yıl içinde metastatik hastalığa yenik düşmektedir ve çoğu çalışmada 2 yıllık sağkalım oranları sadece %10-15 olarak bildirilmiştir [8,46]. Sonucu iyileştirmeye yönelik çok sayıda girişime rağmen, hasta köpekler için sağkalımı uzatma konusunda çok az ilerleme kaydedilmiştir. Bu klinik çalışmanın amacı, amputasyon ve karboplatin kemoterapisini takiben apendiküler OSA’lı köpeklerde piroksikam ve siklofosfamidin tek başına veya toceranib ile birlikte kullanıldığı metronomik kemoterapinin hem hastalıksız periodu hem de genel sağkalımı etkileyip etkilemeyeceğini belirlemektir. Bu çalışmanın sonuçları, toceranib ile piroksikam ve siklofosfamid metronomik tedavisinin, tek başına piroksikam ve siklofosfamide kıyasla apendiküler OSA’lı köpeklerde ortalama hastalıksız geçen süreyi, ortalama sağkalım süresini veya 1 yıllık sağkalım oranını iyileştirmediğini göstermiştir. Bu çalışmada rapor edilen ortalama DFI ve sağkalım süreleri, amputasyondan sonra karboplatin kemoterapisi alan köpekler için rapor edilenlerle benzerlik göstermektedir [3,7]. Ayrıca, toceranib ile tedavi edilen köpekler ve kontrol grubu köpekler için sırasıyla %38,4 ve %34,9 olan 1 yıllık sağkalım oranları, tek başına karboplatin için bildirilen %35,4’lük 1 yıllık sağkalım oranıyla karşılaştırılabilir. Benzer sonuçlar tek başına veya karboplatin ile kombinasyon halinde doksorubisin, tek başına sisplatin ve gemsitabin ile eş zamanlı olarak verilen karboplatin ile de elde edilmiştir [5,8,47-49]. Yakın zamanda yapılan retrospektif bir çalışmada, amputasyon sonrası köpek apendiküler OSA için kullanılan çoklu kemoterapi protokolleri karşılaştırılmıştır. Doz yoğunluğu ve seçilen kemoterapi protokolündeki farklılıklar, sırasıyla 291 gün ve 284 gün olarak bildirilen ortalama DFI ve OS’yi önemli derecede etkilememiştir [8]. Bu veriler, mevcut sitotoksik kemoterapötikler kullanılarak mikroskobik metastatik hastalığı tedavi etmek için terapötik yaklaşımların değiştirilmesinin OSA’lı köpekler için kayda değer bir fayda sağlayamayacağı görüşünü desteklemektedir. Bu çalışmada rapor edilen ortalama DFI ve sağkalım süreleri, amputasyondan sonra karboplatin kemoterapisi alan köpekler için rapor edilenlerle benzerlik göstermektedir [3,7]. Ayrıca, toceranib ile tedavi edilen köpekler ve kontrol grubu köpekler için sırasıyla %38,4 ve %34,9 olan 1 yıllık sağkalım oranları, tek başına karboplatin için bildirilen %35,4’lük 1 yıllık sağkalım oranıyla karşılaştırılabilir. Benzer sonuçlar tek başına veya karboplatin ile kombinasyon halinde doksorubisin, tek başına sisplatin ve gemsitabin ile eş zamanlı olarak verilen karboplatin ile de elde edilmiştir [5,8,47-49]. Yakın zamanda yapılan retrospektif bir çalışmada, amputasyon sonrası köpek apendiküler OSA için kullanılan çoklu kemoterapi protokolleri karşılaştırılmıştır. Doz yoğunluğu ve seçilen kemoterapi protokolündeki farklılıklar, sırasıyla 291 gün ve 284 gün olarak bildirilen ortalama DFI ve OS’yi istatistiksel olarak önemli ölçüde etkilememiştir [8]. Bu veriler, mevcut sitotoksik kemoterapötikler kullanılarak mikroskobik metastatik hastalığı tedavi etmek amacıyla terapötik yaklaşımların değiştirilmesinin OSA’lı köpekler için önemli bir fayda sağlamayacağı fikrini desteklemektedir. Metronomik siklofosfamid kullanımının, siklofosfamid 15 mg/m2/gün uygulandığında tümör taşıyan köpeklerde dolaşımdaki düzenleyici T hücrelerinin (Treg) sayısını ve tümör mikrodamar yoğunluğunu azalttığı da görülmüştür [11]. Ne yazık ki, metronomik kemoterapi protokollerinde kullanılan dozlar ve rejimler büyük ölçüde anekdot niteliğindedir ve OSA’lı köpeklerde klinik faydayı öngören biyobelirteçler kapsamlı bir şekilde değerlendirilmemiştir. Bu çalışmada siklofosfamid ve piroksikam sırasıyla 10 mg/m2 ve 0,3 mg/kg EOD dozlarında uygulanmıştır. Bu tedavi rejimi, daha yüksek dozlarda siklofosfamidin immünomodülatör ve antianjiyojenik etkilerinin ortaya konmasından önce, çalışmanın başlangıcında mevcut literatüre dayanılarak oluşturulmuştur. Daha yüksek dozlarda kullanılan siklofosfamidin rapor edilen immünomodülatör ve anti-anjiyojenik etkileri göz önüne alındığında, bu çalışmada siklofosfamidin daha düşük dozda kullanılması ve EOD doz kullanımı, tümör mikroçevresini, devrede olan Treg sayısını veya her ikisini de önemli ölçüde etkilemede yetersiz kalmış olabilir. Metastatik köpek apendiküler osteosarkomunda toceranibin biyolojik etkinliği rapor edilmiş olsa da [37], mevcut çalışmada DFI ve OS’de iyileşme olmaması, köpek OSA’sında hastalığın farklı aşamalarında farklı moleküler etkenler olabileceğini düşündürmektedir. Toceranib tedavisini takiben makroskopik metastatik pulmoner lezyonları olan köpeklerde tümör büyümesi üzerinde etkili olurken, mikroskopik lezyonların kısa bir süre içinde tedaviye dirençli hale gelmesi ve böylece herhangi bir potansiyel terapötik değeri ortadan kaldırması muhtemeldir. Çeşitli fare modellerinden elde edilen veriler, VEGF inhibitörlerinin tümör mikro ortamını metastatik tümör büyümesini gerçekten hızlandırabilecek şekilde modüle ettiğini göstermiştir [28,29,52]. Bu nedenle, VEGFR inhibitörlerinin mikroskobik hastalık ortamında kullanılmasının aslında daha agresif bir fenotipi teşvik edebileceği endişesi söz konusudur. Bu çalışmada, mikroskobik metastatik OSA’lı köpeklerde toceranib kullanımının, tedavi sonrasında daha agresif bir hastalık fenotipinin indüklendiğini gösterecek şekilde sağkalım sürelerinde kısalma veya anormal metastaz paternleri ile sonuçlanmadığı ortaya konmuştur. Yakın zamanda, kanser taşıyan köpeklere 2,75 mg/kg EOD toceranib uygulanması, muhtemelen dolaylı immünomodülatör mekanizmalar yoluyla dolaşımdaki Treg’lerde önemli bir azalma ile ilişkilendirilmiştir [39]. Tescilli dozun altındaki toceranib dozları (2,4-2,9 mg/kg EOD arasında değişen) hala hedef inhibisyonu ile sonuçlanmakta ve bu çalışmada 2,75 mg/kg kullanımını desteklemektedir [37]. Bu nedenle, burada bildirilen DFI ve OS’deki iyileşme yetersizliği, mevcut etiket dozundan daha düşük toceranib dozunun kullanılmasına bağlı değildir. VEGFR inhibisyonu bu çalışmada spesifik olarak değerlendirilmemiş olsa da, toceranib tedavisini takiben plazma VEGF konsantrasyonlarının yükselmesi daha önce 2,4-2,9 mg/kg EOD alan köpeklerde etkili VEGFR2 inhibisyonu ile tutarlılık göstermiştir [37]. Siklofosfamid yerine klorambusil uygulanmasını gerektiren yan etkiler 8 köpekte meydana gelmiş ve bunlardan biri hariç hepsi steril sistite bağlı görülmüştür. Siklofosfamid kaynaklı sistitin genel insidansı veteriner literatüründe düşüktür ve artan risk daha yüksek kümülatif siklofosfamid dozu ve daha yüksek doz yoğunluğu ile ilişkilendirilmiştir [53]. Her grupta sistit görülen çok az sayıda köpek olduğundan (n = 2 kontrol, n = 5 toceranib), toceranib ile tedavi edilen daha fazla sayıda köpekte sistit görülmesi muhtemelen tesadüftür. Metronomik klorambusil kullanımı, çeşitli spontan köpek tümörlerinde bazı antitümör aktivitelerle ilişkilendirilmiştir ve klorambusil alan köpeklerde dolaşımdaki Treg sayılarında başlangıca kıyasla azalmalar olduğu tespit edilmiştir [51]. Metronomik siklofosfamid ve klorambusilin immünomodülatör etkileri bildirilmiş olsa da, bu çalışmada klorambusil uygulamasının etkisi bilinmemektedir. Bununla birlikte, siklofosfamid yerine bu ilacı almaya devam eden az sayıda köpek olduğu göz önüne alındığında, her iki grupta da sonucu önemli ölçüde etkilemesi pek mümkün değildir. Proksimal humerusta meydana gelen OSA’nın prognostik önemi hakkında çok sayıda araştırma rapor edilmiştir [3,7,54-57]. Mevcut çalışmada proksimal humerus yerleşimli tümörlü köpeklerde sağkalım sürelerinde azalma kaydedilirken, OS’deki fark diğer tümör yerleşimleriyle karşılaştırıldığında anlamlı değildi. Bu durum, çalışmaya proksimal humerus hastalığı ile katılım gösteren köpek sayısının az olmasından kaynaklanmış olabilir (n = 31). Alternatif olarak, metronomik tedavinin bu popülasyonda sağkalımı iyileştirmek için sonuç üzerinde etkili olması mümkündür. Bu hasta alt grubunda metronomik kemoterapinin faydalarını belirlemek için gelecekte kontrollü çalışmalar yapılması gerekmektedir. Toceranib ile tedavi edilen köpekler, kontrol köpeklerine kıyasla daha yüksek yan etki profiline sahip olmakla birlikte, bildirilen yan etkiler daha önce yayınlanmış çalışmalara dayanarak beklenenlerle tutarlılık göstermekteydi. Mevcut çalışmada, toceranib kullanırken yan etki yaşayan köpeklerin ilaca ara verme, eşlik eden ilaçlar ve/veya doz azaltımı ile etkili bir şekilde tedavi edildiğini belirtmek önemlidir. Yan etkilerin sıklığı, 2,4-2,9 mg/kg dozlarında toceranib alan çeşitli solid tümörlü köpekler üzerinde yapılan yakın tarihli bir klinik çalışmada bildirilenden daha düşüktür [37]. Bu çalışmada, yan etki profili toceranibin tescilli dozuyla (3,25 mg/kg) ilişkili olandan çok daha yüksek olmuş, ancak hem yeterli ilaç maruziyeti hem de biyolojik aktivite korunmuştur [37]. Çeşitli çalışmalardan elde edilen bulguların karşılaştırılmasındaki doğal zorluklara rağmen, bu çalışmada kullanılan toceranib dozu (2.75 mg/kg) tescilli doza kıyasla daha iyi tolere edilmiş ve tedavi protokolüne daha iyi uyulmasını sağlamıştır [36,37]. Mevcut çalışmada nekropsi gerekmediği ve metastatik hastalığın tespiti büyük ölçüde klinik bulgulara ve toraks radyografilerine bağlı olduğu için, birçok köpekte diğer bölgelerdeki gros metastatik hastalığın gözden kaçmış olması olası değildi. Abdominal ultrason ile tespit edilebilen gross OSA metastazı insidansı daha önce rapor edilmiş olup, pulmoner metastatik hastalık kanıtı olmayan köpeklerin %0-1,7’sinde abdominal metastaz tespit edilmiştir [58,59]. Ayrıca, ilk muayene sırasında (amputasyondan önce) apendiküler OSA’lı köpeklerde nükleer sintigrafi ile şüphe uyandırmayan osseöz metastaz tespit etme oranı %7,8 olarak bildirilmiştir [60]. Bu nedenle, nekropsi yapılmaması gerçek metastaz insidansının eksik bildirilmesine katkıda bulunmuş olsa da, torasik radyografi, amputasyon ve kemoterapi sonrası çoğu köpekte metastatik hastalığı tespit etmek için güvenilir bir teşhis prosedürü olarak kabul edilir ve ekstratorasik metastazlar genellikle klinik belirtiler (örneğin, kemik metastazı için topallık) sayesinde tespit edilir. Bileşik terapötiklerin kullanımının sonuçlarımızı etkilemiş olması mümkündür. The Apothecary Shoppe (şimdi Avella Specialty Pharmacy), Eczacılık Bileşim Akreditasyon Kurulu tarafından onaylandığı için bileşik siklofosfamid ve piroksikam tedarikçisi olarak seçilmiştir. Bununla birlikte, karışımların yanlışlıkla aşırı dozda veya eksik dozda verilmesinin bazı hastalarda sırasıyla toksisite artışı veya terapötik altı ilaç konsantrasyonları ile sonuçlanabileceği kabul edilmektedir. Mevcut çalışmanın potansiyel olarak zayıf noktası, metronomik tedavi rejiminin karboplatin kemoterapisinin tamamlanmasından sonra başlamış olmasıdır. Bu durum, kalan mikroskobik metastatik tümör hücrelerine çoklu tedavilere karşı direnç geliştirmeleri için zaman kazandırmış ve böylece sonraki tedavinin olası etkilerini ortadan kaldırmış olabilir. Apendiküler osteosarkomlu köpeklerde karboplatin ile eş zamanlı olarak uygulanan metronomik siklofosfamid ve piroksikam kullanımının başka bir çalışmada iyi tolere edildiği rapor edilirken [50], eş zamanlı uygulama ile sağkalım süresinde herhangi bir iyileşme kaydedilmemiştir. Bununla birlikte, toceranibin metronomik kemoterapi ve karboplatin ile birlikte eş zamanlı kullanımının DFI ve OS’yi önemli ölçüde etkileyip etkilemediğini belirlemek gerekebilir. |
SonuçYaygın olarak kullanılan metronomik kemoterapi protokolüne toceranib eklenmesi, amputasyon ve karboplatin kemoterapisinden sonra apendiküler OSA’lı köpeklerde DFI, OS ve 1 yıllık sağkalım oranlarını tek başına metronomik tedaviye kıyasla iyileştirememiştir. Ayrıca, bu çalışmadaki DFI, OS ve 1 yıllık sağkalım oranları, daha önce OSA’lı köpeklere tek başına amputasyon ve karboplatin kemoterapi tedavisi uygulandığında bulunanlarla benzerlik göstermiştir. Bu çalışma, tümör mikroçevresine karşı aktiviteyi optimize etmeyi amaçlayan yeni yaklaşımların başarılı bir şekilde kullanılabilmesi için hastalığın çeşitli aşamalarında görülen tümör ilerlemesini yönlendiren moleküler mekanizmaların kapsamlı bir şekilde incelenmesi gerektiğinin altını çizmektedir. Ek BilgiS1 Tablosu. Yan Etki Oranları (sayı/30 gün) ve Oran Rasyoları (RR’ler). Tablo yalnızca en az beş hastanın ve her tedavi grubunda en az iki hastanın yaşadığı olayları içermektedir. (DOCX) TeşekkürlerOhio Devlet Üniversitesi Veteriner Hekimlik Fakültesi Klinik Araştırmalar Ofisi (CTO) (Nicole Stingle, Tamra Mathie, Ashley Smith) vaka rapor formlarının oluşturulması, numunelerin toplanması, verilerin harmanlanması, kalite güvencesi, diğer klinik sahaların koordinasyonu ve tüm çalışma sahalarından gelen tüm veriler üzerinde nihai kalite kontrolü dahil olmak üzere bu çalışmanın tüm yönlerini koordine etmiştir. Bu proje Translasyonel Bilimler Gelişim Ulusal Merkezi’nden UL1TR001070 ve Ulusal Kanser Enstitüsü’nden Ohio Eyalet Üniversitesi’ne P30CA016058 numaralı fonlar ile desteklenmiştir. Bu klinik çalışma için finansman Zoetis tarafından sağlanmıştır. İçerik yalnızca yazarların sorumluluğundadır ve Ulusal Translasyonel Bilimler Gelişim Merkezi, Ulusal Kanser Enstitüsü veya Ulusal Sağlık Enstitüleri veya Zoetis’in resmi görüşlerini temsil etmemektedir. Katkıda Bulunan YazarlarDeneyleri tasarlayan ve düzenleyen: CAL. Deneyleri gerçekleştiren: CAL HLG RP MLP CAC MPR DMV LEW KLC HW-R AB CJH DBB JL NCN MC-J VLG MKK DMR DHT BP GP. Verileri analiz eden: CAL HLG MLP. Reaktif / malzeme / analiz araçlarına katkıda bulunanlar: MLP. Makaleyi yazan: CAL HLG MLP. Veri girişini organize eden ve kalite kontrolünü yapan: TM NS. |
Kaynakça
|