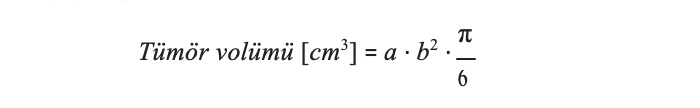AÇIK ERİŞİM
Editör: Carlos Eduardo Fonseca-Alves, Paulista Üniversitesi, Brezilyal
İnceleyen:
Elisabetta Razzuoli, Piedmont, Liguria ve Valle Deneysel Zooprofilaktik Enstitüsü
d’Aosta (IZSTO), İtalya Zeinab Shankayi,
Tarbiat Modares Üniversitesi, İran
*İlgili kişi:
Felipe Maglietti felipemaglietti@gmail.com
Uzmanlık alanı: Bu makale Frontiers in Veterinary Science dergisinin bir bölümü olan Comparative and Clinical Medicine’e gönderilmiştir.
Sunum Tarihi: 03 Şubat 2022
Kabul Tarihi: 17 Haziran 2022
Yayınlanma tarihi: 27 Temmuz 2022
Bu makaleye atıfta bulunmak için: Tellado M, Mir LM and Maglietti F (2022) Veterinary Guidelines for Electrochemotherapy of Superficial Tumors. Front. Vet. Sci. 9:868989. doi:10.3389/fvets.2022.868989
Elektrokemoterapi (ECT), tümör hücrelerine kemoterapötik ilaç iletiminin (bleomisin, sisplatin veya kalsiyum) artırılması için elektrik pulslarının uygulanmasıdır. Veteriner onkolojisinde son derece önemli bir tedavi seçeneği haline gelmiştir. Sadece palyatif bir tedavi olarak değil, aynı zamanda küratif yaklaşımda da faydalı olan etkili ve güvenli bir tedavi yöntemidir. Tedavinin uygun şekilde yapılması, mümkün olan en iyi sonuçların en az sayıda seansta alınmasını sağlayacak ve komplikasyonları azaltacaktır. Genellikle, mükemmel sonuçlar elde etmek için sadece bir seans yeterlidir, ancak tedavinin tekrarlanması gerekebilir. Tam olarak tedavi edilmemiş veya çok genişlemiş lezyonların yanı sıra yeni lezyonların ortaya çıkması durumunda birkaç seans uygulanması gerekebilir. EKT, elektrotların erişebildiği yüzeysel veya oral tümörlerde etkilidir. Bleomisinin uygulanması için tercih edilen ilaç ve yol intravenöz olup, diğer uygulama yolları ve ilaçlar seçilen vakalara göre belirlenmektedir. Bu makalede sunulan rehber niteliğindeki bilgiler, EKT’nin dayandığı esaslara ilişkin bilgilerini geliştirmek isteyen ve EKT’yi yeterli ve etkili bir şekilde uygulamak isteyen veteriner hekimlere yöneliktir. Bu makalede ayrıca, sık karşılaşılan sorunlar ve bunların nasıl çözüleceği ele alınmakta ve yeni başlayan veteriner hekimlerin ortak soru ve hatalarına dayanarak tedaviyi daha iyi sonuçlandırmaya yarayacak pratik ipuçlarına yer verilmektedir.
Anahtar Kelimeler: elektroporasyon, kanser, onkoloji, evcil hayvanlar, köpekler, kediler, atlar, prosedürler
GİRİŞ
Elektrokemoterapi: Kavram, Uygulama Alanı ve Avantajları
Elektrokemoterapi (EKT), veteriner hekimlikte 1997’den beri Avrupa’da (1) ve 2008’den beri Latin Amerika’da uygulanan köklü bir tedavi yöntemidir. İnsan tıbbında kullanımı 1991 yılında yayınlanan klinik bir çalışma ile başlamış (2, 3) ve 2006 yılında insan hastalarda EKT uygulaması için standart operasyon prosedürleri yayınlandığında ve uygun ekipman kullanıma sunulduğunda standart bir tedavi haline gelmiştir (4).
Veteriner hekimlikte, EKT standart bir bakım yöntemi olarak artık dünyanın birçok ülkesinde uygulanmaktadır. EKT kullanımı, veteriner elektroporatörleri üretildikten sonra ve özellikle Slovenya, Brezilya ve Arjantin’de eğitim kursları verilmeye başlandıktan sonra hızlı bir artış göstermiştir. Bu etki, sadece Latin Amerika’da, Brezilya ve Arjantin’deki yıllık toplantıların dünyanın dört bir yanından gelen kullanıcıların bilgi ve deneyimlerini paylaşmasıyla ortaya çıkmıştır. Şimdiye kadar nispeten az sayıda yayın çıkmış olmasına rağmen, sadece Latin Amerika’da 120’den fazla merkezde 20.000’den fazla hasta tedavi edilmiştir (2019 yılında Brezilya’da düzenlenen son kullanıcı toplantısından elde edilen bilgiler).
EKT, başlangıçta histolojisi ne olursa olsun deri ve deri altı tümörlerinin palyatif tedavisi için kullanılmıştır. Ancak günümüzde, tek başına veya diğer tedavilerle birlikte ilk basamak tedavi olarak kullanılabilmektedir. Veterinerlik ve insan tıbbı için özel olarak tasarlanmış elektrotların yardımıyla farklı anatomik bölgelerdeki tümörleri tedavi etmek için kullanılabilmektedir (5-11).
EKT, hücrelere elektrik uygulanması yoluyla hücrelerin geçici ve geri dönüşümlü olarak permeabilize edilmesidir. Bu, belirli moleküllerin hücresel girişini artırarak sitotoksik ve antikanser etkinliklerini 1.000 kata kadar yükseltir (12). Bleomisin, sisplatin veya kalsiyum etkili olduğu kanıtlanmış ilaçlardır ve diğerine kıyasla bleomisin bariz bir şekilde daha avantajlıdır (13, 14). Bu avantajın temelinde bleomisinin replike olan hücreleri seçici olarak öldürmesi, replike olmayan sağlıklı dokuları koruması, immün sistem yanıtını indüklemesi ve intravenöz olarak uygulanarak tedavi edilen bölgede yeterli doz kullanılabilirliği sağlaması yatmaktadır (13, 15).
İlaç hücre içine fiziksel bir şekilde nüfuz ettiğinden, penetrasyon hücre tipine bağlı değildir. Histolojisi ne olursa olsun tümörler çok iyi sonuçlarla tedavi edilebilmektedir ve objektif yanıt oranı %70-100 civarındadır. Bu yüksek yanıt oranı köpeklerde, kedilerde, atlarda ve elbette insan hastalarda da görülebilmektedir (11, 16, 17). Özellikle malign melanomda erken evrelerde objektif yanıt oranı %90 (9), skuamöz hücreli karsinomlarda %80 (18), sarkoidlerde %97 (11) ve 2 cm3’ten küçük mast hücreli tümörlerde %100 (19) civarındadır.
Elektroporasyon pulslarının uygulanması aynı zamanda tedavi edilen bölgedeki kan akışının anlık olarak kesilmesini sağlayarak vasküler kilitlenmeye neden olur. Böylece ilacın tümörün içine hapsedilmesi, tümörün aç bırakılması ve tedavi edilen bölgede anında hemostaz sağlanması gibi tedaviye ek faydalar sağlanır (20, 21).
İmmün yanıt tedavinin etkinliğinde çok önemli bir rol oynamaktadır, zira immün sistemi baskılanmış farelerde tedaviye yanıtın oldukça düşük olduğu görülmüştür (13, 22, 23). Ayrıca, veteriner hekimlikte, bağışıklık sisteminin rolü tedavinin etkisini artırdığı için son derece önemlidir ve hatta bazı özel durumlarda abscopal etkilere yol açabilir (24).
Sonuç olarak, tümörün boyutuna ve konumuna bağlı olarak çoğu vakada bir veya iki seansta oldukça iyi sonuçlar elde edilebilmektedir. Terapinin, örneğin debulking cerrahisi, kemo veya radyoterapi ile birlikte, etkilerini artıran diğer tedavi yöntemleriyle birleştirilebileceğini hatırlamak da önemlidir (25). Son olarak, EKT başka hiçbir tedavi seçeneği mevcut olmadığında da uygulanabilir ve yine de iyi sonuçlar verir, bu da EKT’yi veteriner onkolog için oldukça cazip bir yöntem haline getirmektedir (26).
Hassas tıpta tedaviler, etkinliklerini artırmak ve yan etkilerini azaltmak için hastaların özellikleri, genetiği ve çevresel faktörler dikkate alınarak seçilir ve kişiselleştirilir (27). Hassas tıp, bir yandan hastanın ve hastalığının biyolojik ve kimyasal özelliklerine, diğer yandan da tedavinin biyolojik ve kimyasal etkilerine dayanmaktadır. EKT, fiziksel bir yaklaşım olduğu için hassas tıbba özgün bir müdahaledir. Bugüne kadarki tüm klasik fiziksel yaklaşımların (radyoterapi, brakiterapi, kriyoterapi, hipertermi, yüksek frekanslı ultrason ve hatta ≪ mekanik ≫ yaklaşım olarak cerrahi dahil) ablatif yöntemler olduğunu, yani kanserli ve normal hücreler arasında seçici bir ayrım yapmadıklarını belirtmek önemlidir. Buna karşın EKT ablatif bir yöntem değildir. Sonraki bölümlerde tartışılacağı gibi, elektropermeabilizasyon ve bleomisin gibi geçirgen olmayan bir sitotoksik ilacın mükemmel kombinasyonu ile tümör hücreleri son derece hassas ve seçici bir şekilde yok edilir. Böylece normal hücrelerin ve doku parçalarının korunmasını sağlayarak klasik kemoterapinin ve ablatif prosedürlerin yan etkileri önemli ölçüde azaltılır. Bu nedenle EKT, hassas tıp için etkili, uygulaması kolay ve güvenli yeni bir yöntemdir. EKT hassasiyeti özellikle tümör kitlesinin sınırlarının ve çevresinin etkili ve güvenli bir şekilde tedavi edilmesini sağlar çünkü söz konusu hacim içinde bulunan az sayıdaki tümör hücresi ortadan kaldırılırken aynı hacimdeki normal hücreler canlı kalacaktır. Çoğalan hücrelerin, yani tümör hücrelerinin öldürülmesindeki bu hassasiyet, EKT’nin neden sağlıklı dokuları koruduğunu ve organ fonksiyonlarını koruduğunu açıklamaktadır ki bu, bazı hastalarda tedavi seçiminde, özellikle de yaşam kalitesinin korunmasında en önemli unsurdur. Bu seçicilik, tedavinin hafif ve kendi kendini sınırlayan şekilde seyreden yan etkilerini azaltmakta ve hatta deri ve deri altı tümörlerinin tedavisinde çok iyi sonuçlar vermektedir (28). Ayrıca, birden fazla ilaca ve hatta radyoterapiye direnç gösteren genetik özellikleri olan tümörler söz konusuysa bile, EKT bu engelleri aşma kabiliyeti nedeniyle önemli bir rol oynamaktadır. EKT, ilacı hücrelere girmeye zorlayarak diğer tedavilerin başarısız olduğu durumlarda mükemmel sonuçlar elde etmektedir. Son olarak, (23)’te gösterildiği gibi sadece elektrik pulsları bile kendi başına immünolojik açıdan adjuvan etki göstermekle kalmaz, aynı zamanda EKT immünojenik hücre ölümüne de neden olur (29) ki bu da kansere yönelik hassas tıptaki başarının önemli bir parçasıdır.
Veterinerlik ortamında çoğu zaman EKT, insan hastalar için yapılan standart prosedürler izlenerek gerçekleştirilir ve bu da etkisini azaltmaktadır. Veteriner hekimlikte EKT, hastaların kendine has özellikleri ve tedavi edilen türler arasındaki farklılıklar göz önünde bulundurularak uygulanmalıdır. Maksimum potansiyele ulaşmak için tedavinin uygun şekilde planlanması çok önemlidir. Elektrotun doğru seçimi hastanın anatomisine, tümörün konumuna, invazyon derinliğine ve boyutuna bağlı olmalıdır. Ayrıca, doğru ilacın ve doğru uygulama şeklinin seçilmesi de çok önemlidir.
Bu çalışmada, veteriner hekimler için yüzeysel tümörlere elektrokemoterapi uygulama rehberi sunulmaktadır. Bu rehber, hakemli dergilerde yayınlanmış verilere dayanmakta ve kullanıcıların soruları ve sık karşılaşılan zorlukların dikkatli bir şekilde derlenmesiyle hazırlanmıştır. Tedavinin etkisini azaltabilecek potansiyel sapmaların bir listesini ve bunların sonuçlarını hafifletmenin yollarını sunmaktayız. EKT uygulamasında bu sapmaların önlenmesi, bu rehberdeki bilgilerin doğru uygulanması kadar önemlidir.
MATERYAL, EKİPMAN VE HASTALAR
Hastalar
Temel amacımız, kanser hastalarına mümkün olan en iyi tedaviyi sunmak ve tedavinin başarı ihtimalini en üst düzeye çıkarmaktır.
Bazı hastalarda EKT tek başına çok iyi bir tedavi seçeneği olabilir ve mükemmel sonuçlar verebilir. Ancak veteriner hekimlikte, hastanın hastalığın çok ileri evrelerinde, EKT’nin tek başına etkili olamayacağı veya çok fazla seans gerektireceği büyük tümörlere sahip olması yaygındır. Bu durumlarda, EKT’nin diğer tedavi yöntemleriyle birleştirilmesi, daha sonra bu makalede anlatılacağı gibi son derece etkilidir. Bu nedenle EKT tek başına veya neoadjuvan, adjuvan veya cerrahi, kemoterapi veya radyoterapi ile eşzamanlı uygulanabilir (25, 30). Hastanın onkolojik durumuna göre uygun tedavi seçimi, en iyi sonuçların elde edilmesi için çok önemlidir.
Hasta sahibi, seçilen tedavinin beklentilerini ve alternatiflerini anlamalı ve ardından rızasını gösteren bir belge imzalamalıdır.
EKT’nin Endike Olduğu Durumlar
- Birinci basamak tedavileriyle tatmin edici bir şekilde tedavi edilemeyen histolojisi ne olursa olsun kutanöz veya subkutanöz tümörler (primer veya metastatik) (26, 31).
- Kanama, ülserasyon veya ağrı nedeniyle yaşam kalitesini etkileyen primer veya metastatik tümörler (26).
- Oral veya Nazal tümörler, tek başına tedavi olarak veya cerrahi ile kombinasyon halinde (8, 9, 32).
- Tam olarak rezeke edilmemiş tümörler (cerrahi skarlar, deri flepleri ve diğer cerrahi müdahaleler dahil) veya cerrahi sırasında güvenlik marjlarını genişletmek için (33).
- Diğer birinci basamak tedavilerin mümkün olduğu durumlarda seçmeli EKT tedavisi. Diğer tedavi seçenekleri hakkında kapsamlı bir açıklama yapılmalı ve bunlar hasta sahibi tarafından geri çevrilmelidir (31, 34).
- Elektrotlara erişimi olan (yüzeysel veya cerrahi yaklaşımla) primer veya metastatik tümörlerde kanser yükünün azaltılması (26, 35).
Sistemik tedavi altındaki hastalarda, tedaviye iyi yanıt vermeyen lezyonların tedavisi için.
- Cerrahi öncesi büyük tümörlerde, nükssüz sağkalımı arttırmak için.
- Tedavi seçeneği olmayan hastalarda, palyatif amaçla yaşam kalitesini artırmak için.
Tedavi Öncesi Yapılacak Testler ve Dikkat Edilecek Hususlar
Tedavi öncesi zorunlu testler aşağıda belirtilmiştir.
Gebe veya emziren hayvanlar; bleomisin ve sisplatin gelişmekte olan fetüse zarar verebileceğinden kısırlaştırılmamış dişilerde özel dikkat gösterilmelidir.
- Böbrek ve karaciğer fonksiyonlarını belirlemek için yapılan kan testleri normal parametreler içinde olmalıdır. Hematolojik ve koagülasyon parametreleri normal olmalı ve basit bir cerrahi prosedür için gerekenlerle karşılaştırılabilir olmalıdır.
- Kardiyolojik muayene de dahil olmak üzere anestezi riski değerlendirilmelidir.
Tümörün histopatolojik tanısı.
- Metastaz veya diğer komorbiditelerin varlığını değerlendirmek için üç poz toraks röntgeni, batın ultrasonu, CT taraması veya gerekirse MR dahil olmak üzere tam onkolojik evreleme.
- Her bir vakaya göre, EKT’den önce ağrı kesici tedavi gerekebilir ve sonrasında yeniden ayarlanabilir.
- Daha önce bleomisin almış hastalarda riski mutlaka değerlendirin; köpekler için maksimum kümülatif doz 200.000 IU/m2 iken kediler için bu doz henüz belirlenmemiştir (36). Bu doza ulaşan hastalar sisplatin (kediler hariç) veya intratümöral olarak uygulanan kalsiyum ile tedavi edilmelidir. Bu mümkün değilse, başka bir tedavi seçeneği düşünülmelidir.
- Bleomisin veya sisplatine karşı alerji veya aşırı duyarlılık öyküsü.
Köpek ve kedilerde, tedavinin uygulanması zor olabileceğinden ve başarı şansı azaldığından, aşağıdaki hususlara bilhassa dikkat edilmelidir.
- Larinkste veya larinkse yakın tümörler. Anestezi prosedürüne başlamadan önce lezyonun entübasyonu engellemediğinden emin olun. Tedaviden sonra lezyonun şişeceğini ve hava yolunu tıkayabileceğini göz önünde bulundurun. Lezyon büyükse ve hava yolunun önemli bir kısmını tıkıyorsa, lezyonu debulk edin ve tümöral yatağı tedavi edin. Geçici veya kalıcı trakeostomi, tedaviden sonra ve iyileşme sırasında hava yolu tıkanıklığı riskini azaltmak için iyi bir seçenek olabilir.
- Dildeki tümörler. Dil terminal irrigasyona sahiptir ve elektrik pulslarının çok geniş bir şekilde uygulanması, vasküler kilit olgusu nedeniyle rostral kısmının nekrozuna neden olabilir. Eğer tümör kaudal yerleşimli ise, tedaviden sonra hava yolunu tıkayabilir. Her iki durumda da cerrahi debulking ve ardından tümöral yatakta EKT uygulamayı düşünün. Erken iyileşme dönemlerinde beslenme tüpüne ihtiyaç duyulabilir.
- Kribriform plakayı, retro-orbital bölgeyi, paranazal sinüsleri veya diğer ulaşılamayan yapıları tehlikeye atan tümörler. Nazal kanalın kaudal bölgesinde bulunan tümörler, ulaşılması çok zor olduğu için standart elektrotlar kullanılarak başarılı bir şekilde tedavi edilemeyen etmoidal hücreleri istila edebilir. Bu da sonuçta tedaviyi başarısızlığa uğratacaktır. Cerrahi artı radyoterapi gibi diğer tedavi yöntemlerini düşünün.
Atların tedavisi için özel hususlar.
- Genel anestezi altında tedavi edilmeli ve prosedür için uygun cerrahi öncesi muayeneleri yapılmalıdır. Veteriner hekimin takdirine bağlı olarak tetanoz aşısı veya hiperimmün serum uygulanabilir.
- IV yolun kullanımı, gereken yüksek ilaç miktarları göz önüne alındığında oldukça masraflıdır ve bu konuda yeterli sayıda güvenlik çalışması bulunmamaktadır. Ayrıca, insan tüketimine sunulan hayvanlarda intravenöz sitostatiklerin kullanımından kaçınılmalıdır.
- En sık tedavi edilen neoplaziler sarkoidler, kutanöz malign melanom ve skuamöz hücreli karsinomdur ve bunların hepsinde iyi sonuçlar elde edilmiştir (19, 37). Diğer histolojiler, mevcut elektrotlar kullanılarak tedavileri uygun olduğunda uygulanabilir.
- Ülserli lezyonların tedavisi hayvanın yaşam koşullarına uyarlanmalıdır ve antibiyotik ve/veya repellant uygulaması gerekebilir.
Tümör Boyutunun ve Sayısının Değerlendirilmesi
En iyi tedavi stratejisini belirlemek için tüm lezyonları sayın ve ölçün. Tedaviye verilen yanıtı belgelemek için cetvel de kullanarak fotoğraf çekilmesi önerilir. Fotoğraflar her seferinde aynı açıdan ve perspektiften çekilmelidir. Ayrıca, tedavinin etkisini belgelemek için diğer görüntüleme yöntemleri de kullanılabilir. Tümör volümünü hesaplamak için aşağıdaki formülü kullanın,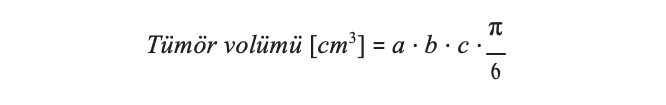
Aşağıda a, b ve c sırasıyla tümörün uzunluğu, eni ve kalınlığı belirtilmektedir. İnce tümörler için (veya lezyon kalınlığı ölçülemediğinde) aşağıdaki formülde görülebileceği gibi c’yi b ile değiştirin,
Tümöral yük, tedavi edilen hayvanın büyüklüğü bağlamında ele alınmalıdır, ancak tümörün büyüklüğü tek başına tedavi sonucu üzerinde önemli bir etkiye sahiptir.
Bu noktada, EKT’nin palyatif mi yoksa tedavi amaçlı mı uygulanacağı ve bu amaç için gereken seans sayısı belirlenmelidir.
Tedavi Amaçlı EKT
Şekli ne olursa olsun, 3 cm3’e kadar olan tümörler iyi sonuçlarla kolayca tedavi edilebilir. Ameliyatın zor olduğu durumlarda, ameliyat sonrası komplikasyonlardan kaçınmak için veya tümör önemli organlara yakın olduğunda cerrahiye alternatif olarak kullanılabilir (38-40).
Kalınlığı <1 cm olan geniş yüzeysel tümörler söz konusu olduğunda, EKT, 3 cm3 ‘ten büyük olsalar bile, birinci basamak tedavi yöntemleri başarısız olduğunda veya uygulanabilir olmadığında iyi bir seçenektir (38, 41-43).
Elektrot iğnesinin uzunluğu tümöral yatağı tedavi etme olasılığını azaltabileceğinden, tümörün kalınlığına özellikle dikkat edilmelidir. Lütfen, iğnelerin sadece iletken kısmının dikkate alınması gerektiğini unutmayın (bazı cihazlar, iğnenin uzun olmasına rağmen iğnenin bir kısmının izole edildiği elektrotlar kullanır). Tümör kalınlığı, iğnenin iletken kısmının uzunluğundan daha az olmalıdır, bu da üreticiye bağlı olarak genellikle 1 ila 4 cm arasında değişir. Tümör iletken iğnenin uzunluğundan daha kalınsa, tümör yatağının ve kenarlarının EKT’sini takiben debulking yapılması önerilir. Eğer debulking yapılmazsa, tedaviyi tamamlamak için ikinci bir EKT seansı planlanmalı ve ilk seansa yanıt alındıktan sonra uygulanmalıdır. Bu ek EKT kürleri tedavi planlamasının bir parçasıdır ve hastanın ilk değerlendirmesi sırasında belirlenmelidir (44). Şekil 1‘e bakınız.
Palyatif Amaçlı EKT
EKT çok faydalı bir tedavi stratejisidir ve bu bağlamda, küratif alternatifler olmadığı sürece, yüzeysel olarak geniş veya büyük tümörler yaşam kalitesini artırmak için tedavi edilebilir (45).
Hasta Sahibinin Bilgilendirilmesi ve Bilgilendirilmiş Onam
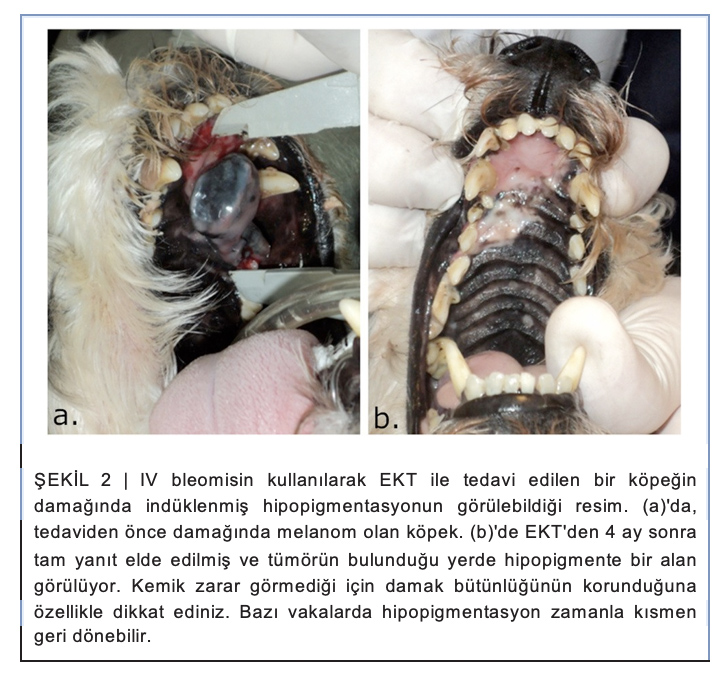
Hasta sahipleri tüm tedavi seçenekleri, EKT’nin yararları ve sakıncaları ve olası yan etkileri hakkında bilgilendirilmelidir. Hasta sahipleri ayrıca tedavinin olası sonuçları hakkında da bilgilendirilmelidir. Bu konular açıklığa kavuşturulduktan sonra, hasta sahibi tarafından bilgilendirilmiş onam formu imzalanmalı ve bu form şunları içermelidir (i) prosedür için kullanılan ilaçla ilişkili riskler, örneğin yüksek dozlarda bleomisin kullanan bir hastada akciğer fibrozisi ve alopesi ve/veya tedavi edilen derinin pigmentasyonunda değişiklik riski (bkz. Şekil 2), (ii) tedavi sonrasında oluşabilecek ağrı riski, ki bunun için yeterli bir yönetim planı sağlanmalıdır, (iii) fistül oluşumu, geniş nekroz veya tümörün dokuyu tamamen kapladığı durumlarda
tedavi sonrası rekonstrüktif cerrahi gerektirebilecek ciddi anatomik defekt riski ve (iv) bazı durumlarda daha fazla tedavi seansına ihtiyaç duyulması ihtimali.
Elektroporatörler ve Puls Ayarları
EKT için kabul edilen standart puls parametreleri, kullanılan elektrotlara bağlı olarak 1.000-1.300 V/cm voltaj-mesafe oranı ile 1-5.000 Hz arasında tekrar eden frekanslarda verilen 100 µs’lik 8 monopolar kare dalgalı pulslardır. Tekrar eden frekans alınan yanıtı etkilemez. 100 Hz’den daha yüksek frekanslar kullanıldığında, sadece kas kasılması görülür ki bu da hastanın toleransını ve konforunu artırır (46, 47).
Monopolar kare dalgalı pulslar EKT için tercih edilen puls türüdür. Bununla birlikte, birçok bipolar puls konfigürasyonu da iyi sonuçlar vermiştir (34, 48). Gen elektrotransferinde veya EKT’de bipolar puls kullanmanın faydaları olup olmadığını belirlemek için daha fazla araştırmaya ihtiyaç vardır (24, 49).
Veteriner hekimlikte EKT uygulamak için birçok elektroporatör mevcuttur. Bunlardan bazıları laboratuvar kullanımı içindir ve diğerleri özellikle veteriner kliniklerinde kullanılmak üzere tasarlanmıştır.
Konfigürasyon hataları önlendiği için otomatik cihazlar tercih edilmektedir. Elektroporatör, akımın 8 pulsunun her birinde voltajı (düşme olmadan) koruyabilmelidir. Bu, jeneratörün yeterli miktarda maksimum güç çıkışı sağlayabilmesi halinde mümkündür. Deneyimlerimize göre, 35 A’lik güç çıkışları (puls süresinin 100 µs’si boyunca) her türlü tümörün tedavisi için yeterlidir.
Daima cihazın üreticisi tarafından sağlanan elektrotları kullanmak çok önemlidir. Bir hasta için seçilebilecek en iyi elektrotun seçimine ilişkin bilgiler aşağıdaki bölümde ele alınmaktadır.
Ayarlanabilir elektroporatör kullanılıyorsa, uygun şekilde ayarı yapılmalıdır. Bu amaçla, kullanılacak elektrotun iğneleri arasındaki mesafeyi kontrol edin ve kullanılacak voltajı elde etmek için bu mesafeyi cm cinsinden 1.000 ile çarpın. Örneğin, birbirinden 0,4 cm uzaklıkta iğne elektrotlar kullanıyorsanız, cihaz çıkış voltajını 400 V olarak ayarlamanız gerekir (1.000∗0,4= 400). Eğer deri üzerine plakalar uygulanıyorsa, mesafeyi 1.300 ile çarpmanız gerekir. Böylece, aynı örnekte, cihaz çıkış voltajını 520 V’a ayarlamanız gerekir (1.300∗0,4 = 520). Plakaların doğrudan tümör üzerine uygulanması durumunda, iğnelerde olduğu gibi 1.000 V/cm kullanın. Ardından puls uzunluğunu 100 µs’ye ve puls aralığını 100 µs ile 1 s arasına ayarlayın (5.000 ile 1 Hz arasında tekrarlayan frekans için). Cihazı 8 puls (50) verecek şekilde ayarlayın.
Kullanılan İlaçlar
EKT uygulamak için sadece 3 ilacın kullanımı onaylanmıştır; intravenöz veya intratümöral olarak uygulanan bleomisin, intratümöral olarak uygulanan sisplatin veya intratümöral olarak uygulanan kalsiyum. Her birinin kullanımı için gerekli olan karar verme yöntemi bir sonraki bölümde açıklanmıştır.
METODLAR: TEDAVİ
Anestezi
Plaka elektrotlar kullanıldığında bile tedavi genel anestezi altında yapılmalıdır. Puls verilmesiyle indüklenen hisler ve kas kasılmaları ağrılı olabilir ve hastayı strese sokarak ağrıya bağlı saldırganlığa yol açabilir (51).
EKT için gereken anestezi prosedürü, aynı bölgede yapılması düşünülen cerrahiyle benzerlik gösterir. Bunu uygulayacak olan profesyonelin uzmanlığına ve aşinalığına göre seçilmelidir.
Örnek olarak, köpekler ve kediler için uygulanan standart tedavi rejimi aşağıdaki gibi olabilir: (i) 0,5 mg/kg ksilazin ve 2 mg/kg tramadol intramüsküler verilerek premedikasyon; (ii) 3 mg/kg propofol intravenöz verilerek yapılan indüksiyon; (ii) inhale izofluran %2-3 ve intravenöz fentanil 2 µg/kg ile yapılan bakım tedavisi. Hastaların konforunu artırmak ve anestezik ilaçların dozunu azaltmak için anestezi uzmanının kriterlerine göre bölgesel anestezi de ilave edilebilir. Örneğin, burun tedavisi sırasında infraorbiter sinir bloğu uygulanabilir. Anti-enflamatuar ilaçlar işlem sırasında veya sonrasında kullanılabilir ve daha sonra görüleceği gibi sonraki günlerde de devam ettirilebilir.
Atlarda genel anestezi her zaman tavsiye edilir. Gereken anestezi seviyesinin derinliğini azaltmak için bölgesel-genel anestezi kombinasyonu ile birlikte standart bir tedavi rejimi uygulanabilir (52). İndüksiyon güvenli ve dikkatle seçilmiş bir ortamda gerçekleştirilmelidir. Hasta tüm prosedür boyunca doğru analjezik uygulama altında olmalıdır.
Küçük hayvanlarda, özellikle burun veya ağız tedavi edildiğinde, hasta tamamen uyanıncaya kadar anestezi sonrası gözlem çok önemlidir.
İlacın Kullanım Şekli
Hastayı tartarak başlayın. Ardından, tümöral volümleri hesaplamak için lezyonları ölçün. Ölçümlerden sonra, tümörün ve sınırlarının iyi bir şekilde görülebilmesi için tedavi edilecek alanın tüylerini kırpmaya devam edin. Tedavi edilecek tüm alanı (tümör ve marjinler) temizlemek ve dezenfekte etmek için iyot solüsyonu kullanın. EKT sonrası enfeksiyon riski çok düşük olsa da, steril elektrotların kullanılması veya üreticinin önerileri doğrultusunda sterilize edilmesi şiddetle tavsiye edilir (53).
Antineoplastik ilaçların seyreltilmesi ve uygulanması için eldiven ve laboratuvar önlüğü giyilmesi, yüz ve ağız maskesi kullanılması zorunludur. Mümkünse, II. sınıf laminer hava akış kabininde çalışılması tavsiye edilir (54).
İntravenöz
Lezyonun boyutuna bakılmaksızın tüm vakalar için intravenöz bleomisin kullanılmasını öneriyoruz (daha sonra açıklanacağı gibi sadece bleomisin intravenöz yolla kullanılabilir). Bu öneri birkaç nedene dayanmaktadır: (i) uygulama süresi dikkate alındığında tümör ve marjinlerinde ilacın yeterli şekilde dağılımı ve konsantrasyonu sağlanabilmektedir, (ii) intratümöral uygulama tekniğindeki hatalardan dolayı oluşabilecek ilaç konsantrasyonunun yetersiz kaldığı tümör alanlarının oluşması önlenmektedir, (iii) intratümöral uygulama sırasında oluşabilecek dökülme ve sızıntılar önlendiğinden ilacın uygulanması daha güvenlidir ve (iv) tek başına immün sistemi aktive ederek tedavinin indüklediği lokal immün yanıta katkıda bulunmaktadır (23).
İntravenöz bleomisinin atlar için önerilmediğini, çünkü çok fazla miktarda ilaca ihtiyaç duyulduğunu unutmayın. Bleomisinin gücü antimikrobiyal aktivite birimleriyle ölçülmektedir. Birçok ülkede bleomisin mg ya da Uluslararası Birim (IU) olarak dozlanırken, ABD’de kullanılan terim Birim (USP)’dir. Buna göre eşdeğerlik 1 USP ünitesi = 1 mg (etki gücüne göre) = 1.000 Uluslararası Ünite (IU) şeklinde olacaktır (55).
Hastanın kilosunu kullanarak aşağıdaki formül yardımıyla vücut yüzey alanını (BSA) hesaplayın.
Vücut yüzey alanı [m2] = k · weight[kg]2/3
Burada k köpekler için 0,101 ve kediler için 0,1’dir (56).
İntravenöz Yöntem için Uygulama Tekniği
İlaç bolus halinde 15.000 IU/m2 BSA dozunda (30-45 sn içinde) uygulanır ve maksimum doz 30.000 IU (2 m2 BSA’ya karşılık gelir) ile sınırlandırılır (50). Elektrik pulslarının uygulanması, ilaç tümöral dokuya yayıldıktan 5-8 dakika sonra başlayabilir.
Uygulamadan sonra, uygulanan Bleomisin dozunun yaklaşık yarısı renal atılımla elimine edilir, bu nedenle böbrek fonksiyonu azalmış hastalarda daha düşük doz kullanılabilir (57, 58). Bleomisinin başlıca yan etkisi olan akciğer fibrozisini önlemek için köpeklerde maksimum kümülatif dozun 200.000 IU/m2 olduğunu, kedilerde ise henüz belirlenmediğini unutmayın (36). İlaç, bleomisin hidrolaz enzimi tarafından dokularda metabolize edilir, bu enzim deri ve akciğerlerde çok düşük konsantrasyondadır ve bu dokuların bleomisin toksisitesine olan hassasiyetine açıklık getirmektedir (58).
Veteriner hastaların boyutları ve vücut ağırlıkları arasındaki büyük fark, tedavi sürecini tayin ederken göz önünde bulundurulmalıdır. Bu süre birçok faktörden etkilenebilir, bunların arasında dokudaki kan akış hızının (59) kalp atış hızından etkilenmesi de vardır. Bilindiği gibi, kalp hızı vücut ağırlığıyla ilişkilidir (60), bu nedenle kediler ve küçük köpekler için 5-25 dakika ve diğerleri için 8-40 dakikaya yakın bir tedavi aralığını takdiri olarak düşünebiliriz. İnsan tıbbında da benzer şekilde, 65 yaşından genç hastalarda 5-15 dakikalık bir tedavi aralığı varken, daha yaşlı hastalar için 8-40 dakikalık tedavi aralığı söz konusudur ve bu fark böbrek fonksiyonuyla ilişkilidir (61). Farklı tür ve vücut ağırlığına sahip hastalarda tedavi aralığını doğru bir şekilde belirlemek için bleomisin farmakokinetiği üzerine daha fazla çalışmaya ihtiyaç vardır.
Pulsların uygulanması için en etkili sonuç, ilacın uygulanmasından 40 dakika sonra görülür. Ancak bu süre yaşlı hastalarda ve böbrek fonksiyon bozukluğu olan hastalarda uzatılabilir. Her durumda, hala lezyonlar üzerinde devam eden bir etki olduğundan, bu süreden sonra bile kalan lezyonlara elektrik pulslarının uygulanmasına devam edilmesi önerilir. Bu lezyonların kontrol sırasında tanınması için işaretlenmesi tavsiye edilir (57, 62).
İntratümöral Yöntem
İntratümöral uygulama 2 cm3 ‘e kadar olan küçük tümörlerde uygulanabilir (63). Büyük tümörlerde, özellikle atlarda ve kedilerde bu yöntem zorlayıcı olabilir. Buna karşın, intravenöz yöntem her durumda ilacın yeterli şekilde dağılmasını sağlayacaktır ve bu nedenle mümkün olan her durumda tercih edilmelidir.
Bleomisin, sisplatin ve kalsiyum intratümöral olarak uygulanabilir. Elektrik pulslarının verilmesi uygulamadan hemen sonra başlamalıdır.
Bleomisin
İntratümöral uygulama için önerilen bleomisin konsantrasyonu 1.000 IU/ml’dir ve doz 250 IU/cm3 tümördür (50).
İntravenöz yöntemle uygulanacak dozdan daha düşük miktarda verilen toplam dozla tümör tamamen infiltre edilmelidir. Bu mümkün değilse, önceki bölümde açıklanan koşullar altında intravenöz yöntemi kullanın.
Kaplumbağalar, yılanlar veya kuşlar gibi istisnai türlerde, bu hayvanlarda sistemik bleomisinin dozajı ve etkileri hakkında yeterli bilgi olmaması nedeniyle intratümöral yöntem tercih edilmektedir.
Sisplatin
Sisplatin kullanılırken önerilen konsantrasyon 1 mg/ml’dir ve önerilen enjeksiyon dozu tümör hacmini ilaçla doldurmaktır (50). Sisplatinin önerilen veya daha yüksek konsantrasyonda bulunmaması durumunda bleomisin kullanılmasını öneriyoruz. Daha düşük bir konsantrasyonun kullanılması mümkündür ancak hastanın yeniden tedaviye ihtiyacı olabileceğinden yakın takip gerektirir (64).
Sisplatin atların tedavisi için iyi bir seçenektir (11, 19). Buna karşın, bu ilaç kedilerde önerilmemektedir (65).
Sisplatin mevcut değilse karboplatin kullanılabilir, ancak etkinliği sadece in vitro olarak kanıtlanmıştır (66).
Kalsiyum
Kalsiyum klorür kullanıldığında önerilen konsantrasyon 9 mg/ml’dir. Tümör hacminin yarısına eşit hacimde kalsiyum klorür solüsyonu enjekte edin (67, 68). Kalsiyum ile elektroporasyon iyi sonuçlar verebilir ve bleomisin veya sisplatin mevcut olmadığında üçüncü seçenek olarak kullanılabilir. Ayrıca küçük tümörlerle sınırlı tutulmalıdır (67).
İntratümöral Yöntem için Uygulama Tekniği
İğneyi tümörün merkezinde tek bir noktaya yerleştirin ve dökülmeyi önlemek için ilacı radyal olarak uygulayın. İlacı enjekte ederken, ilacın dökülmesini veya sızmasını önlemek için iğneyi çok hızlı çıkarmamaya dikkat edin. Bu teknikle sadece küçük tümörlerin tedavi edilmesi gerektiğinden, güvenli marjinler, lezyondan ilaç difüzyonu ile kaplanır ve marjinlerin başarılı bir şekilde tedavi edilmesi için yeterli konsantrasyon sağlanır. Sağlıklı doku, önceki ilaçlardan herhangi biri tarafından infiltre edilirse nekrotize olabilir ve bu nedenle çevredeki sağlıklı dokuya doğrudan enjeksiyondan kaçınılmalıdır (69).
Elektrik pulsları, ilacın uygulanmasından hemen sonra verilmelidir, çünkü ilaç hızlı bir şekilde uçup gitmektedir (50).
Tedavi edilecek birden fazla lezyon varsa, ilacın uygulanması ve pulsların teker teker verilmesi önerilir. İlacın ilk etapta tüm tümörlere uygulanması ve puls dağıtımının bundan sonra gerçekleştirilmesi durumunda, en son puls uygulanacak olanların yeterli ilaç konsantrasyonuna sahip olmayabileceğini unutmamak önemlidir.
İntravenöz bleomisin verilmesinin mümkün olmadığı atlarda, büyük tümörler şu şekilde tedavi edilebilir; lezyonun yarısına enjekte edin ve hemen ardından puls gönderin. Sonra diğer yarısını enjekte edin ve puls gönderin. Bu şekilde büyük lezyonlar başarılı bir şekilde tedavi edilebilir.
Elektrot Seçimi
Elektrot Türleri ve Avantajları
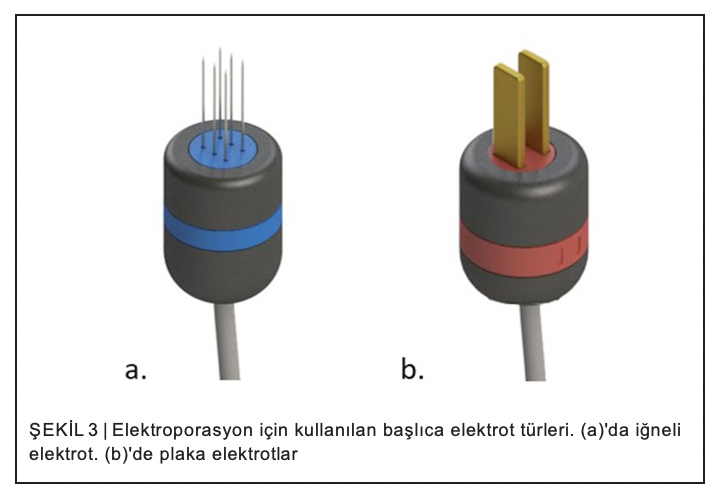
Genel olarak çoğu cihaz iki tip elektrotla birlikte gelir; iğne elektrot ve plaka elektrot (bkz. Şekil 3).
Her zaman cihazın üreticisi tarafından sağlanan elektrotları kullanın ve bunlar için öngörülen maksimum kullanım sayısına uyun. Öngörülen maksimum kullanım sayısının aşılması tedavinin etkinliğini önemli ölçüde düşürebilir. Varsa, tek kullanımlık elektrotlar önerilir.
İğne Elektrotlar
Bu tip elektrotlar, tümörlerin büyük çoğunluğunda tedavi için önerilmektedir.
Veteriner hastalarda deri, insanların cildinden daha kalındır (70) ve tümör seviyesindeki elektrik alanının homojenliğini ve yoğunluğunu engelleyebilecek çok dirençli bir tabakadır. Dahası, deri kalınlığı ve dolayısıyla derinin elektrik empedansı, tür, ırk, yaş ve tümörün vücudun hangi bölgesinde olduğu gibi birçok faktöre bağlı olarak son derece değişkenlik göstermektedir. İğneler kullanılarak bu kalın tabaka aşılır ve elektrik alanı yeterli bir şekilde dağıtılarak uygulanabilir. Bu nedenle iğne elektrotlar her zaman daha çok tercih edilir.
İğneler genellikle birbirinden 0,4-0,5 cm uzaklıkta, üçlü veya dörtlü iki sıra halinde yerleştirilmiştir. Altıgen gibi aynı şekilde işleyen başka örnekler de vardır.
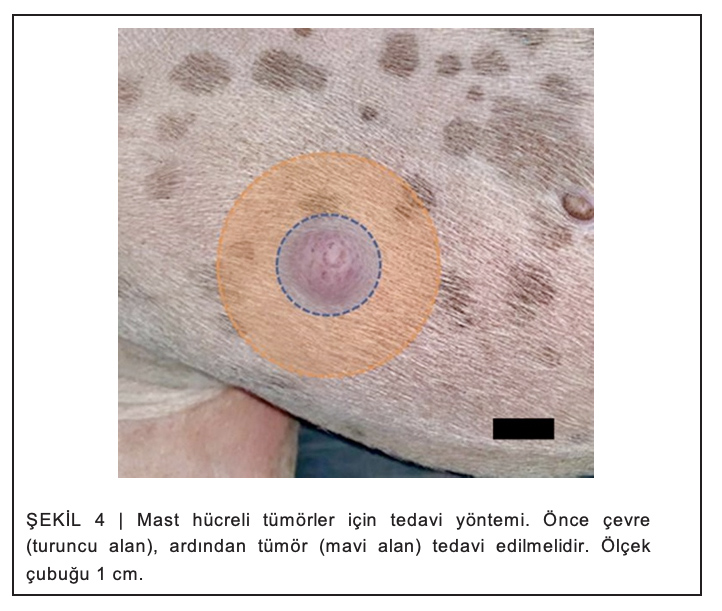
Tümörü yeterince tedavi etmek için tüm tümör yüzeyi kaplanmalıdır. Özellikle mast hücreli tümörler çevreden merkeze doğru spiral olarak tedavi edilmelidir (bkz. Şekil 4). Elektrik alanı elektrotların dışında çok hızlı bir şekilde kaybolduğundan, tedavi edilmemiş alanlar bırakmamak için yapılan uygulamada asgari ölçüde süperpozisyon gereklidir. Eğer tümör iğnelerin uzunluğundan daha kalınsa, cerrahi debulking gerekebilir. Ayrıca, tümörün büyümemesi koşuluyla, bölgenin aşırı tedavisinden kaçınmak için en az 4 hafta arayla birden fazla seansta tedavi edilebilir. Tümöral dokularda büyüme görülürse, bir sonraki tedavi seansı mümkün olan en kısa sürede yapılmalıdır. Tümörün ilk seansta sadece kısmen tedavi edilmesi istisnai bir durumdur. Bu durumda, tedavi edilmeyen dokular endişe edilmeden ertesi gün tedavi edilebilir.
Daha önce tedavi edilmiş bir tümörün ne zaman yeniden tedavi edileceğine ilişkin karar vermek için lütfen Takip ve Tedavinin Tekrarlanması bölümüne bakın.
Paralel Plakalı Elektrotlar
Paralel plakalı elektrotlar, birkaç milimetre invazyonlu yüzeysel lezyonları tedavi etmek için çok kullanışlıdır. Bu tür elektrotların tedavi derinliği plakalar arasındaki mesafeye göre değişmektedir (71). Şekil 5’te gösterilen modele göre, plakaları birbirinden 4 mm uzaklıkta olan elektrotlarda maksimum tedavi derinliği <3 milimetredir. Bundan daha derine invaze olan lezyonlar iğne elektrotlarla tedavi edilmelidir. Unutulmamalıdır ki, yüzeysel lezyonları deriden tedavi etmek için voltaj-mesafe oranı 1.300 V/cm olmalıdır (72). Ancak, debulking cerrahisinden sonra tümöral yatağın tedavisi için 1.000 V/cm yeterlidir. Deri çıkarıldıkça, elektrik akımı dokuların daha derin kısımlarına ulaşabilir (71).
Plakalı elektrotlar, göz kapaklarını ve plakaların arasına yerleştirerek kulakları tedavi etmek için oldukça kullanışlıdır.
Kontak elektrotlar ve L şekilli elektrotlar gibi diğer tasarımlar da plaka elektrotlara benzer şekilde çalışır. Bu tür elektrotlar sadece yüzeysel tümörlerin tedavisinde kullanılır ve plaka elektrotlarda olduğu gibi dokular iletken parçaların arasına yerleştirilerek tedavi edilemez. Özellikle bazı cihazlarda L şeklindeki elektrot 4 puls verecek şekilde yapılandırılmıştır ve bu nedenle iki puls sinyali arasında ortogonal rotasyon gereklidir.
Doku ile elektrotlar arasındaki teması daima kontrol edin (73).
Eğer yeterli değilse, elektrik dağılımını ve dolayısıyla tedavinin sonucunu iyileştirmek için iletken jel kullanılmalıdır. Jelin iletkenliği tedavi edilen dokuya benzer olmalıdır. Genel kullanım amacıyla ultrasonografi jeli yeterlidir. Tümör ve elektrot arasındaki teması iyileştirmek için aşırı miktarda jel kullanmanın yetersiz jel kullanmaktan daha iyi olduğunu unutmayın (74). Elektrik akımının akışını engelleyerek tedavinin etkisini azaltabileceğinden vazelin kullanmaktan kaçının. Ayrıca, istenmeyen doku hasarına veya aşırı nekroza neden olabileceğinden, özellikle sağlıklı dokuda iki uygulamanın üst üste yapılmasından kaçının (ayrıca bkz. Bölüm Alınabilecek Önlemler).
Güvenlik Önlemleri
Kullanılan elektroporatör, yeterli puls iletimi sağlamak için ark hatası algılama, kısa devre algılama ve düşük voltaj alarmı dahil olmak üzere temel güvenlik standartlarına uygun olmalıdır.
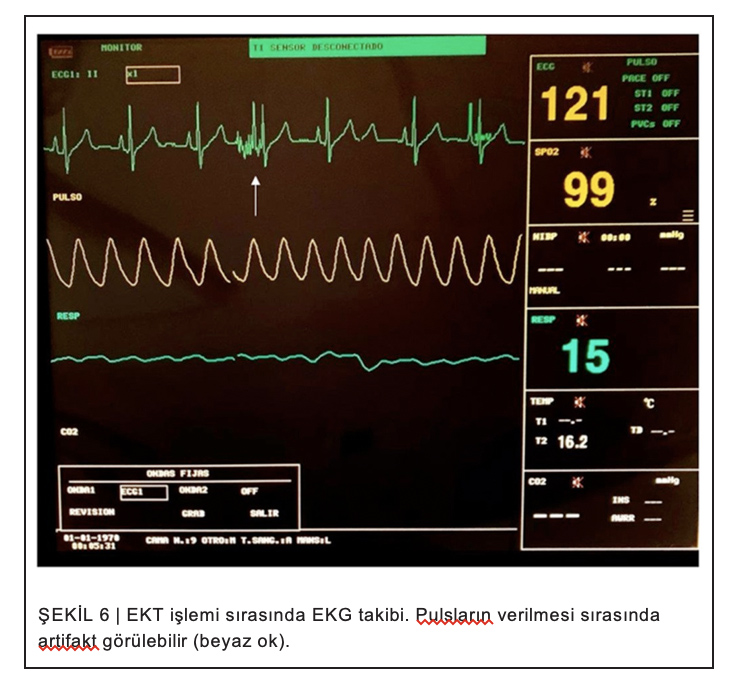
EKG monitörlerindeki artefaktlar, cihazlar arasındaki elektriksel etkileşim nedeniyle puls verme esnasında görülebilir ve bunlar aritmi veya başka bir kardiyak değişiklikle karıştırılmamalıdır (bkz. Şekil 6).
Metalik cerrahi aletler elektrotlardan ve tedavi alanından uzak tutulmalı ve puls verme sırasında temastan kaçınılmalıdır. Bu konuya Alınabilecek Önlemler bölümünde değinilecektir..
Tedavi Sonrası Antibiyotik ve Analjezi
Profilaktik antibiyotikler işlemden önce veya sonra ağızdan veya kas içine uygulanabilir.
Non-steroid anti-inflamatuar ilaçların (NSAİİ) kullanımı ağrının kontrol edilmesinde genellikle tavsiye edilen bir seçenektir, çünkü tedaviden sonra tedavi edilen dokunun inflamasyonu ağrıyı tetikleyebilir. Büyük lezyonlarda, NSAİİ’lerin opioidlerle birlikte kullanılması faydalı olabilir. Tedavi burun, dil, göz kapakları veya larinkse yakınsa, kortikosteroidlerin kullanımı, daha büyük anti-enflamatuar etki göstermeleri nedeniyle ilk 48 saat boyunca NSAİİ’lere tercih edilir. NSAİİ’ler kortikosteroidlerin kesilmesinden sonra kullanılabilir. Ancak, insan tıbbında yaygın olan her ikisinin aynı anda kullanımı, yan etkileri artırdığı için köpek ve kedilerde endike değildir (75).
Yara Bakımı
Tedaviden sonra yara için pansuman gerekmez. Tedaviyi takip eden günlerde, tedavi edilen bölgede akıntı olabilir ve bu akıntı hasta sahibi tarafından temizlenebilir. Elizabeth yakalar kedi ve
köpeklerde hayvanın tedavi edilen bölgeyi yalamasını önlemek için kullanılabilir.
SONUÇLARIN DEĞERLENDİRİLMESİ
Takip ve Tedavinin Tekrarlanması
Takip, hastaların ihtiyaçlarına göre bireysel olarak planlanır ve tedaviden 15 gün sonra ve 1, 2, 4 ve 6 ay sonra önerilir. Her takipte, tedaviye verilen yanıtı belgelemek için lezyon ölçülmeli ve fotoğraflanmalıdır.
Tümör tedavi edildikten sonra, çok az nekrozla veya hiç nekroz olmadan yavaşça küçülür. Bleomisinin etki mekanizması DNA iplikçiklerinin kesilmesinden oluşur ve hücreler bölünmeye çalışırken ölür. Bu nedenle, tümöral hücreler ölmek üzere “işaretlenir”, ancak sadece bölünmeye çalıştıktan sonra ölürler (58, 62). Lezyon küçülmeye devam ettiği sürece, daha fazla tedavi seansına gerek yoktur, çünkü zaten tedavi edilmiş hücreleri tedavi etmenin bir faydası yoktur. Aksine, dokunun nekrozuna neden olabilir. Maksimum terapötik etki 6-8 hafta sonra görülür, ancak daha uzun sürebilir. Bazen tümör durağan hale geçerek 2 veya 3 ay sonra tekrar küçülmeye başlar.
Yeni bir tedavi seansı planlamadan önce, bir sonraki seansı kesin bir zamana göre gerçekleştirmek yerine tam yanıt beklenmelidir. Bu, daha önce tedavi edilmiş bir lezyonun yeniden tedavi edilmesi için de geçerlidir.
Daha önce tedavi edilmemiş dokular veya tümörün tedavi edilmeden bırakılmış kısımları olması durumunda (örneğin atlarda çok büyük lezyonlar olması durumunda), bu tedavi edilmemiş dokuları tedavi etmek için seansı ertelemeye gerek olmadığını unutmayın. Tedavi edilen lezyonların tekrar büyümesi durumunda, yeni tedavi seansı geciktirilmemelidir.
Tümör lizis sendromu çok nadir görülse de, büyük tümörler tedavi edilirken bunu önlemek için özel önlemler alınmalıdır, her durumda hızlı tanı ve hızlı tedavi esastır.
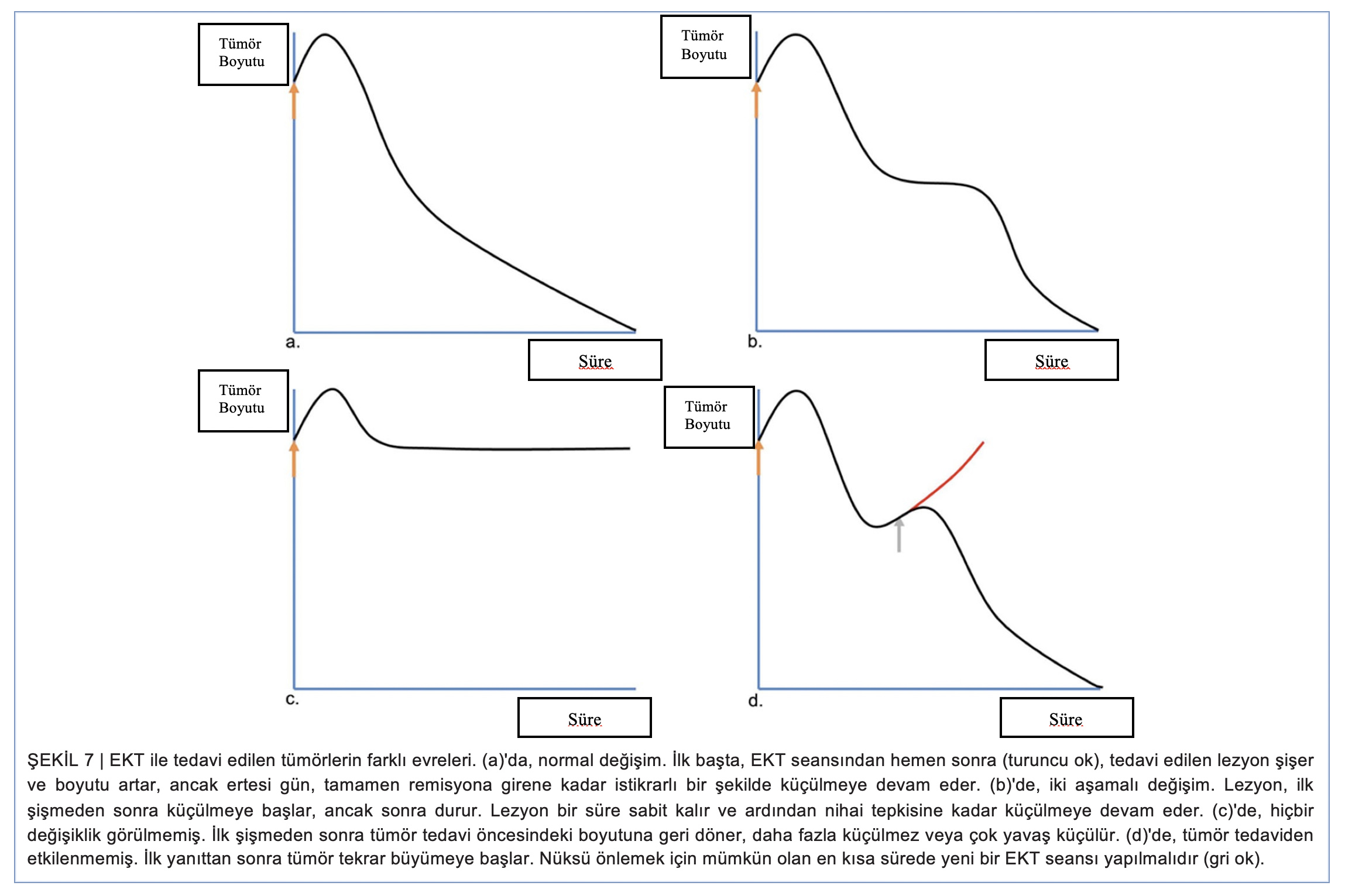
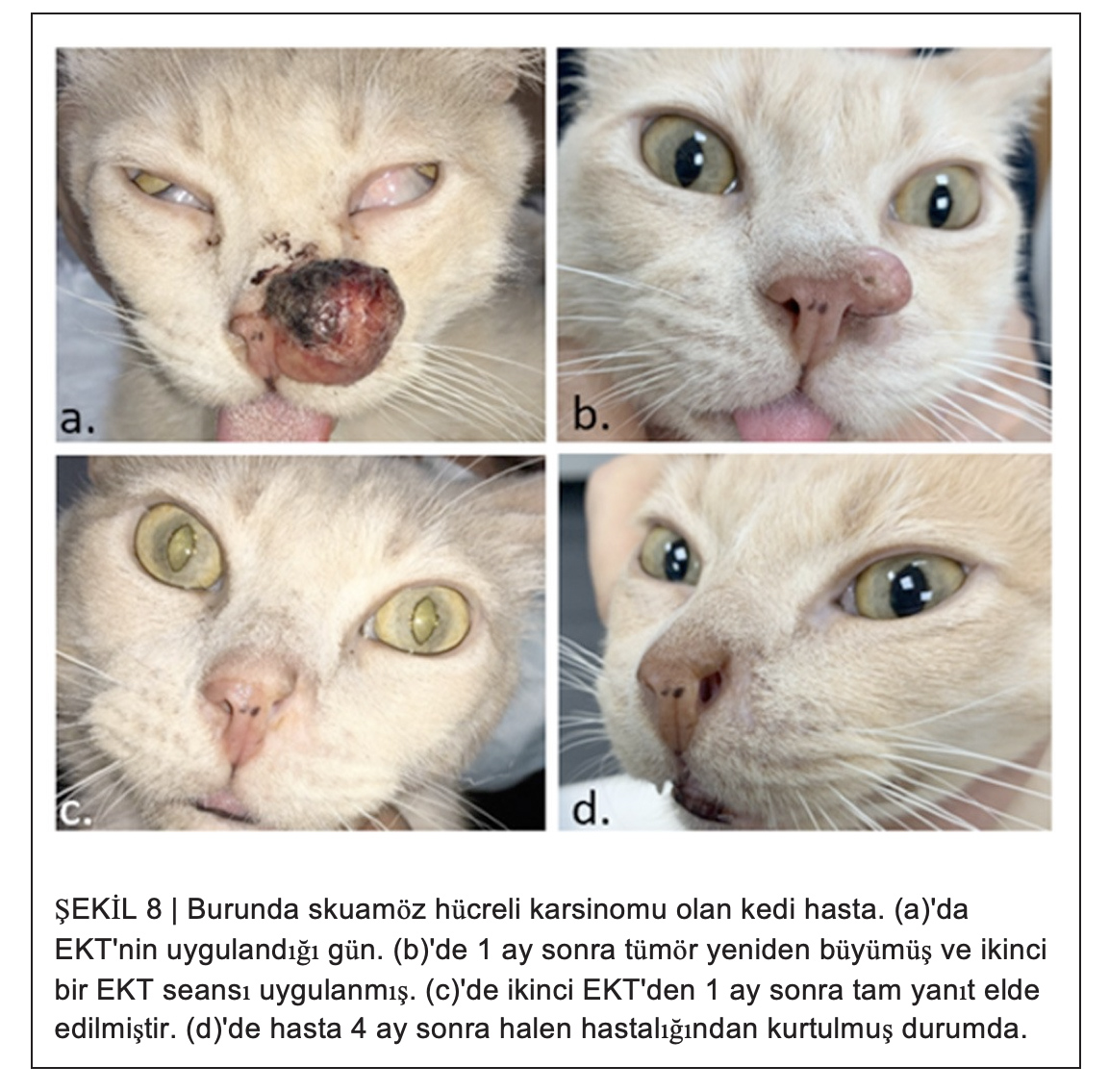
EKT ile tedavi edilen bir tümörün takibinde dört çeşit değişiklik görülebilir. Normal değişim çoğu vakada görülen durumdur. Tümör başlangıçtaki şişmenin ardından küçülür ve nihai yanıt elde edilene kadar küçülmeye devam eder (Şekil 7a). Bazen, başlangıçta lezyon bir önceki gibi davranır, ancak kısa bir süre sonra küçülmeyi durdurur. Belirli bir süre boyunca aynı boyutta kalır, ardından küçülmeye devam eder. Buna iki kez değişim diyoruz (Şekil 7b). Bu, hücre bölünme döngüsüne giren ve DNA iplikleri bleomisin tarafından kesildiği için hemen öldürülmeden sadece o anda ölen bölünmeyen tümöral hücrelere bağlanabilir. Bir başka değişim türü de tedaviden sonra yüksek sayıda durağan hücre popülasyonu nedeniyle belirgin bir küçülme göstermeyen lezyonlarla karakterizedir (bkz. Şekil 7c). Biz buna değişiklik görülmemesi şeklinde adlandırıyoruz. Tümörün tedaviden etkilenmemesi ise, ilk küçülmeden sonra tümörün tekrar büyümeye başlamasıyla görülür (bkz. Şekil 7d). Bu durumda, tümör yeterince tedavi edilmediği için gecikme olmaksızın yeni bir tedavi seansı planlanmalıdır (bkz. Şekil 8). Dört vakada da yanıt aynı olabileceğinden, tümör değişiminin alınan yanıttan farklı olabileceğine dikkat etmek önemlidir. Tümör değişimini anlamak, tedavinin tekrarlanıp tekrarlanmayacağını belirlemek için çok önemlidir. İlk üç değişim tipinde beklenmesi ve lezyonun yakın takibinin yapılması önerilir. Özellikle iki kez görülen değişimde veya değişimin görülmediği durumlarda, tümör tedaviden etkilenmeyebilir. Bu özellikle önemlidir, çünkü ilk üç değişim türünden birini takip ederek gelişen lezyonların tedavisi gereksiz olabilir ve hatta aşırı tedavi nedeniyle doku nekrozuna yol açabilir. Durağan seyreden herhangi bir lezyonla ilgili şüpheler varsa, tümör kalıntısının rezidüel skar dokusuyla karıştırılmaması için biyopsi yapılması önerilir.
Tekrarlanan tedaviler arasında olması gereken minimum süreye ilişkin herhangi bir veri bulunmamaktadır, ancak intravenöz bleomisin kullanıldığında en az 4 hafta tavsiye edilmektedir.
Aşağıdaki durumlarda tedaviyi tekrarlamayı düşünün
– Lezyon ilk seansta yeterince tedavi edilmemiş.
– Lezyon büyümeye başladı
– Yeni lezyonlar gelişti.
Diğer Tedavilerle Kombinasyon
EKT diğer tedavileri engellemez, aksine onların etkinliğini artırabilir. Bu nedenle, cerrahi (10, 44, 51), kemoterapi (30), immünoterapi (24, 76) ve radyoterapi (77) gibi birçok standart tedavi EKT ile birlikte daha etkili olabilir (25).
3-4 cm3’ten büyük tümörler için EKT, ameliyatın daha küçük çaplı yapılması için neoadjuvan sitoredüktif bir araç olarak ameliyatla kombine edilebilir ve böylece fonksiyon veya
organ korunabilir. EKT ayrıca yetersiz rezeke edilmiş marjinleri temizlemek için adjuvan bir tedavi olarak da kullanılabilir. Ayrıca, rezeksiyonun tümöral yatağını temizlemek için intraoperatif olarak da kullanılabilir (10, 25, 44, 51).
Kemoterapi veya metronomik kemoterapi EKT’ye adjuvan olarak kullanılabilir. Bununla birlikte, EKT’nin bağışıklık sistemini aktive eden faydalı etkisi göz önünde bulundurulduğunda, sistemik kemoterapinin immünosupresif etkisiyle tedaviye alınan yanıt olumsuz yönde değişebilir (29). EKT ile neoadjuvan, eşzamanlı veya adjuvan kemoterapinin kombinasyonunda olası risklerin faydalardan daha ağır basıp basmayacağı dikkatle değerlendirilmelidir (25).
Radyoterapi, özellikle elektrotların erişemeyeceği bir alanı istila eden tümörler için EKT ile birlikte kullanılabilir. Bunun tersi de mümkündür, EKT radyoterapiden sonra radyorezistan nüksleri tedavi etmek için kullanılabilir (77, 78).
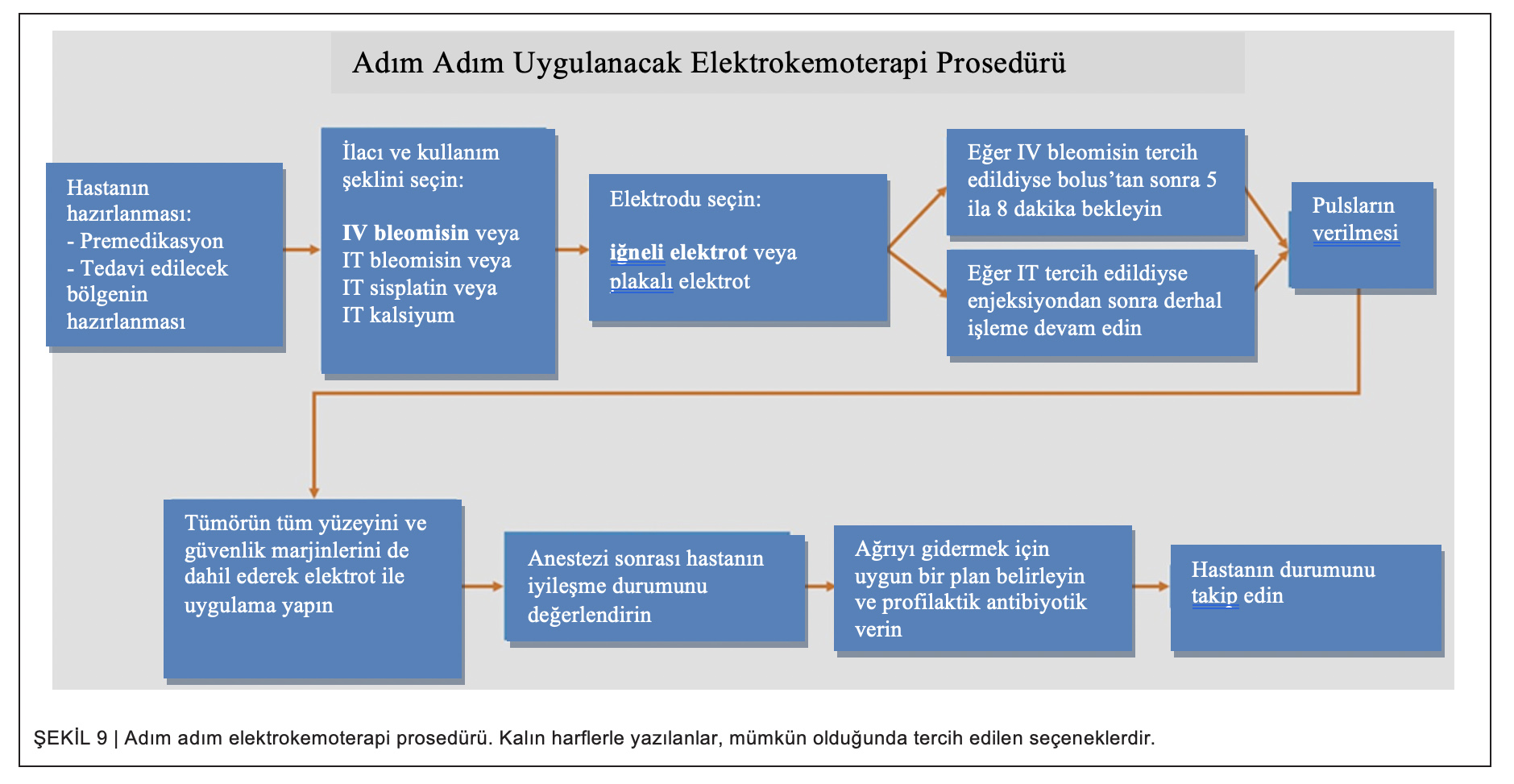
Son olarak, tedavinin nasıl gerçekleştirileceğine dair adım adım uygulanacak prosedür Şekil 9‘da gösterilmiştir.
UYGULANABİLECEK TAVSİYELER: PROSEDÜRDE SIKLIKLA GÖRÜLEN VE SONUÇLARIN DAHA İYİ OLMASI İÇİN KAÇINILMASI GEREKEN SORUNLAR
Hasta ile İlgili Konular
Sorun
Bazen ilk konsültasyon ile EKT prosedürü arasında çok fazla zaman geçebilir. Çok aktif tümörlerde bu durum hastanın durumunu tamamen değiştirebilir ve EKT’nin hala en iyi tedavi seçeneği olduğunu doğrulamak için yeniden evreleme gerekebilir.
Tavsiye
EKT öncesi yapılacak tetkikler tedaviden en fazla 4 gün önce yapılmalıdır. Gerekirse yeni görüntüleme tetkikleri isteyin.
Sorun
Bir öncekinde olduğu gibi, ilk konsültasyon ile EKT arasında uzun bir süre geçerse, tümör çok büyümemiş olsa bile, hasta ciddi şekilde kötüleşebilir. Bu, özellikle yeterli biçimde beslenmeyi engelleyen tümörler için geçerlidir. Bu durum anestezi riskini artırabilir ve işlem imkansız hale gelebilir.
Tavsiye
EKT tedavisinin en iyi koşullar altında gerçekleştirilmesi amacıyla gerekli klinik desteği (yeterli hidrasyon, beslenme takviyesi ve yeterli analjezi) sağlayacağınızdan emin olun.
Ciddi derecede kötüleşmiş hastalarda lezyonun sadece yarısını tedavi etmek mümkündür. Birkaç gün içinde hastalığın seyri olumluya dönerse, lezyonun ikinci yarısını mümkün olan en kısa sürede tedavi edin.
Tedavi Yöntemi ile İlgili Konular
Sorun
Optimum tedavi süresi dolmuş ancak hala tedavi edilmesi gereken doku kalmıştır.
Tavsiye
Geçen süreye bakmaksızın, tedavi edilmesi gereken kalan tüm dokuları tedavi etmeye devam edin. Optimal tedavi süresi dışında tedavi edilen tüm lezyonlar işaretlenmeli ve yeniden büyüme veya yanıt alınamaması durumunda derhal yeniden tedavi için dikkatle takip edilmelidir. Özellikle çok geniş lezyonları olan hastalarda veya işlem intraoperatif olarak
yapıldığında bleomisin uygulamasının ne zaman yapılacağının planlanması tavsiye edilir.
İlaç intratümöral olarak uygulanırken, enjekte olunan tümör volümü mümkün olduğunca çabuk tedavi edilmelidir. Tümör büyükse ve enjeksiyon 2 dakikadan fazla sürüyorsa (19), enjekte edilen kısımda pulsları verin ve bundan sonra diğer kısımları enjekte etmeye ve pulslamaya devam edin.
Daha fazla bilgi için lütfen İlacın Kullanım Şekli bölümüne bakınız.
Sorun
Tümör oldukça kalın ve en derin kısımların tedavisi mümkün değil.
Tavsiye
Elektrik alanı, elektrotların iğneleri veya plakaları arasındaki bölgenin dışında çok hızlı bir şekilde kaybolur. Bu nedenle, daha derin kısımları da dahil olmak üzere tüm tümör volümünü tedavi ederken özel önlemler alınmalıdır. Nüks riskini azaltmak için tümörün tamamını, özellikle de yatağını kaplamak çok önemlidir. Yüzey elektrotları kullanıldığında, tedavi derinliği maksimum 3 mm civarındadır. Daha derinlere yayılan tümörlerde, elektrik alanının daha derin dokulara yeterli erişimini sağlamak için her zaman iğne elektrotlar kullanılmalıdır (79). Tümörün kalınlığı iğnelerin uzunluğundan daha fazlaysa, daha önce açıklandığı gibi EKT’den önce debulking ile devam edin.
Sorun
Yuvarlak veya pediküllü lezyonlarda iğne elektrotlarının uygunsuz şekilde kullanılması.
Zararlı Etkileri Azaltma Prosedürü
Aşırı tedaviden dikkatle kaçınarak tümörün tamamının tedavi edilmesini sağlamak son derece önemlidir.
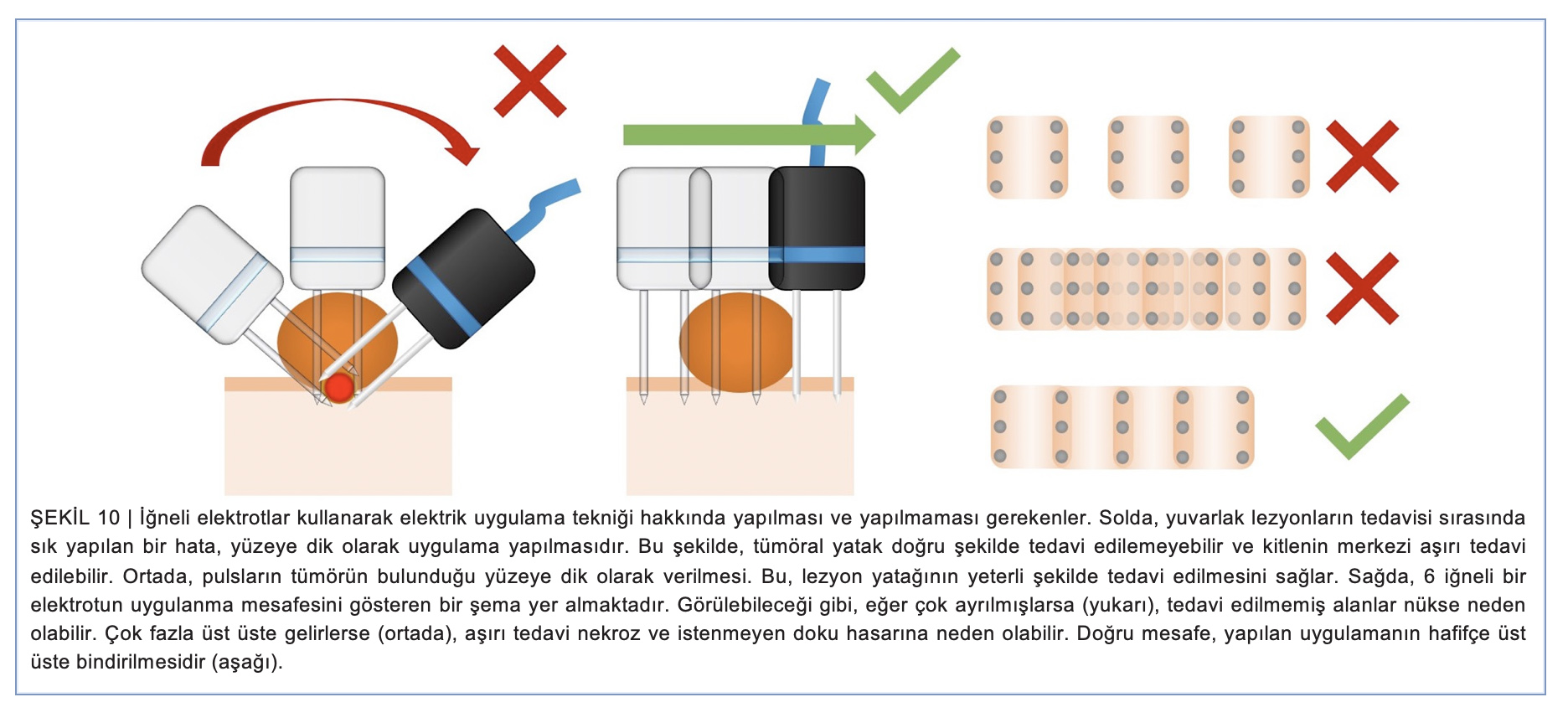
Lezyonun tabanının elektrik alanıyla kaplanması son derece önemlidir. Yuvarlak veya pediküllü lezyonlarda sık yapılan bir hata, iğneli elektrodu tümör yüzeyine dik olarak yerleştirmektir. Bu yaklaşım tümörün merkezini aşırı tedavi ederek geri dönüşümsüz elektroporasyona neden olur ve tümör yatağını kapsamaz. Doğru olan yöntem, iğneli elektrotun tümörün yerleştiği yüzeye dik olarak uygulamaktır. Elektrotun yerleştirilmesinde hafif bir üst üste binme olması faydalı olacaktır ve elektrotun yerleştirilmesinde büyük boşluklardan veya çok fazla üst üste binmeden kaçınılmalıdır (bkz. Şekil 10).
Sorun
Tümör bir dişin etrafını sarmış.
Tavsiye
İğneler arasında dişin bulunması elektriğin yayıldığı alanı ciddi şekilde etkileyebilir. Tümör iğnelerin arasına sığarsa, aralarındaki mesafeyi arttırmadan tedavi edilebilir. Ancak, hastalığın ilerlemesi muhtemelen dişin gevşemesine yol açacağından (daha sonra zaten çekilmesi gerekecektir), dişin çekilmesi ve bölgenin doğru şekilde tedavi edilmesi önerilir.
Sorun
Elektrotlara yakın metalik implantlar veya cerrahi aletler elektriği iletebilir ve kısa devreye neden olarak cihaza zarar verebilir.
Zararlı Etkileri Azaltma Prosedürü
İğnenin herhangi bir metalik implanta veya cerrahi alete temas edecek şekilde veya çok yakınından sokulmaması için özellikle dikkat edilmelidir.
Sorun
Tedavi edilen bölgede kan bulunması iletkenliği artırabilir ve bir ark oluşturabilir veya elektrik alanını saptırarak tümörün eksik/yanlış tedavi edilmesine neden olabilir.
Tavsiye
İşlem sırasında yeterli hemostaz gereklidir.
Sorun
EKT’de bleomisin, sisplatin veya kalsiyum dışındaki ilaçların kullanılması.
Tavsiye
EKT için sadece etkinliği kanıtlanmış kemoterapötik ilaçlar olan bleomisin, sisplatin ve kalsiyumu İlacın Kullanış Şekli bölümünde önerilen reçetelere göre kullanın. Klasik kemoterapide belirli kanserler için etkili olan ilaçlar vardır, ancak EKT için uygun ilacın seçimi histolojik tipe bağlı değildir. Yaygın şekilde kullanılan kemoterapi ilaçlarının çoğu, elektrik pulsları ile test edilmiş ve çok az fayda sağlamış ya da hiç fayda sağlamamıştır (80) çünkü bu ilaçlar, herhangi bir hücre permeabilizasyonu olmasa bile hücrelere kısıtlama olmaksızın zaten nüfuz etmektedir.
Cihazla İlgili Konular
Sorun
Elektroporatör düzgün çalışmıyor.
Tavsiye
Cihazların düzgün çalıştığından emin olmak için hastayı uyutmadan önce her zaman havaya bir puls verin. Sorun devam ederse, cihazı kapatıp tekrar açmayı deneyin, elektrotun ve pedalın cihaza doğru bağlanıp bağlanmadığını kontrol edin ve ardından bu testi tekrarlayın. Sorun devam ederse cihazın üreticisiyle iletişime geçin.
Sorun
Elektrik güç kaynağının bozulması, hemen hemen her ortamda meydana gelebilecek öngörülemeyen bir olaydır. Tıbbi cihazların çoğunda çalışmaya devam etmelerini sağlayan dahili bir batarya bulunur. Elektroporasyon cihazlarında genellikle pil bulunmaz ve bu nedenle elektrik güç kaynağı arızası sırasında çalışmaya devam edemezler.
Tavsiye
750W’lık düzenli bir kesintisiz güç kaynağı (UPS), cihazlarınızın elektrik tüketimine bağlı olarak 4 veya 5 tedavi seansını tamamlamak için yeterli güç sağlayabilir.
Sorun
Yanıt elde etmek için birçok tedavi seansı gerekir ve/veya iğnelerin keskinliğini kaybetmesi nedeniyle tedavi güçleşebilir.
Tavsiye
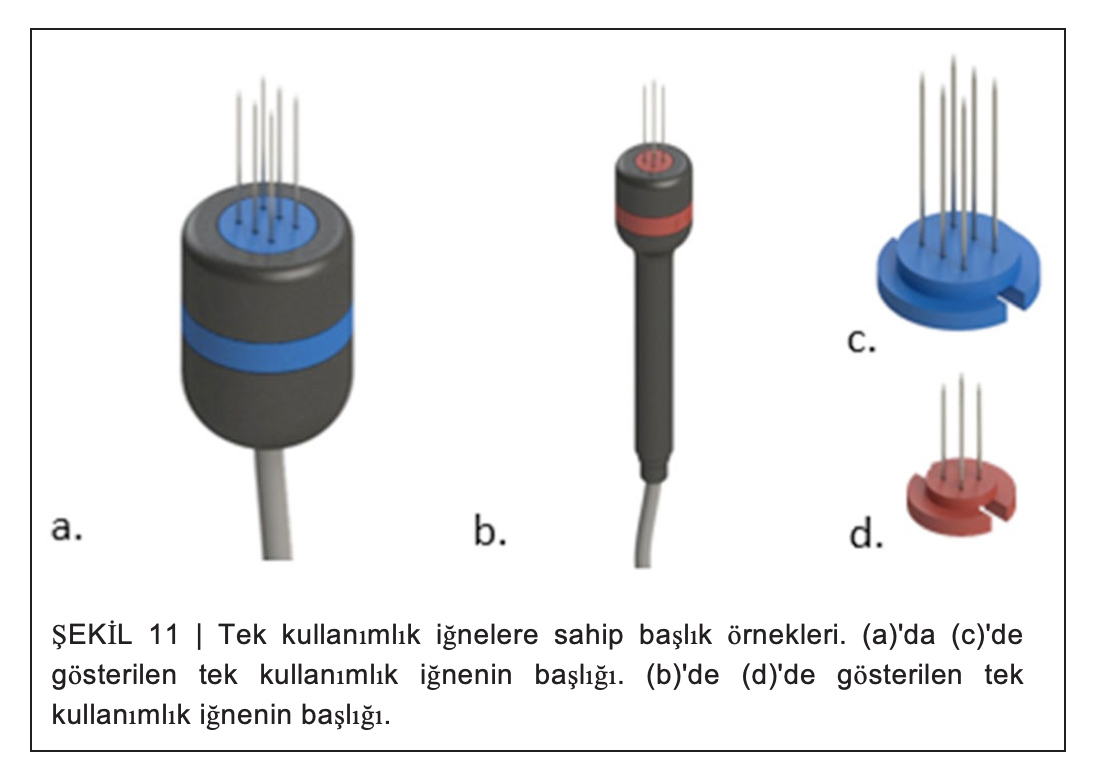
İnsan tıbbında, tek kullanımlık elektrotlar tedavinin uygulanabilmesi için tek seçenektir, ancak veterinerlik tıbbında tek kullanımlık olmayan elektrotların kullanılması hala mümkündür. İğne elektrotları tek bir EKT seansından sonra bile ciddi şekilde etkilenebilir. İğnelerin yüzeyinin oksidasyonu, elektrik alanlarının dağılımını büyük ölçüde etkilendiğinden iğnelerin bazı kısımlarını izole edebilir ve böylece tedavi etkinliğini azaltabilir. Bu oksidasyon gözle görülemeyebilir. Mümkünse tek kullanımlık elektrotlar kullanın (bkz. Şekil 11). Eğer mevcut değillerse, tedaviden önce iğneler zımparalanarak elektrotların bakımı yapılmalıdır. Bu, oksidasyonu giderecek ve elektrik iletimini daha iyi hale getirecektir.
Elektrotlarınızı iyi çalışır durumda tutun, düzenli aralıklarla kontrol edin ve aşınma belirtileri göstermeleri halinde yenilerini alın.
İğnelerin keskinliği de etkilenebilir ve bu iğnelerin daha sonra kullanılması dokuda istenmeyen travmalara yol açabilir. Zaten kullanılmış iğneler de doku içinde kayma eğilimi gösterebilir, birbirlerinden uzaklaşabilir (yetersiz elektrik alanı oluşturabilir) veya birbirlerine doğru eğilebilir (ark veya kısa devre oluşturabilir). İğneler bükülmüşse, dokuya yerleştirmeden önce bükülmeyi düzeltin.
Sorun
Elektroporatör pulsları göndermeye çalışırken uyarı veriyor.
Tavsiye
Bazı tümörler çok yüksek elektrik iletkenliği gösterir, bu da yeterince elektrik alanı sağlamak için çok yüksek elektrik akımlarına ihtiyaç duyulduğu anlamına gelir. Elektroporatörler bu tür yüksek akımları sağlayamayabilir. Kullandığınız cihaz elektrik alanının doğru şekilde sağlanamadığı konusunda uyarı veriyorsa, iğneleri yarıya kadar çıkarın ve pulsları verin. Lezyonun en derin kısmının tedavi edilmeyeceğini ve yüzeysel kısım (tedavi edilen volüm) yanıt verir vermez yeni bir seans planlanması gerektiğini unutmayın. Nekroza neden olabileceğinden ve/veya tedavi etkinliğini ciddi şekilde azaltabileceğinden tedavi parametrelerini modifiye etmekten kaçının.
TARTIŞMA: VETERINER HEKIMLIK ALANINDA EKT KULLANIMI
EKT, veteriner hekimlikte köklü bir uygulamadır. Yüksek etkisi, yan etkilerinin azlığı, diğer tedavi yöntemlerinin başarısız olduğu veya zahmetli olduğu durumlarda yeterli tedavi sağlaması nedeniyle oldukça hızlı bir şekilde kabul görmüştür. Günümüzde EKT düzenli olarak kediler, köpekler ve atlarda kullanılırken, aralarında gelincikler (81), filler, balıklar, kaplumbağalar (82, 83), kirpiler (84), yılanlar (85), kuşlar (86, 87) ve domuzların (88) da bulunduğu çeşitli türlerdeki hastalar da başarıyla tedavi edilmiştir.
İnsan tıbbında EKT çok değerli bir araçtır. Palyatif bir tedavi olarak başlamış ve 2006 yılında ESOPE çalışması (5) ve tıbbi amaçlı elektroporatör olan Cliniporator’un (Igea, Carpi, İtalya) onaylanmasından sonra rutin kullanıma girmiştir. Ana endikasyonları, diğer tedavi yöntemlerine uygun olmayan her histolojideki kutanöz ve subkutanöz tümörlerdir. Son zamanlarda, hastanın isteği üzerine ilk tedavi seçeneği olarak veya internal, derin yerleşimli tümörlerin tedavisi için de uygulanabilmektedir (50). Amerika Birleşik Devletleri ve dünyanın geri kalanı diğer jeneratörlerin geliştirilmesini yakından takip etmiştir. Latin Amerika’da kullanımı, 2020 yılında başka bir tıbbi amaçlı elektroporatör olan OncoPore’un (BIOTEX SRL, Buenos Aires, Arjantin) onaylanmasının ardından Arjantin’de başlamıştır. Gehl ve arkadaşları tarafından yayınlanan EKT için Güncellenmiş Standart Kullanım Prosedürlerinde belirlenen endikasyonların yanı sıra, EKT uygulamalarını karaciğer (12), beyin (89), pankreas (12) ve kemikler (12) gibi diğer organlara genişletmek için yoğun araştırmalar devam etmektedir. Endoskopik elektrot EndoVe, kolorektal kanser (90) ve özofagus (91) tedavisi için geliştirilmiştir. EKT günümüzde onkologlar için son derece değerli bir araçtır. Tek başına veya diğer tedavilerle birlikte kullanılabilir ve diğer tedavilerin başarısız olduğu veya uygulanabilir olmadığı durumlarda yeni bir tedavi seçeneği sunabilmektedir (30).
Yazarların kişisel deneyimleri, 10 yılı aşkın bir süredir çeşitli hayvan türlerinde tedavi edilen 4.000’den fazla vakayı kapsamaktadır. Bu deneyim aynı zamanda klinik ortamda insan hastaların tedavisini de içermekte olup, tedavilerin arasındaki
önemli farklılıkların bilincinde olmamızı sağlamaktadır. Ayrıca EKT üzerine Latin Amerika seminerlerinin düzenlenmesine, Latin Amerika ve İspanya’dan 150’den fazla veteriner hekime 9 kurs verilmesine ve sorularını yanıtlamak için farklı çevrimiçi platformlar aracılığıyla birçok kullanıcıya hizmet vermesine de dayanmaktadır (https://vetoncologia.com/ ect).This guide provides updated practical and useful information to the veterinarians.
Bu çalışmada, veteriner hekimliği kapsamındaki geniş hasta yelpazesinin tedavisinde göz önünde bulundurulması gereken önemli hususlar hakkında ayrıntılı bilgiler sunulmuştur.
VERİ ERİŞİM BEYANI
Bu makalede yer alan sonuçları destekleyen işlenmemiş veriler, herhangi bir çekince olmaksızın yazarlar tarafından temin edilecektir.
ETİK BEYAN
Consejo Profesional de Médicos Veterinarios’un (Arjantin) tüm yönetmeliklerine uyulmuştur. Bu çalışma, Arjantin Buenos Aires Üniversitesi Veteriner Bilimleri Fakültesi IACUC tarafından onaylanmıştır. Protokol Numarası: 2018/31.
Hayvan sahiplerinden hayvanlarının bu çalışmaya katılımı için bilgilendirilmiş onam alınmıştır.
KATKIDA BULUNAN YAZARLAR
Tüm yazarlar makalenin hazırlanması, yazılması ve düzeltilmesine eşit derecede katkıda bulunmuş ve sunulan versiyonu onaylamıştır.
TEŞEKKÜRLER
Yazarlar, sahipli hayvanlar için EKT’nin araştırılması, yayılması ve öğretilmesinde görev alan tüm kişilere teşekkür etmektedir. İlgili tüm kişileri içeren kapsamlı bir liste yapmak mümkün değildir. Son olarak, Dr. Guillermo Marshall’a EKT’nin Arjantin’de insan ve veteriner tıbbında tanıtılması için gösterdiği sürekli çabalardan dolayı teşekkür ederiz.
EK BİLGİLER
Bu makale için Ek Bilgiler çevrimiçi olarak şu adreste bulunabilir: https://www.frontiersin.org/articles/10.3389/fvets. 2022.868989/full#supplementary-material
KAYNAKÇA
- Mir LM, Devauchelle P, Quintin-Colonna F, Delisle F, Doliger S, Fradelizi D, et al. First clinical trial of cat soft-tissue sarcomas treatment by Br J Cancer. (1997) 76:1617– 22. doi: 10.1038/bjc.1997.606
- Belehradek M, Domenge C, Luboinski B, Orlowski S, Belehradek J, Mir Electrochemotherapy, a new antitumor treatment. First clinical phase I-II trial. Cancer. (1993) 72:3694– 700. doi: 10.1002/1097-0142(19931215)72:12<3694::aid-cncr2820721222>3.0. co;2-2
- Mir LM, Belehradek M, Domenge C, Orlowski S, Poddevin B, Belehradek J Jr, et al. [Electrochemotherapy, a new antitumor treatment: first clinical trial]. C R Acad Sci III. (1991) 313:613–8.
- Mir LM, Gehl J, Sersa G, Collins CG, Garbay J-R, Billard V, et Standard operating procedures of the electrochemotherapy: instructions for the use of bleomycin or cisplatin administered either systemically or locally and electric pulses delivered by the CliniporatorTM by means of invasive or non-invasive electrodes. Eur J Cancer Suppl. (2006) 4:14– 25. doi: 10.1016/j.ejcsup.2006.08.003
- Marty M, Sersa G, Garbay JR, Gehl J, Collins CG, Snoj M, et al. Electrochemotherapy – An easy, highly effective and safe treatment of cutaneous and subcutaneous metastases: results of ESOPE (European Standard Operating Procedures of Electrochemotherapy) Eur J Cancer Suppl. (2006) 4:3–13. doi: 10.1016/j.ejcsup.2006.08.002
- Benazzo M, Bertino G, Groselj Electrochemotherapy of head and neck cancer. Handbook Electroporation. (2017) 1903– 15. doi: 10.1007/978-3-319-32886-7_102
- Gargiulo M, Serra Mestre JM, Cortese A, Murphy DC, Parascandolo S, Razzano Long term effectiveness of electrochemotherapy for the treatment of lower lip squamous cell carcinoma. J Craniomaxillofac Surg. (2018) 46:1968–74. doi: 10.1016/j.jcms.2018.08.013
- Maglietti F, Tellado M, Olaiz N, Michinski S, Marshall G. Minimally invasive electrochemotherapy procedure for treating nasal duct tumors in dogs using a single needle Radiol Oncol. (2017) 51:422– 30. doi: 10.1515/raon-2017-0043
- Tellado MN, Maglietti FH, Michinski SD, Marshall GR, Signori E. Electrochemotherapy in treatment of canine oral malignant melanoma and factors influencing treatment outcome. Radiol (2020) 54:68– 78. doi: 10.2478/raon-2020-0014
- Cemazar M, Tamzali Y, Sersa G, Tozon N, Mir LM, Miklavcic D, et al. Electrochemotherapy in veterinary J Vet Intern Med. (2008) 22:826– 31. doi: 10.1111/j.1939-1676.2008.0117.x
- Tamzali Y, Borde L, Rols MP, Golzio M, Lyazrhi F, Teissie J. Successful treatment of equine sarcoids with cisplatin electrochemotherapy: a retrospective study of 48 Equine Vet J. (2012) 44:214– 20. doi: 10.1111/j.2042-3306.2011.00425.x
- Probst U, Fuhrmann I, Beyer L, Wiggermann Electrochemotherapy as a new modality in interventional oncology: a review. Technol Cancer Res Treat. (2018) 17:1533033818785329. doi: 10.1177/153303381878 5329
- Mir LM. Bases and rationale of the electrochemotherapy. In: 11th Mediterranean Conference on Medical and Biomedical Engineering and Computing. Ljubljana (2007). p.
- Sersa G, Miklavcic D. Electrochemotherapy of Tumours. J Vis (2008) 22:1038. doi: 10.3791/1038
- Mir LM, Orlowski S. The basis of electrochemotherapy. Electrochemotherapy Electrogenetherapy Transdermal Drug Deliv. (2000) 37:99–117. doi: 1385/1-59259-080-2:99
- Spugnini EP, Baldi Electrochemotherapy in veterinary oncology: from rescue to first line therapy. Methods Mol Biol. (2014) 1121:247– 56. doi: 10.1007/978-1-4614-9632-8_22
- Gehl J, Serša Electrochemotherapy and its clinical applications. Handbook Electroporation. (2017) 1771–86. doi: 10.1007/978-3-319-32886-7_91
- Tozon N, Pavlin D, Sersa G, Dolinsek T, Cemazar M. Electrochemotherapy with intravenous bleomycin injection: an observational study in superficial squamous cell carcinoma in J Feline Med Surg. (2014) 16:291– 9. doi: 10.1177/1098612X13507071
- Tozon N, Kramaric P, Kos Kadunc V, Sersa G, Cemazar M. Electrochemotherapy as a single or adjuvant treatment to surgery of cutaneous sarcoid tumours in horses: a 31-case retrospective study. Vet Rec. (2016) 179:627. doi: 1136/vr.103867
- Gehl J, Geertsen PF. Palliation of haemorrhaging and ulcerated cutaneous tumours using electrochemotherapy. Eur J Cancer (2006) 4:35– 7. doi:10.1016/j.ejcsup.2006.07.007
- Gehl J, Skovsgaard T, Mir LM. Vascular reactions to in vivo electroporation: characterization and consequences for drug and gene delivery. Biochim Biophys (2002) 1569:51–8. doi:10.1016/S0304-4165(01)00233-1
- Calvet CY, Mir LM. The promising alliance of anti-cancer electrochemotherapy with immunotherapy. Cancer Metastasis Rev. (2016) 35:165–77. doi: 1007/s10555-016-9615-3
- Calvet CY, Famin D, André FM, Mir LM. Electrochemotherapy with bleomycin induces hallmarks of immunogenic cell death in murine colon cancer Oncoimmunology. (2014)3:e28131. doi: 10.4161/onci.28131
- Maglietti F, Tellado M, De Robertis M, Michinski S, Fernández J, Signori E, et al. Electroporation as the immunotherapy strategy for cancer in veterinary medicine: State of the art in Latin America. (2020) 8:537. doi: 10.3390/vaccines8030537
- Tellado M, Maglietti F, Impellizeri J. Electrochemotherapy as a multi- modality component of cancer treatment: combinations with surgery, cryosurgery, radiation therapy, and chemotherapy. In: Impellizeri JA, editor. Electroporation in Veterinary Oncology Practice. Cham: Springer (2021). p. 205–16.
- Tozon N, Milevoj N, Impellizeri J. Electrochemotherapy in veterinary oncology. In: Impellizeri JA, editor. Electroporation in Veterinary Oncology Practice. Cham: Springer (2021). p.63–112.
- Hodson Precision medicine. Nature. (2016) 537:S49. doi: 10.1038/537S49a
- Bonadies A, Bertozzi E, Cristiani R, Govoni FA, Migliano E. Electrochemotherapy in skin malignancies of head and neck cancer patients: clinical efficacy and aesthetic benefits. Acta Derm Venereol. (2019) 99:1246–52. doi: 2340/00015555-3341
- Sersa G, Teissie J, Cemazar M, Signori E, Kamensek U, Marshall G, et al. Electrochemotherapy of tumors as in situ vaccination boosted by immunogene electrotransfer. Cancer Immunol Immunother. (2015) 64:1315– 27. doi: 1007/s00262-015-1724-2
- Campana LG, Edhemovic I, Soden D, Perrone AM, Scarpa M, Campanacci L, et al. Electrochemotherapy – Emerging applications technical advances, new indications, combined approaches, and multi-institutional collaboration. Eur J Surg (2019) 45:92–102. doi: 10.1016/j.ejso.2018.11.023
- Lowe RJ. Benefits and side-effects of electrochemotherapy in veterinary patients. 1st World Congress on Electroporation and Pulsed Electric Fields in Biology, Medicine and Food & Environmental Technologies. Singapore: Springer (2016). p. 437–40.
- Edhemovic I, Brecelj E, Gasljevic G, Marolt Music M, Gorjup V, Mali B, et al. Intraoperative electrochemotherapy of colorectal liver metastases. J Surg Oncol. (2014) 110:320–7. doi:1002/jso.23625
- Mali B, Miklavcic D, Campana LG, Cemazar M, Sersa G, Snoj M, et al. Tumor size and effectiveness of electrochemotherapy. Radiol Oncol. (2013) 47:32–41. doi: 2478/raon-2013-0002
- Whelan MC, Larkin JO, Collins CG, Cashman J, Breathnach O, Soden DM, et al. Effective treatment of an extensive recurrent breast cancer which was refractory to multimodal therapy by multiple applications of Eur J Cancer Suppl. (2006) 4:32–4. doi: 10.1016/j.ejcsup.2006.07.006
- Campana LG, Testori A, Mozzillo N, Rossi CR. Treatment of metastatic melanoma with J Surg Oncol. (2014) 109:301– 7. doi: 10.1002/jso.23512
- Campana LG, Valpione S, Mocellin S, Sundararajan R, Granziera E, Sartore L, et al. Electrochemotherapy for disseminated superficial metastases from malignant Br J Surg.(2012) 99:821–30. doi: 10.1002/bjs.8749
- Lowe R, Gavazza A, Impellizeri JA, Soden DM, Lubas G. The treatment of canine mast cell tumours with electrochemotherapy with or without surgical excision. Vet Comp (2017) 15:775–84. doi: 10.1111/vco.12217
- Cemazar M, Sersa Recent advances in electrochemotherapy. Bioelectricity.
(2019) 1:204–13. doi: 10.1089/bioe.2019.0028
- Miklavcic D, Pucihar G, Pavlovec M, Ribaric S, Mali M, Macek- Lebar A, et The effect of high frequency electric pulses on muscle contractions and antitumor efficiency in vivo for a potential use in clinical electrochemotherapy. Bioelectrochemistry. (2005) 65:121–8. doi: 10.1016/j.bioelechem.2004.07.004
- Pucihar G, Mir LM, Miklavcic D. The effect of pulse repetition frequency on the uptake into electropermeabilized cells in vitro with possible applications in electrochemotherapy. (2002) 57:167– 72. doi: 10.1016/S1567-5394(02)00116-0
- Spugnini EP, Baldi A. Electrochemotherapy in veterinary oncology: state- of-the-art and perspectives. Vet Clin North Am Small Anim Pract. (2019) 49:967–79. doi:1016/j.cvsm.2019.04.006
- Potocˇnik T, Miklavcˇicˇ D, Macˇek Lebar A. Gene transfer by electroporation with high frequency bipolar pulses in vitro. (2021) 140:107803. doi:10.1016/j.bioelechem.2021.107803
- Gehl J, Sersa G, Matthiessen LW, Muir T, Soden D, Occhini A, et Updated standard operating procedures for electrochemotherapy of cutaneous tumours and skin metastases. Acta Oncol. (2018) 57:874– 82. doi: 10.1080/0284186X.2018.1454602
- 32. Simcˇicˇ
P, Lowe R, Granziera V, Pierini A, Torrigiani F, Lubas G.
- Tozon N, Lampreht Tratar U, Znidar K, Sersa G, Teissie J, Cemazar M.
Electrochemotherapy in treatment of canine oral non-tonsillar squamous cell carcinoma. A case series report. Vet Comp Oncol. (2020) 18:428– 32. doi: 10.1111/vco.12530
- Spugnini EP, Renaud SM, Buglioni S, Carocci F, Dragonetti E, Murace R, et al. Electrochemotherapy with cisplatin enhances local control after surgical ablation of fibrosarcoma in cats: an approach to improve the therapeutic index of highly toxic chemotherapy drugs. J Transl Med. (2011) 9:152. doi: 1186/1479-5876-9-152
- Spugnini EP, Azzarito T, Fais S, Fanciulli M, Baldi A. Electrochemotherapy as first line cancer treatment: experiences from veterinary medicine in developing novel protocols. Curr Cancer Drug (2015) 16:43– 52. doi: 10.2174/156800961601151218155340
- Cutrera J, King G, Jones P, Kicenuik K, Gumpel E, Xia X, et al. Safe and effective treatment of spontaneous neoplasms with interleukin 12 electro-chemo-gene therapy. J Cell Mol Med. (2015) 19:664–75. doi: 1111/jcmm.12382
- Papich MG. Papich Handbook of Veterinary Drugs – E-Book. Amsterdam: Elsevier Health Sciences (2020). p.
- Rols MP, Tamzali Y, Teissié Electrochemotherapy of horses. A preliminary clinical report. Bioelectrochemistry. (2002) 55:101– 5. doi: 10.1016/S1567-5394(01)00156-6
- Milevoj N, Tozon N, Licen S, Lampreht Tratar U, Sersa G, Cemazar M. Health-related quality of life in dogs treated with electrochemotherapy and/or interleukin-12 gene Vet Med Sci. (2020) 6:290– 8. doi: 10.1002/vms3.232
Operating procedures of the electrochemotherapy for treatment of tumor in dogs and cats. J Vis Exp. (2016). doi: 10.3791/54760
- Gozalo-Marcilla M, Ringer SK. Recovery after general anaesthesia in adult horses: a structured summary of the literature. (2021) 11:1777. doi: 10.3390/ani11061777
- Tozon N, Kodre V, Sersa G, Cemazar M. Effective treatment of perianal tumors in dogs with Anticancer Res. (2005) 25:839–45.
- Martin S, Larson Chemotherapy-handling practices of outpatient and office-based oncology nurses. Oncol Nurs Forum. (2003) 30:575– 81. doi: 10.1188/03.ONF.575-581
- Stefanou A, Siderov Society of Hospital Pharmacists of Australia Committee of Specialty Practice in Oncology. Medical errors dosage nomenclature of bleomycin needs to be standardised to avoid errors. BMJ. (2001) 322:1423–4.
- Vail DM, Thamm DH, Liptak J. Withrow and MacEwen’s Small Animal Clinical Oncology – E-Book. Amsterdam: Elsevier Health Sciences (2019). p.
- Groselj A, Krzan M, Kosjek T, Bosnjak M, Sersa G, Cemazar M. Bleomycin pharmacokinetics of bolus bleomycin dose in elderly cancer patients treated with electrochemotherapy. Cancer Chemother Pharmacol. (2016) 77:939– 47. doi: 1007/s00280-016-3004-z
- Dorr Bleomycin pharmacology: mechanism of action and resistance, and clinical pharmacokinetics. Semin Oncol. (1992) 19:3–8.
- Jerzsele Comparative Veterinary Pharmacokinetics. Readings in Advanced Pharmacokinetics – Theory, Methods and Applications. Vienna: InTech (2012).
- Hezzell MJ, Dennis SG, Humm K, Agee L, Boswood Relationships between heart rate and age, bodyweight and breed in 10,849 dogs. J Small Anim Pract. (2013) 54:318–24. doi:10.1111/jsap.12079
- Groselj A, Bosnjak M, Krzan M, Kosjek T, Bottyán K, Plesnik H, et al. Bleomycin concentration in patients’ plasma and tumors after electrochemotherapy. A study from InspECT Group. (2021) 13:1324. doi: 10.3390/pharmaceutics13091324
- Mir LM, Tounekti O, Orlowski S. Bleomycin: Revival of an old drug. Gen Pharmacol. (1996) 27:745–8. doi: 1016/0306-3623(95)02101-9
- Campana LG, Testori A, Curatolo P, Quaglino P, Mocellin S, Framarini M, et al. Treatment efficacy with electrochemotherapy: a multi-institutional prospective observational study on376 patients with superficial Eur J Surg Oncol. (2016) 42:1914–23. doi: 10.1016/j.ejso.2016.06.399
- Spugnini EP, Vincenzi B, Citro G, Dotsinsky I, Mudrov T, Baldi A. Evaluation of Cisplatin as an electrochemotherapy agent for the treatment of incompletely excised mast cell tumors in dogs. J Vet Intern Med. (2011) 25:407–11. doi: 1111/j.1939-1676.2011.0678.x
- Knapp DW, Richardson RC, DeNicola DB, Long GG, Blevins Cisplatin toxicity in cats. J Vet Intern Med. (1987) 1:29–35. doi: 10.1111/j.1939-1676.1987.tb01983.x
- Sersa G, Miklavcic D, Cemazar M, Rudolf Z, Pucihar G, Snoj M. Electrochemotherapy in treatment of tumours. Eur J Surg Oncol. (2008) 34:232–40. doi: 1016/j.ejso.2007.05.016
- Frandsen SK, Vissing M, Gehl J. A comprehensive review of calcium electroporation—a novel cancer treatment modality. (2020) 12:290. doi: 10.3390/cancers12020290
- Frandsen SK, Gehl J, Tramm T, Thoefner MS. Calcium electroporation of equine Animals. (2020) 10:517. doi: 10.3390/ani10030517
- Bik L, Sangers T, Greveling K, Prens E, Haedersdal M, van Doorn M. Efficacy and tolerability of intralesional bleomycin in dermatology: A systematic review. J Am Acad Dermatol. (2020) 83:888–903. doi: 1016/j.jaad.2020.02.018
- Bronaugh RL, Stewart RF, Congdon ER. Methods for in vitro percutaneous absorption II Animal models for human skin. Toxicol Appl Pharmacol. (1982) 62:481–8. doi:10.1016/0041-008X(82)90149-1
- Cindricˇ H, Kos B, Miklavcˇicˇ D. Electrodes and electric field distribution in clinical practice. In: Impellizeri JA, editor. Electroporation in Veterinary Oncology Practice. Cham:Springer (2021). 21–59.
- Bertino G, Sersa G, De Terlizzi F, Occhini A, Plaschke CC, Groselj A, et European Research on Electrochemotherapy in Head and Neck Cancer (EURECA) project: results of the treatment of skin cancer. Eur J Cancer. (2016) 63:41–52. doi: 10.1016/j.ejca.2016.05.001
- Corovic S, Al Sakere B, Haddad V, Miklavcic D, Mir Importance of contact surface between electrodes and treated tissue in electrochemotherapy. Technol Cancer Res Treat. (2008) 7:393–400. doi: 10.1177/153303460800700507
- Ivorra A, Al-Sakere B, Rubinsky B, Mir Use of conductive gels for electric field homogenization increases the antitumor efficacy of electroporation therapies. Phys Med Biol. (2008) 53:6605–18. doi: 10.1088/0031-9155/53/22/020
- Narita T, Sato R, Motoishi K, Tani K, Naito Y, Hara The interaction between orally administered non-steroidal anti-inflammatory drugs and prednisolone in healthy dogs. J Vet Med Sci.(2007) 69:353–63. doi: 10.1292/jvms.69.353
Eur J Cancer Suppl. (2006) 4:45–51. doi: 10.1016/j.ejcsup.2006. 08.006
- Jaroszeski MJ, Dang V, Pottinger C, Hickey J, Gilbert R, Heller R. Toxicity of anticancer agents mediated by electroporation in vitro. Anticancer Drugs. (2000) 11:201–8. doi:1097/00001813-200003000-00008
- Racnik J, Svara T, Zadravec M, Gombac M, Cemazar M, Sersa G, et al. Electrochemotherapy with bleomycin of different types of cutaneous tumours in a ferret (Mustela putorius furo). Radiol Oncol. (2017) 52:98– 104. doi: 1515/raon-2017-0057
- Donnelly KA, Papich MG, Zirkelbach B, Norton T, Szivek A, Burkhalter B, et al. Plasma bleomycin concentrations during electrochemotherapeutic treatment of fibropapillomas in green turtleschelonia mydas. J Aquat Anim Health. (2019) 31:186–92. doi: 1002/aah.10067
- Brunner CHM, Dutra G, Silva CB, Silveira LMG, de Fátima Monteiro Martins M, Electrochemotherapy for the treatment of fibropapillomas in Chelonia mydas. J Zoo Wildl (2014)45:213–8. doi: 10.1638/2010-0125.1
- Spugnini EP, Lanza A, Sebasti S, Baldi Electrochemotherapy palliation of an oral squamous cell carcinoma in an African hedgehog (Atelerix albiventris). Vet Res Forum. (2018) 9:379–81. doi: 10.30466/vrf.2018.33109
- Lanza A, Baldi A, Spugnini Surgery and electrochemotherapy for the treatment of cutaneous squamous cell carcinoma in a yellow-bellied slider (Trachemys scripta scripta). J Am Vet Med Assoc. (2015) 246:455– 7. doi: 10.2460/javma.246.4.455
- Lanza A, Baldi A, Rossi G, Spugnini EP. Electrochemotherapy for the treatment of an incompletely excised subcutaneous low-grade epithelioid hemangioendothelioma in a budgerigar parakeet (Melopsittacus undulatus). Open Vet (2019) 9:269. doi: 10.4314/ovj.v9i3.13
- Racnik J, Svara T, Zadravec M, Gombac M, Cemazar M, Sersa G, et al. Electrochemotherapy with cisplatin for the treatment of a non-operable cutaneous fibroma in a cockatiel (Nymphicus hollandicus). N Z Vet J. (2019) 67:155–8. doi: 1080/00480169.2018.1564393
- Weissman M, Donnelly LL, Branson K, Glahn A, Nagy D, Havis B, et Electrochemotherapy for a cutaneous squamous cell carcinoma in a Vietnamese pot-bellied Pig (Susscrofa). J Exotic Pet Med. (2020) 34:37– 43. doi: 10.1053/j.jepm.2020.03.013
- Linnert M, Agerholm-Larsen B, Mahmood F, Iversen HK, Gehl J. Treatment of brain tumors: electrochemotherapy. In: Hayat MA, Tumors of the Central Nervous System, Volume 12: Molecular Mechanisms, Children’s Cancer, Treatments, and Radiosurgery. Dordrecht: Springer Netherlands (2014). p. 247–259.
- Hansen HF, Bourke M, Stigaard T, Clover J, Buckley M, O’Riordain M, et al. Electrochemotherapy for colorectal cancer using endoscopic electroporation: a phase 1 clinical study. Endosc Int Open. (2020) 08:E124– 32. doi: 1055/a-1027-6735
- Egeland C, Baeksgaard L, Johannesen HH, Löfgren J, Plaschke CC, Svendsen LB, et al. Endoscopic electrochemotherapy for esophageal cancer: a phase I clinical study. Endosc Int Open. (2018) 6:E727–34. doi: 10.1055/a-05 90-4053
Çıkar Çatışması Beyanı: Yazarlar, araştırmanın potansiyel bir çıkar çatışması olarak yorumlanabilecek herhangi bir ticari veya maddi ilişki olmaksızın yürütüldüğünü beyan etmektedir.
- Milevoj N, Tratar UL, Nemec A, Brožicˇ A, Žnidar K, Serša G,
et al. combination of electrochemotherapy, gene electrotransfer of plasmid encoding canine IL-12 and cytoreductive surgery in the treatment of canine oral malignant melanoma. Res Vet Sci. (2019) 122:40–9. doi: 10.1016/j.rvsc.2018.11.001
- Campana LG, Valpione S, Falci C, Mocellin S, Basso M, Corti L, et al. The activity and safety of electrochemotherapy in persistent chest wall recurrence from breast cancer after mastectomy: a phase-II study. Breast Cancer Res Treat. (2012) 134:1169–78. doi: 1007/s10549-012-2095-4
- Sersa G, Cufer T, Paulin SM, Cemazar M, Snoj M. Electrochemotherapy of chest wall breast cancer recurrence. Cancer Treat Rev. (2012) 38:379– doi: 10.1016/j.ctrv.2011.07.006
- Miklavcic D, Corovic S, Pucihar G, Pavselj Importance of tumour coverage by sufficiently high local electric field for effective electrochemotherapy.
Yayıncının Notu: Bu makalede ifade edilen tüm iddialar yalnızca yazarlara aittir ve bağlı oldukları kuruluşların ya da yayıncının, editörlerin ve hakemlerin görüşlerini temsil etmeyebilir. Bu makalede değerlendirilebilecek herhangi bir ürün veya üreticisi tarafından ileri sürülebilecek herhangi bir iddia, yayıncı tarafından teminat altına alınmamış veya desteklenmemiştir.
Telif Hakkı © 2022 Tellado, Mir ve Maglietti. Bu, Creative Commons Attribution License (CC BY) koşulları altında dağıtılan açık erişimli bir makaledir. Orijinal yazar(lar)a ve telif hakkı sahip(ler)ine atıfta bulunulması ve bu dergideki orijinal yayına atıfta bulunulması koşuluyla, kabul görmüş akademik teamüllere uygun şekilde diğer forumlarda kullanımına, dağıtımına veya çoğaltılmasına izin verilir. Bu şartlara uymayan hiçbir kullanım, dağıtım veya çoğaltmaya izin verilmez.