Onkoloji Bölümü, Brisbane Hayvan Hastanesi, Brisbane, Avustralya
İlgili Kişi
- Morgan, Onkoloji Bölümü, Brisbane Hayvan Hastanesi, 532 Seventeen Mile Rocks Road, Sinnamon Park, Queensland, 4073, Brisbane, Avustralya.
Epostal: elizabeth.morgan1@uqconnect.edu.au
Köpek T hücreli lenfomasının, B hücreli benzerine kıyasla daha önce prognoz bakımından kötü bir gösterge olduğu tespit edilmiştir. Siklofosfamid, doksorubisin, vinkristin ve prednizolon protokolü köpek lenfoması için ilk basamak tedavi olarak yaygın şekilde kabul görmektedir. T hücreli lenfoma için alternatif protokolleri araştıran birkaç çalışma yapılmıştır. Bu çalışmada, T Hücreli lenfomalı 35 köpekte modifiye lomustin, vinkristin, prokarbazin ve prednizolon protokolünün ilk basamak tedavi olarak kullanımı araştırılmıştır. Tüm 35 köpek için ortalama progresyonsuz sağkalım (PFS) süresi 431 gün olup 6 aylık, 1 yıllık, 2 yıllık ve 3 yıllık PFS sırasıyla %69, %54, %29 ve %12’dir. Ortalama sağkalım süresi (MST) 507 gündü. Yirmi dokuz köpekte tam yanıt elde edilmiş ve ortalama PFS süresi 509 gün olmuştur. Otuz köpek protokol esnasında bazı yan etkiler yaşamış ve bunların %73’ü grade 1 veya 2 şeklindeydi. Bu protokol, önceki çalışmalara kıyasla daha yüksek ortalama PFS süresi ve MST göstermiştir bunun yanı sıra köpek T hücreli lenfomasına karşı ilk basamak kemoterapi protokolü olarak kullanılmasını tavsiye etmektedir.
ANAHTAR KELİMELER
köpek, kemoterapi, LOPP, onkoloji, T hücreli lenfoma
1 | GİRİŞ
Lenfoma, risk altındaki her 100.000 köpekte 13 ila 24 arasında değişen yıllık insidans raporlarıyla köpeklerde en sık görülen neoplazmlardan biridir.1 T hücreli lenfoma insidansının %13 ila %39 arasında değiştiği bildirilmiştir.2-10 Birçok çalışmada lenfoma tedavisi araştırılmış olup, T hücreli lenfoma aynı protokolle tedavi edildiğinde B hücreli lenfoma ile karşılaştırıldığında daha kötü bir prognoza sahiptir.4 -6,8,11 T hücreli lenfomalı hastalarda tam yanıt (CR) oranı, ortalama progresyonsuz sağkalım (PFS) süresi ve ortalama sağkalım süresi (MST) birçok çalışmada düşük çıkmıştır.
Siklofosfamid, doksorubisin, vinkristin ve prednizolon (CHOP), modifiye CHOP, mekloretamin, vinkristin, prednizolon ve prokarbazin (MOPP), vinkristin, L-asparaginaz, siklofosfamid, doksorubisin ve prednizolon (VELCAP-L) ve tek ajan protokollerini içeren kemoterapi protokollerini kullanan çalışmalar, T hücreli lenfomalı köpeklerde B hücreli lenfomalı köpeklere kıyasla daha kötü sonuçlar verdiğini ortaya koymuştur. Bu çalışmalarda, T hücreli lenfomalı köpekler için MST 120 ila 237 gün ve ortalama PFS 104 ila 200 gün arasında değişiklik göstermiştir.4-6,8,11
2010 yılında Beaver ve ark.7 tek doz doksorubisin ile tedavi edilen T hücreli lenfomalı köpeklerde genel yanıt oranının %50, B hücreli lenfomalı köpeklerde ise %100 olduğunu tespit etmiştir.
Zandvliet ve ark.12 lenfomalı köpeklerin %55,6’sında ilaç direncinin meydana geldiğini saptamıştır. Kemoterapi direnci, sitotoksik ilaçların ATP-bağlayıcı kaset (ABC) ailesinin taşıyıcı proteinleri tarafından aktif olarak dışarı atılması ile ilişkilendirilmiştir. T hücreli lenfomalı köpeklerin B hücreli lenfomalı köpeklere göre daha yüksek intrinsik ilaç direncine sahip olduğunu ve ilaca dirençli T hücreli lenfomalı köpeklerde ABCG2 mRNA ekspresyonunun arttığını bulmuşlardır. ABCG2, doksorubisine karşı taşıma ve hücresel duyarlılıkta rol oynamaktadır ve insanlarda doksorubisin direnci ile ilişkilendirilmiştir.12 Bu bulgular, T hücreli lenfomalı köpeklerin doksorubisine karşı daha az duyarlı olduğunu ve bu hastalığın tedavisi için doksorubisin bazlı olmayan protokoller uygulanması gerektiğini göstermektedir.
Standart kemoterapi protokollerine alınan yanıtın düşük olması nedeniyle, T hücreli lenfomanın alternatif kemoterapi protokollerine yanıtını araştıran çeşitli çalışmalar yapılmıştır. Araştırılan protokoller arasında L-asparaginaz ve MOPP, vinkristin, L-asparaginaz, siklofosfamid, lomustin, doksorubisin, prednizolon, prokarbazin ve mekloretamin (VELCAP-TSC) ve lomustin, vinkristin, prokarbazin ve prednizolon (LOPP) bulunmaktadır. Bu çalışmalarda 237 ila 323 gün arasında seyreden daha iyi genel MST süreleri bulunmuştur.13-16
T hücreli lenfomanın yaygın olarak kullanılan kemoterapi protokollerine verdiği yanıtın yetersiz olması ve hastalığın yüksek insidansı, bu hastalığın tedavi seçeneklerine yönelik daha fazla
Kısaltmalar: IV, intravenöz; LOPP, lomustin, vinkristin, prokarbazin ve prednizolon; PO, ağızdan (per os).
araştırma yapılmasını zorunlu kılmaktadır. Bu çalışma, ilk basamak tedavi olarak modifiye LOPP protokolü ile tedavi edilen T hücreli lenfomalı bir grup köpeğin sonuçlarını retrospektif olarak araştırmayı amaçlamaktadır. Hipotezimize göre, bu hastalar doksorubisin bazlı protokollerle tedavi edilen B hücreli lenfomalı köpeklerle karşılaştırılabilir sağkalım sürelerine sahiptir.
1 | MATERYAL VE METOD
- | Çalışma grubu
Tek bir onkoloji danışmanlık grubu tarafından T hücreli lenfoma için modifiye LOPP kemoterapisi ile tedavi edilen köpeklere ait vaka materyalleri şu dört özel sağlık merkezinden toplanmıştır: 2008-2010 yılları arasında Queensland Uzman Veteriner Kliniği (Brisbane), 2010-2013 yılları arasında Uzman Veterinerlik Hizmetleri (Brisbane), 2013-2016 yılları arasında Veteriner Onkoloji Uzmanları (Brisbane) ve 2016-2017 yılları arasında Hayvan Hastanesi (Brisbane). Tüm bu sağlık merkezleri aynı şehirde yer almaktaydı.
Çalışmaya dahil edilme kriterleri arasında hastalığın klinik olarak hızlı ilerlemesi, lenfoma tanısı, T hücre immünofenotipi, modifiye LOPP kemoterapi protokolü ile tedavi edilme hedefi ve tedavi öncesi evreleme bulunmaktaydı. Epiteliyotropik lenfomalı köpekler çalışmaya dahil edilmemiştir. Hiçbir köpek daha önce kemoterapi protokolü almamıştır. Tüm hastaların yeterli vaka materyali ve öyküsünün kaydedilmiş olması gerekiyordu. Takip sırasında tüm köpeklerin mortalite bilgileri (canlı ve ölü) mevcuttu ve ölüm tarihi veya ayı mevcut olduğunda kaydedildi. Protokoldeyken remisyondan çıkan veya ilerleyici hastalığı (PD) olan vakalar daha sonra diğer tedavi protokolleriyle kurtarılabilir.
1.2 | Teşhis ve evreleme
İmmünositokimya dahil sitoloji, immünohistokimya dahil histopatoloji, akış sitometrisi veya antijen reseptör yeniden düzenlemeleri için polimeraz zincir reaksiyonu (PARR) temelinde CD3 antijen boyaması ile kesin T hücreli lenfoma tanısı konan köpekler çalışmaya dahil edilmiştir. Örnekler lenf nodu veya nod dışı bölgelerden (karaciğer, dalak, kan veya vücut sıvısı) alınabilir. Klinik evreleme Dünya Sağlık Örgütü’nün köpek lenfoması için beş evreli kriterlerine göre yapılmıştır. Hastalar ayrıca klinisyenin değerlendirmesine göre “a” klinik olarak iyi veya “b” klinik olarak iyi değil şeklinde alt evrelere ayrılmıştır.
Hastaların evrelendirilmesinde kan yayması ile birlikte tam kan sayımı (CBC), çoklu biyokimyasal analizler (MBA), iyonize kalsiyum, idrar tahlili, göğüs radyografileri ve abdominal ultrason kullanılmıştır. Hastalara rutin olarak karaciğer ve dalak aspiratları yapılmamıştır, bu nedenle III. ve IV. evre hastalar arasındaki ayrım
karaciğer ve dalaktaki anormal ultrason bulgularına göre yapılmıştır. Klinisyen ve hasta sahibinin tercihi nedeniyle hastaların hepsine tam evreleme yapılmamış ve hastalara mevcut bilgilere dayanarak birer evre atanmıştır.
1.3 | Tedavi protokolü
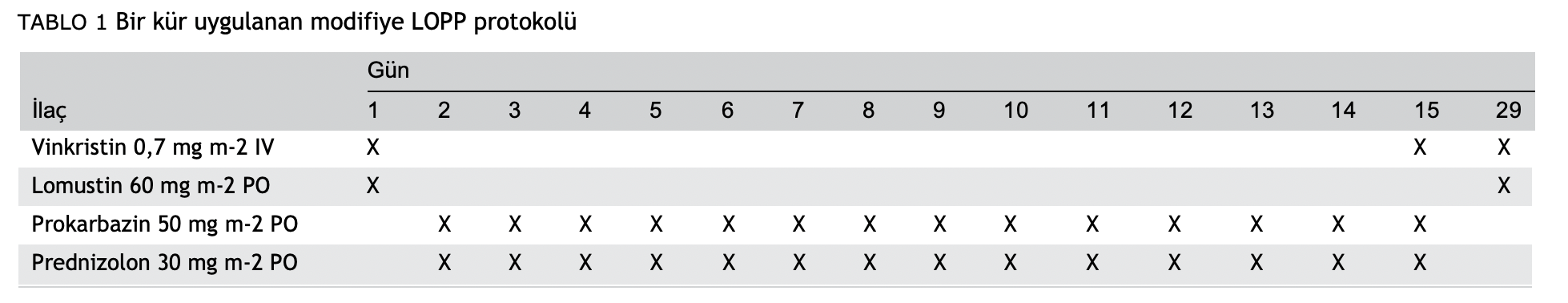
Tüm vakalar Tablo 1’e göre uygulanan LOPP’yi içeren modifiye bir LOPP protokolü ile tedavi edilmiştir. Bir LOPP kürü, 1. günde vinkristin 0,7 mg m-2 intravenöz (IV) ve lomustin 60 mg m-2 ağızdan (PO); 2. günde başlayıp 14 gün boyunca devam eden prokarbazin 50 mg m-2 gün-1 PO ve prednizolon 30 mg m-2 gün-1 PO ve 15. günde vinkristin 0,7 mg m-2 IV’den meydana gelmekteydi. Prednizolon her kürde verildi. Kür her 28 günde bir tekrarlanmış ve protokolün tamamı 23 hafta boyunca 5,5 kürden oluşmuştur.
Tüm hastalarda remisyon durumunu ve kemoterapiye bağlı toksisite bulgularını değerlendirmek için her vinkristin ve lomustin dozundan önce tam kapsamlı fizik muayene, CBC ve kan yayması yapılmıştır. Nötrofiller < 2000 μL-1 veya trombositler < 75 000 μL-1 ise tedavi ertelenmiştir. Ekstranodal tutulumu olan bazı vakalarda aralıklı olarak abdominal ultrasonografi yapıldı. Hepatotoksisiteye işaret edebilecek yüksek karaciğer değerlerini araştırmak için tedavinin başlangıcında ve lomustin tedavisinin her saniyesinden önce (yani siklus 1, 3 ve 5) MBA yapıldı.
Modifiye edilmiş 23 haftalık LOPP protokolünün tamamlanmasından sonra, remisyon durumunu izlemek için 6 haftada bir tekrar kontrol muayenesi yapılması tavsiye edilmiştir. Yapılan kontroller arasında tüm hastalarda lenf düğümlerinin palpe edilmesi de vardı. Hastanın primer prezentasyonuna bağlı olarak CBC, kan yayması, MBA, toraks röntgeni veya batın ultrasonunu gibi ek testler de yapılabilir.
1.4 | Tedaviye alınan yanıt
Tedaviye alınan yanıtlar, periferik nodal lenfoma için Veteriner Onkoloji Grubu (VCOG) değerlendirme kriterleri kullanılarak belirlenmiştir.17 CR, klinik olarak tespit edilebilen tüm hastalığın ortadan kalkması şeklinde tanımlanmıştır. Bu durum hastayı tedavi eden klinisyen tarafından değerlendirilmiş ancak sitoloji veya histopatoloji ile doğrulanmamıştır. Kısmi yanıt (PR) hedef lezyonların boyutunda (yani ortalama toplam en uzun çap) en az %30 azalma, stabil hastalık (SD) %30’dan az azalma ancak boyutta %20’den az artış ve PD ise boyutta %20’den fazla artış olarak kabul edilmiştir.
1.5 | Yan Etkiler
Yan etkilerin (AE) şiddet derecesini belirlemek için VCOG yan etkiler için ortak terminoloji kriterleri (CTCAE) kullanılmıştır.
Miyelosupresyon (nötrofiller ve trombositler), gastrointestinal toksisite (bulantı, kusma ve ishal) ve hepatotoksisite (yüksek alanin aminotransferaz [ALT]) dahil olmak üzere çeşitli AE’lerin saptanması için klinik kayıtlar ve kan sonuçları retrospektif olarak incelenmiştir. AE’ler VCOG-CTCAE’ye göre 1’den 5’e kadar derecelendirilmiştir.
Kronik renal toksisite de protokolün tamamlanmasından sonra kan üre nitrojeni (BUN) ve kreatinin yüksekliği ile değerlendirilmiştir.
1.1 | İstatistiksel analiz
PFS birincil sonlanım noktası olarak kabul edilmiş ve tedavinin başladığı tarihten PD veya herhangi başka bir sebepten ölüm tarihine kadar olacak şekilde hesaplanmıştır. MST, tedavinin başladığı tarihten herhangi bir nedenden ölüm tarihine kadar hesaplanmıştır. Analiz sırasında hala hayatta olan veya takibi yarım kalan köpekler sansürlenmiş ancak hiçbir köpeğin takibi yarım kalmamıştır.
Yapılan analizlerde hastayla ilgili dikkate alınan değişkenler arasında tanının konulduğu yaş (yıl), cinsiyet (erkek vs dişi), ırk (Boxer/Boxer melezleri vs Boxer olmayan), klinik evre (I-IV vs V), tümörün yeri (multisentrik vs diğer), alt tip (a vs b) ve hiperkalsemi olup olmadığı ( var vs yok) yer almıştır. Tedaviyle ilgili değişkenler arasında CR (evet vs hayır), tedavinin ertelenmesi (evet vs hayır) ve doz düşürülmesi (evet vs hayır) yer almıştır. Yaş sürekli, diğer tüm değişkenler kategorik olarak ele alınmıştır.
Ortalama PFS süresi %95 güven aralıkları (CI) ile 35 köpeğin tamamı için ve daha sonra hasta ve tedaviyle ilgili değişkenlere göre hesaplanmıştır. Ortalama PFS süresi yüzdesi %95 GA ile 6, 12, 24 ve 48. aylarda hesaplanmıştır.
Ortalama PFS süresi ile hasta ve tedaviyle ilgili değişkenler arasındaki ilişkileri değerlendirmek için tek değişkenli Cox orantılı tehlike modeli kullanılmıştır. Tek değişkenli analizde P < 0.25 düzeyinde PFS ile ilişkili olan hasta değişkenleri çok değişkenli model ile değerlendirilmiştir. En büyük Wald P-değerlerine sahip
değişkenleri, yalnızca P ≤ 0,10 düzeyinde anlamlı olanlar kalana kadar sırayla çıkarmak için geriye doğru seçim tekniği kullanılmıştır.
Ek araştırma analizleri, kategorik değişkenler için Fisher’in kesinlik testi ve sürekli değişkenler için Wilcoxon işaretli sıralar testi kullanılarak CR’ye ulaşma (evet ve hayır) ile hasta değişkenleri arasındaki ilişkinin değerlendirilmesi şeklinde yapılmıştır.
Verilerin tüm analizi Stata (Sürüm 13.1; Stata- Corp, College Station, Texas) kullanılarak yapılmıştır.
3 | SONUÇLAR
3.1.| Çalışma grubu
Otuz beş köpek çalışmaya dahil edilme kriterlerini karşılamış ve çalışmaya dahil edilmiştir. Yirmi üç köpeğe histopatoloji ve immünohistokimya, 11 köpeğe sitoloji ve immünositokimya, bir köpeğe ise sitoloji ve PARR kullanılarak tanı konulmuştur. Modifiye LOPP protokolüne başlayan 35 köpekten 20’si 5,5 kürün tamamını tamamlamıştır. Dokuz köpek (%26) çalışma tamamlandığında hayattaydı ve sansürlendi. Sansürlenen hastaların ortalama takip süresi 710 gün, sansürlenmeyen hastaların ortalama takip süresi ise 238 gündü.
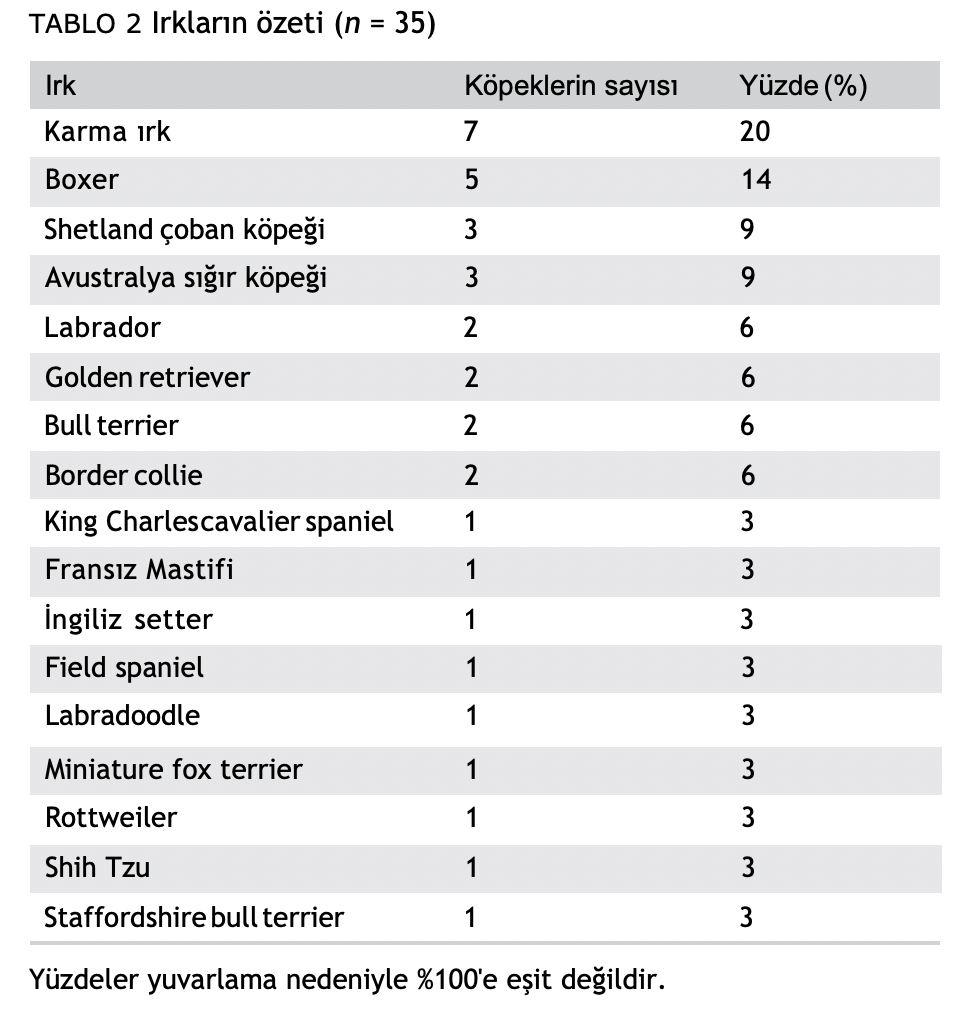
Ortalama yaş 6,5 ( yaş aralığı 2-14,4) olup 17 farklı köpek ırkı bulunmaktaydı (Tablo 2). Melez köpeklerden ikisi Boxer meleziydi ve bunlar veri analizinde ırk (Boxer/Boxer melezleri vs Non-Boxer) analiz edilirken safkan Boxer’larla birlikte değerlendirildi. Klinik özellikler Tablo 3’te sunulmuştur.
3.2 | Tedaviye alınan yanıt
Yirmi köpek (%57) protokolü tamamlamıştır. Protokolü tamamlamama nedenleri PD (sekiz köpek), AE’ler (kemik iliği [3] ve
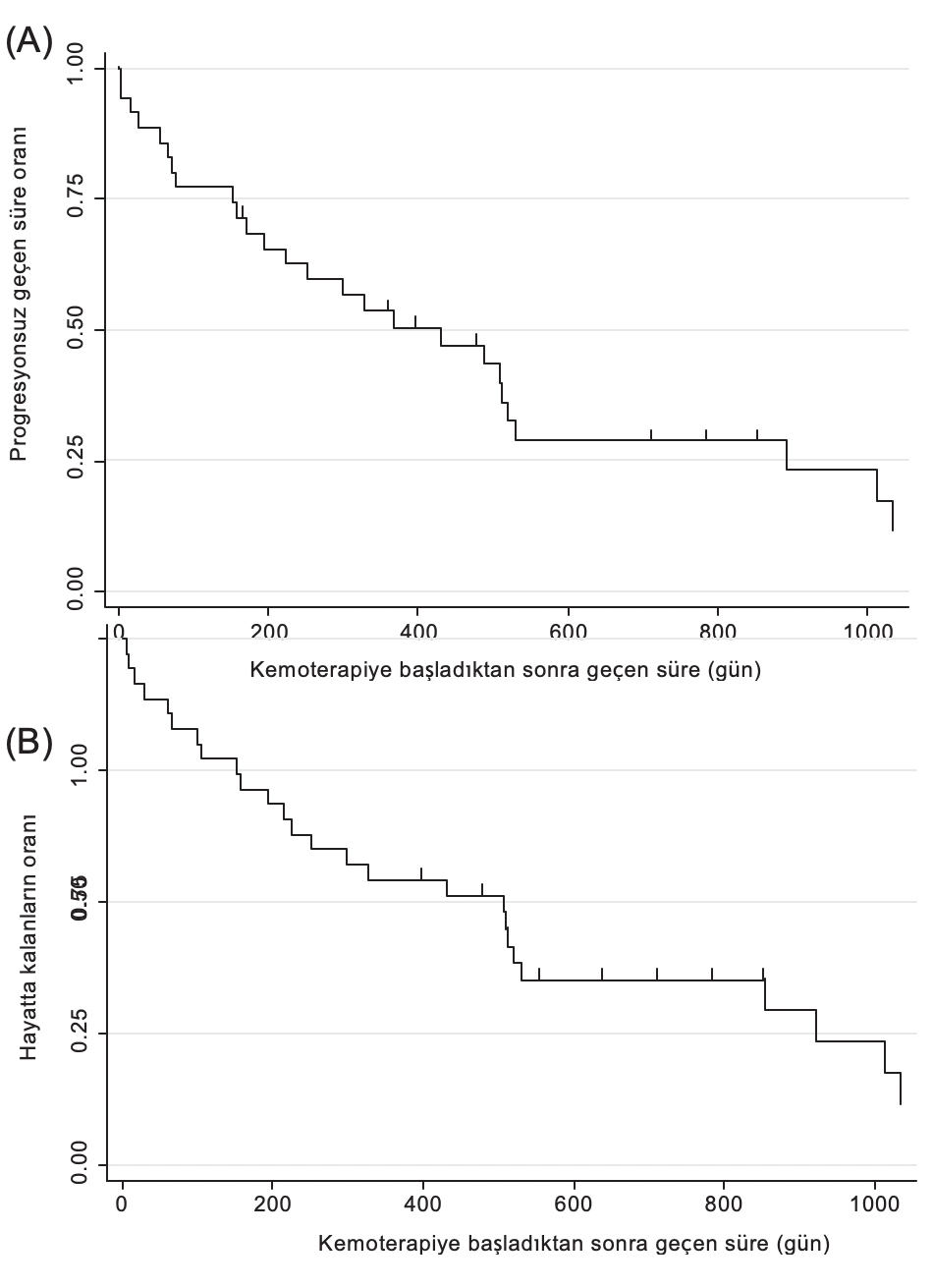
ŞEKİL 1 A, Kaplan-Meier progresyonsuz sağkalım eğrisi (progresyon veya tüm nedenlere bağlı mortalite). B, Kaplan-Meier sağkalım eğrisi (tüm nedenlere bağlı mortalite)
gastrointestinal [1]), maddi durum (2) ve bilinmeyen (1) şeklindeydi. Yirmi dokuz köpekte (%83) CR elde edilmiş ve dört köpekte (%11) PR elde edilerek genel yanıt oranı %94 olmuştur. İki köpekte (%6) PD görülmüş ve hiçbir köpekte SD görülmemiştir.
Tüm 35 köpek için ortalama PFS süresi 431 gündü (%95 GA 194-519 gün, aralık 1-2714 gün, Şekil 1) ve 6 aylık, 1 yıllık, 2 yıllık ve 3 yıllık PFS %69, %54, %29 ve %12 idi. MST 507 gün (%95 GA: 214-854 gün, aralık 6-2714 gün, Şekil 1B) ve 6 aylık, 1 yıllık, 2 yıllık ve 3 yıllık sağkalım sırasıyla %71, %54, %35 ve %12’dir.
LOPP’yi tamamlamayan 15 hastadan 4’ü tedavi kesildiğinde remisyondaydı ve uzun süre (en az 923 gün) hayatta kaldı. Dört hasta kurtarma protokolleri almıştır. Bir köpek L-asparaginaz, vinkristin ve metronomik siklofosfamid ile dönüşümlü olarak vinkristin ve sitozin arabinosid almıştır. Diğer üç hastanın kurtarma protokolleri prokarbazin, metronomik siklofosfamid ve prednizolon şeklindeydi. Bu hastalardan ikisine PH nedeniyle kurtarma tedavisi başlandı yalnızca 28 ve 44 gün yaşadılar. Üçüncü hasta LOPP’nin tamamlanmasından sonra PD’nin tespit edilmesi üzerine kurtarma tedavisine başlamıştır. Bu hasta çalışmanın tamamlandığı tarihe kadar 183 gün boyunca kurtarma protokolü almıştır.
3.3 | Prognostik faktörler
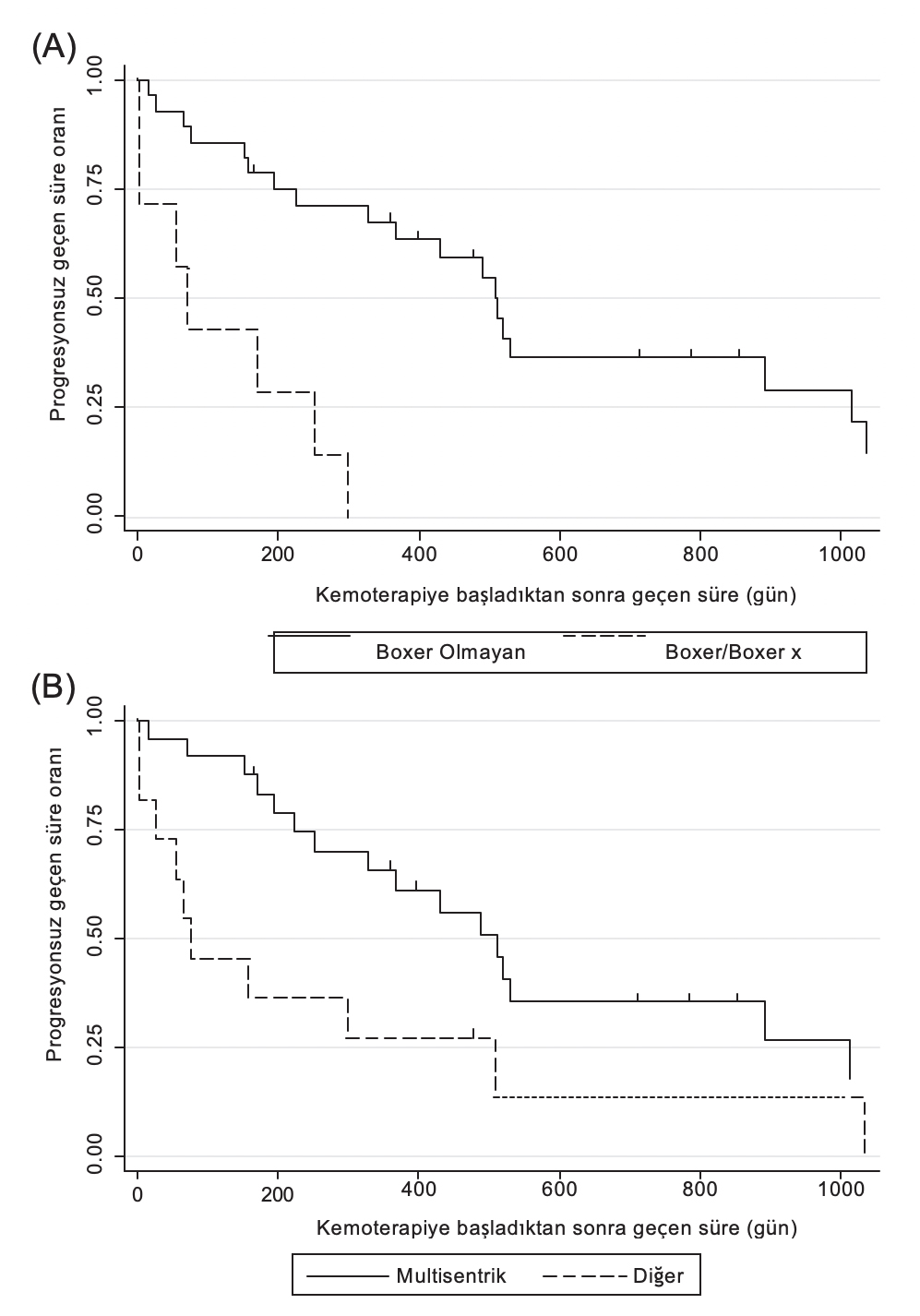
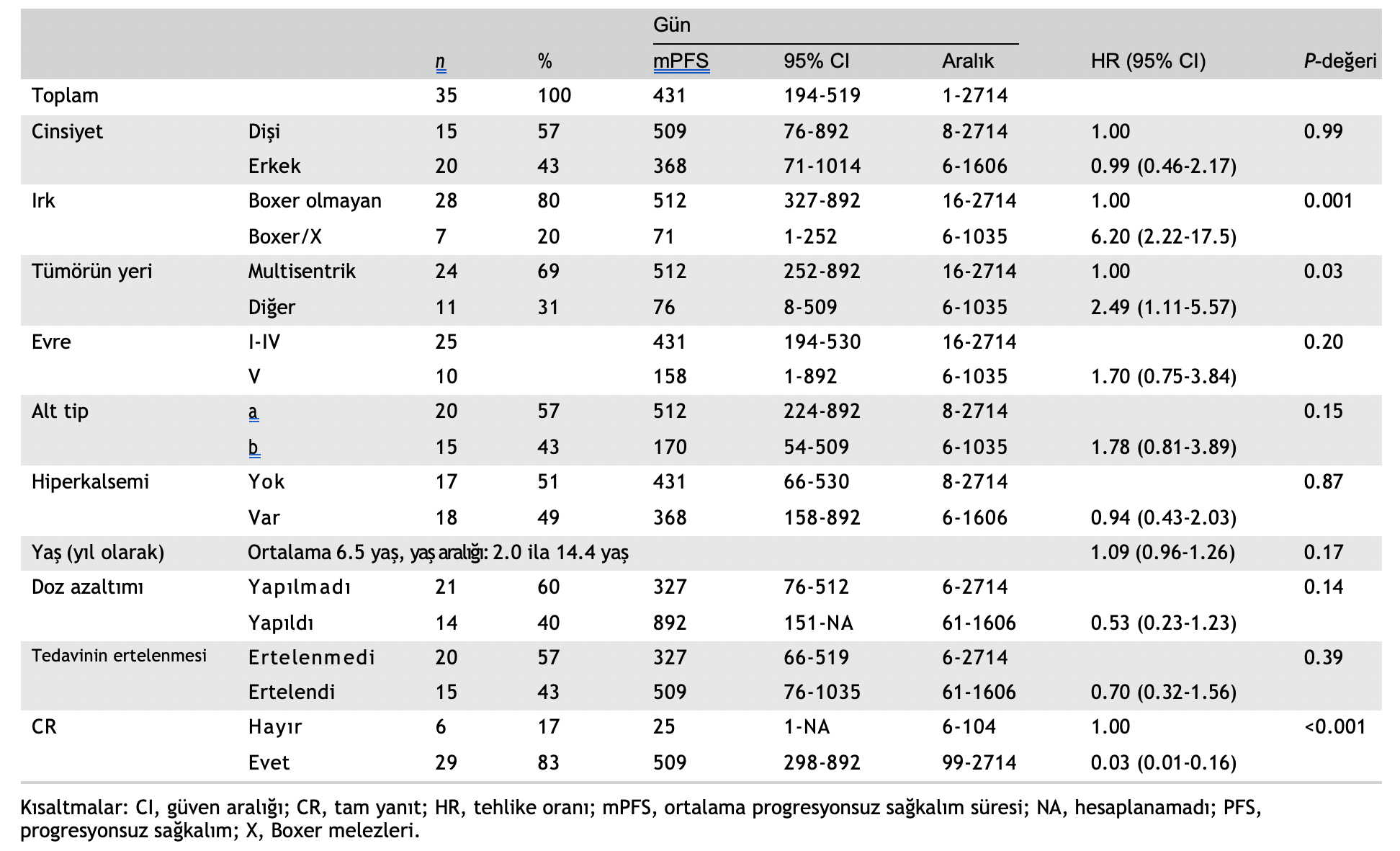
Tek değişkenli analizde ırk (Boxer/Boxer melezleri vs Boxer olmayan, Şekil 2A), tümörün yeri (multisentrik vs diğer, Şekil 2B) ve hastada CR elde edilip edilmediği (evet vs hayır) PFS süresi ile bağlantılı bulunurken yaş, cinsiyet, evre, alt tip ve hiperkalseminin olup olmaması ile PFS süresi arasında bir bağlantı bulunmamıştır (Tablo 4).
Çok değişkenli analizde, yalnızca ırk P < 0.05 düzeyinde PFS ile ilişkilendirilirken, lokasyon istatistiksel olarak anlamlı olmaya yaklaşmıştır. Boxer ve Boxer melezleri, Boxer olmayanların yaklaşık altı katı oranında PD’ye sahipti (tehlike oranı 5.22, %95 GA 1.82-14.93, P = 0.002) ve multisentrik dışındaki lokasyonlarda lenfoması olan köpekler, multisentrik lenfoması olan köpeklerin yaklaşık iki katı oranında PD’ye sahipti (tehlike oranı 2.0, %95 GA 0.88-4.61, P = 0.10).
3.4 | CR ile ilişkilendirilen faktörler
Lokasyon, CR görülme olasılığı ile ilişkili bulunan tek hasta değişkeniydi. Multisentrik T hücreli lenfomalı köpeklerle karşılaştırıldığında, diğer lokasyonlarda tümörü bulunan köpeklerde CR olasılığı çok daha düşüktü ( olasılık oranı 0.04, %95 CI 0.003-0.37, P = 0.002).
ŞEKİL 2 A, Irka göre Kaplan-Meier progresyonsuz sağkalım (PFS) eğrisi, yani Boxer/Boxer-melezleri vs Boxer olmayan. B, tümörün yerine göre Kaplan-Meier PFS eğrisi, yani multisentrik vs diğer yerler
TABLO 4 mPFS süreleri, %95 CI, PFS süresi aralığı ve dikkate alınan değişkenlerin tek değişkenli Cox regresyon analizi sonuçları
3.5 | Yan Etkiler
Otuz köpekte (%86) protokol sırasında AE görülmüş olup bunların %73’ü grade 1 veya 2’dir (Tablo 5). Yirmi altı hastada (%74) 23 köpekte (%66) bulantı, 19 köpekte (%54) kusma ve 14 köpekte (%40) ishal olmak üzere gastrointestinal yan etkiler görülmüştür. On sekiz köpekte (%51), 15’inde (%43) nötropeni ve 11’inde (%31) trombositopeni olmak üzere miyelosupresyon meydana gelmiştir. Altı köpekte (%17) protokol sırasında ALT artışı görülmüştür.
Genel olarak, sekiz hasta (%23) hastaneye yatırılmıştır; ancak, bu hastalardan 4’ünün başlangıçta alt evrede olduğu ve tedavi başlangıcında hastaneye yatırıldığı ve dört köpeğin (%11) tedavi protokolü sırasında AE’ler nedeniyle hastaneye yatırıldığı unutulmamalıdır. On beş köpekte (%43) AE’ler nedeniyle tedavinin ertelenmesi ve 14 köpekte (%40) doz azaltılması gerekmiştir.
Üç köpek (%9) LOPP tamamlandıktan sonra böbrek yetmezliği nedeniyle ölmüştür.
4 | TARTIŞMA
Bu çalışmada modifiye LOPP protokolü ile tedavi edilen yüksek gradeli T hücreli lenfomalı köpeklerin sonuçları incelenmiştir. Ortalama PFS süresi 431 gün ve MST 507 gün olarak bulunmuştur. Bu sağkalım süreleri, T hücreli lenfomalı köpeklerde daha önce yayınlanan sonuçlardan daha uzundur. Brown ve ark.15 31 köpekte modifiye LOPP protokolünün kullanımını araştıran benzer bir çalışma gerçekleştirmiş ve ortalama hastalıksız geçen süreyi 176 gün (aralık 0-1745) ve MST’yi 323 gün (aralık 51-1758) olarak bulmuştur. Mevcut çalışmada, Brown’ın çalışmasında kullanılan LOPP tabanlı protokole benzer bir protokol kullanılarak, eski protokollere kıyasla daha uzun sağkalım süreleri elde edilmiştir.
CHOP protokolü köpek lenfoması için ilk basamak tedavi olarak yaygın şekilde kullanılmaktadır. Garrett ve ark.19 multisentrik lenfoma için CHOP ile tedavi edilen köpeklerde sırasıyla 282 ve 397 günlük ortalama PFS süresi ve MST bulmuş ancak immünofenotipler arasındaki farklılıkları araştırmamıştır. Rebhun ve ark.16 CHOP’un T hücreli lenfoma için ilk basamak tedavi olarak kullanımını araştırmış, ortalama ilk remisyon süresini 104 gün ve MST’yi 235 gün olarak bulmuştur.
Bu çalışmada, daha önce LeBlanc ve ark. tarafından sunulan LOPP protokolü modifiye edilmiştir. LeBlanc ve ark.20 44 köpekte 28 günlük altı kürden oluşan bir LOPP protokolü kullanmıştır. Hastalara 1. günde lomustin (60-70 mg m-2 PO), 1. ve 8. günlerde vinkristin (0,7 mg m-2 IV), 2 ila 15. günlerde prokarbazin (50 mg m-2 PO) ve prednizolon (30 mg m-2) verilmiştir. Hastaların yüzde yirmi beşi LOPP protokolünü tamamlamıştır. Bu makalede, hastaların sırasıyla %63,6’sı, %38,6’sı ve %38,6’sında en az bir grade 2 veya daha yüksek
nötropeni, trombositopeni ve gastrointestinal toksisite atağı ile ciddi AE’ler bildirilmiştir.
Tedaviye bağlı ölümlerin %9 olduğu ve hastaneye yatış gerektiren 11 ölümcül olmayan septik durumun yaşandığı bildirilmiştir. AE’ler nedeniyle doz azaltma ve tedavide gecikmeler sıklıkla görülmüştür. Mevcut makalede kullanılan protokol, lomustin 60 mg m-2’ye düşürülerek AE’leri azaltmak amacıyla değiştirilmiş ve vinkristin aynı dozda ancak 14 günde bir uygulanacak şekilde yeniden ayarlanmıştır. Prokarbazin ve prednizolon uygulamasında herhangi bir değişiklik yapılmamıştır.
Brown ve arkadaşlarının çalışmasında LOPP protokolünde farklı modifikasyonlar uygulanmıştır. Brown ve arkadaşları vinkristini her 14 günde bir 0,5 mg m-2 olarak uygulamışlardır. Kemoterapi ilaçlarının uygulandığı günlerde de farklılık vardı. Brown ve arkadaşları vinkristin, lomustin ve prokarbazini ardışık günlerde (1-3. günler) uygulamış ve prokarbazin toplam 12 gün boyunca devam ettirilmiştir. Bu çalışmada ise vinkristin lomustin ile aynı gün (1. gün), prokarbazin ise ertesi gün (2. gün) uygulanmış ve 14 gün boyunca devam edilmiştir.
Brown ve arkadaşlarının MST’si mevcut çalışmadaki MST’den daha kısadır, ancak Brown ve arkadaşlarının çalışmasında elde edilen MST’nin mevcut çalışmada elde edilen MST’nin %95 CI’sı içinde olduğu unutulmamalıdır, yani farklı MST’ler rastlantısal ve her iki çalışmadaki köpek sayısının nispeten az olmasından kaynaklanıyor olabilir. İki protokolün etkinliği arasında gerçek bir fark olması da mümkündür. Her iki çalışmada da lomustin, vinkristin ve prokarbazin ilaçları için doz yoğunluğu hesaplamaları yapılmıştır. Mevcut çalışmada, bu ilaçlar için doz yoğunlukları sırasıyla 15 mg hafta-1, 0,35 mg hafta-1 ve 175 mg hafta-1 ve Brown’ın makalesinde 15 mg hafta-1, 0,25 mg hafta-1 ve 150 mg hafta-1 idi. Bu doz yoğunluğu hesaplamaları, mevcut çalışmadaki hastaların maksimum tolere edilebilir doza daha yakın tedavi edildiğini doğrulamaktadır. Daha yüksek doz yoğunlukları, mevcut çalışmada görülen yüksek toksisite oranına da yol açmış olabilir. Hastalar maksimum tolere edilebilir doza daha yakın tedavi edildiklerinden, tedavi daha etkili olmuş ve böylece daha uzun sağkalım süreleri elde edilmiş olabilir. Brown ve arkadaşları ortalama PFS süresini değil hastalıksız geçen süreyi araştırmıştır, dolayısıyla bu parametreler doğrudan karşılaştırılamamaktadır.
Brown ve arkadaşları, mevcut çalışmadaki %86’ya kıyasla AE yaşayan köpeklerin %42’sinde daha düşük toksisite bildirmiştir. Her iki çalışmada da AE’ler VCOG-CTCAE’ye göre derecelendirilmiştir. Bu çalışmadaki gastrointestinal AE’lerin %89’u grade 1 ve 2 idi. Nötropenik duruma gelen 15 köpeğin %80’i grade 3 veya 4 ve trombositopenik hastaların %55’i grade 3 veya 4 idi. Protokol sırasında hiçbir hastada grade 5 AE görülmemiştir. Altı köpekte yüksek ALT seviyeleri görülmüştür, bunların hepsi grade 1 veya 2 idi. Üçüncü lomustin dozundan sonra grade 2 artışı olan bir köpeğe günde bir kez 23 mg kg-1 PO S-Adenozilmetiyonin (SAMe) verildi ve lomustine devam edildi. Bu köpeğin ALT değeri 2 hafta sonra normal sınırlar içindeydi. Yüksek ALT değerlerine sahip diğer köpekler SAMe almadı ve LOPP protokolüne devam etti. Bu köpeklerde ilerleyici nitelikte yüksek ALT değerleri görülmemiştir.
Üç köpek LOPP protokolü ile tedavi edildikten sonra böbrek yetmezliği nedeniyle ötenazi edilmiştir. Bir hastada tedavinin başlangıcında grade 1 hiperkalsemi ve grade 1 BUN ve kreatinin yüksekliği vardı. Hiperkalsemi ve azotemi protokol esnasında düzelmiş ancak 452. günde tekrarladığı tespit edilmiş ve hastaya 854. günde ötenazi uygulanmıştır. Başka bir hasta da ilk geldiğinde hiperkalsemikti (grade 1) ancak BUN ve kreatinin değerlerinde yükselme yoktu. Bu köpekte 918. günde azotemi görülmüş ve 923. günde ötenazi yapılmıştır. Üçüncü hasta, tamamlanan LOPP’nin başlangıcında hiperkalsemik veya azotemik değildi. Bu köpekte 529. günde azotemi görülmüş ve 530. günde ötenazi yapılmıştır. Lomustin uygulaması sonrası renal toksisite köpeklerde daha önce de rapor edilmiştir. Heading ve ark.21 lomustin ile tedavi edilen 206 köpek üzerinde retrospektif bir çalışma gerçekleştirmiş ve 11 köpekte (%12) uygulama sonrası azotemi geliştiğini tespit etmiştir. Bu köpekler için ortalama lomustin dozu sayısı 8,1 ( ortalama 4) idi. Mevcut çalışmada, böbrek yetmezliği nedeniyle ötenazi uygulanan köpeklerde ortalama lomustin dozu sayısı 5,6, ortalama sayısı ise 6’dır.
Goodman ve arkadaşları14 VELCAP-TSC’nin T hücreli lenfomalı köpekler için ilk basamak tedavi olarak kullanımını araştırmış ve ortalama PFS süresini 175 gün (%95 CI 119-231 gün) ve MST süresini 237 gün (%95 CI 186-288 gün) şeklinde bulmuştur. Bu çalışmada, köpeklerin %91’inde gastrointestinal yan etkiler, %90’ında nötropeni ve %41’inde protokol boyunca hastaneye yatış gerektiren ciddi AE’ler görülmüştür. Mevcut çalışmada köpeklerin %74’ü gastrointestinal AE’ler ve %51’i miyelosupresyon yaşamış ve köpeklerin %11’i bu AE’ler nedeniyle hastaneye yatırılmıştır. Bu durum, karşılaştırılabilir diğer LOPP çalışmasından daha yüksek AE’ler görülmesine rağmen, mevcut çalışmada VELCAP-TSC protokolünden daha düşük AE’ler görüldüğünü ve bu çalışmaların her ikisinden de daha uzun PFS ve MST elde edildiğini göstermektedir.
T hücreli lenfoma için birinci basamak kemoterapi protokolünü araştıran başka bir çalışma Brodsky ve arkadaşları13 tarafından yapılmıştır. Bu çalışmada, 50 köpekte L- Asparaginaz ve MOPP kullanılmış ve ortalama PFS süresi 189 gün (%95 CI 99-278 gün) ve MST süresi 270 gün (%95 CI 206-333 gün) olmuştur. Bu protokol kullanıldığında, köpeklerin %76’sında hematolojik toksikozlar (%38’inde nötropeni ve %60’ında trombositopeni) ve %78’inde gastrointestinal AE’ler görülmüştür. LOPP protokolü, mekloretaminin bulunamaması ve karmaşık protokol nedeniyle MOPP protokolüne alternatif olarak geliştirilmiştir.20,22
Mevcut çalışmada 2 yıllık PFS %29 bulunmuştur. 2 yıllık sağkalım oranlarını rapor eden diğer çalışmalarda Brown ve arkadaşları %25, Goodman ve arkadaşları %20, Brodsky ve arkadaşları ise 939 günde (2,5 yıl) hayatta kalan köpeklerin oranını %25 olarak bulmuştur.13-15
LOPP’yi tamamlamayan ancak uzun süreli hayatta kalan dört köpekten ilk hasta dört LOPP döngüsünü tamamlamış ve 923. günde böbrek yetmezliği ve üçüncü derece kalp bloğu nedeniyle ötenazi edilmiştir. İkinci hastada spinal lenfoma vardı, iki kür LOPP’yi tamamladı, grade 3 nötropeni ve grade 1 trombositopeni görüldü ve hastayı sevk eden veterinerde 1035 günde “yaşlılık” nedeniyle ötenazi uygulandı. Bu köpeklerin her ikisinde de protokolün neden sonlandırıldığı bilinmemektedir. Kalan iki hasta Shetland Koyun Köpeği olup, bunlardan birinde ABCB1 durumu heterozigot, diğerinde ise homozigot normaldi. ABCB1 mutasyonları, P-glikoprotein aracılı ilaç taşınmasının inhibisyonundan kaynaklanan bazı kemoterapötik ajanlar da dahil olmak üzere birçok ilaçtan kaynaklanan toksikozlara karşı artan duyarlılıkla ilişkilendirilmiştir.23,24 Bu hastaların her ikisinde de protokol boyunca ciddi kemik iliği baskılanması (grade 3 ve 4 nötropeni ve her ikisinde de grade 4 trombositopeni) yaşanmış ve doz azaltımı ve tedavide gecikmeler yaşanmıştır.
Bu köpekler bu AE’ler nedeniyle LOPP protokolünü tamamlamamıştır. Bir hasta çalışmanın tamamlandığı 783. günde CR aşamasındaydı. Diğer hastada 162. günde PD tespit edilmiş ve L-asparaginaz, vinkristin ve metronomik siklofosfamidden oluşan bir kurtarma protokolü ile vinkristin ve sitozin arabinosid ile dönüşümlü olarak tedavi edilmiştir. Bu kurtarma bir kez kullanılmış ve hastada grade 4 trombositopeni olduğu için kesilmiştir. Bu hasta da çalışmanın tamamlandığı 552. günde CR’deydi.
Mevcut çalışma büyük oranda Boxer ve Boxer melezleri (yedi köpek, %20), Boxerların T hücreli lenfoma hastalığına yatkın olduğunu ortaya koyan çeşitli makalelerle tutarlılık göstermektedir.13,25-28 Bu çalışmada ayrıca Boxerların ve Boxer melezlerinin MST 99 gün (%95 CI 6-252 gün) ile sağkalım sürelerinin kısa olduğu bulunmuştur. Goodman ve arkadaşları14 da benzer şekilde Boxer ırkının T hücreli lenfomalı köpekler için olumsuz bir prognostik gösterge olduğunu ve MST’nin 141 gün (%95 CI 115-167 gün) olduğunu bulmuştur.
Bu çalışmanın çeşitli kısıtlamaları bulunmaktadır. Çalışmada kontrol kolunun olmaması, retrospektif yapısı ve örneklem sayısının az olması önemli kısıtlamalardır; ancak bunlar veteriner literatüründe yaygındır. Her hasta için rutin şekilde tam klinik evreleme yapılmamıştır ve klinisyenin alt evre a veya b değerlendirmesi tamamen subjektiftir ve tutarsız olabilir. Potansiyel olarak yanıltıcı bir faktör de düşük gradeli/ indolent lenfomaların verilere dahil edilmiş olma olasılığıdır. Hastaların hepsinde hızlı PH öyküsü vardı, bu da doğrulanamasa da yüksek gradeli lenfoma ile klinik ilerlemenin nispeten daha uyumlu olduğunu düşündürmektedir.
5 | SONUÇ
Veteriner literatürü, örneklem büyüklüğü ve tedavi seçenekleri açısından beşeri tıp literatürünün oldukça gerisindedir. İnsan literatürü, tedavi protokollerini ileri düzeyde doğrulayan ve tekrarlanan çalışmalarla güçlendirilmiştir. Brown ve arkadaşlarının çalışmasıyla birlikte mevcut çalışma, köpek T hücreli lenfoması için ilk basamak tedavi olarak modifiye edilmiş bir LOPP protokolünün kullanılmasını önermektedir ve her iki çalışma da daha önce görülenden daha uzun MST’ler ortaya koymaktadır. Bu çalışmada kullanılan LOPP protokolü ayrıca T hücreli lenfomalı köpekler için CHOP ile tedavi edilen B hücreli lenfomalı köpeklerde bulunandan daha yüksek bir ortalama PFS süresine ve MST’ye sahipti. Bu çalışmada kullanılan modifiye LOPP protokolü, önceki LOPP çalışmasına kıyasla daha fazla toksisiteye sahip olsa da, tüm hastalar tıbbi tedavi altında tutulmuş ve daha yüksek doz yoğunluğu, hastaların maksimum tolere edilebilir doza daha yakın tedavi edilmesini sağlamıştır; bu da potansiyel olarak daha uzun ortalama PFS süresi ve MST sağlamaktadır. Bu çalışmadan elde ettiğimiz sonuçlara göre önerimiz, bu protokolün kullanımı için daha güçlü kanıtlar sağlamak üzere LOPP ve CHOP’u içeren randomize kontrollü çalışmaların yapılmasıdır.
ORCID
KAYNAKÇA
- Vail D, Pinkerton M, Young K. Hematopoietic In: Withrow SJ, Vail DM, Page RL, eds. Withrow & MacEwen’s Small Animal Clinical Oncology. 5th ed. St Louis,MO: Elsevier; 2013:608.
- Burton J, Garrett-Mayer E, Thamm D. Evaluation of a 15-week CHOP protocol for the treatment of canine multicentric Vet Comp Oncol. 2013;11(4):306-315.
- Guija de Arespacochaga A, Schwendenwein I, Weissenbock Retro- spective study of 82 cases of canine lymphoma in Austria based on the working formulation and immunophenotyping. J Comp Pathol. 2007;136(2–3):186-192.
- Sorenmo K, Overley B, Krick E, et Outcome and toxicity associated with a dose-intensified, maintenance-free CHOP-based chemotherapy protocol in canine lymphoma: 130cases. Vet Comp Oncol. 2010;8(3):196-208.
- Simon D, Nolte I, Eberle N, et al. Treatment of dogs with lymphoma using a 12-week, maintenance-free combination chemotherapy proto- J Vet Intern Med.2006;20:948-954.
- Rassnick K, Bailey D, Malone E, et al. Comparison between L-CHOP and an L-CHOP protocol with interposed treatments of CCNU and MOPP (L-CHOP-CCNU-MOPP) for lymphoma in dogs. Vet Comp Oncol. 2010;8(4):243-253.
- Beaver L, Strottner G, Klein Response rate after administration of a single dose of doxorubicin in dogs with B-cell or T-cell lymphoma: 41 cases (2006–2008). J AmVet Med Assoc. 2010;237(9):1052-1055.
- Curran K, Thamm D. Retrospective analysis for treatment of naive canine multicentric lymphoma with a 15-week, maintenance-free CHOP Vet CompOncol. 2016;14(1):147-155.
- Pawlak A, Rapak A, Drynda A, et Immunophenotypic characteriza- tion of canine malignant lymphoma: a retrospective study of cases diagnosed in Poland Lower Silesia, over the period 2011-2013. Vet Comp Oncol. 2016;14(Suppl 1):52-60.
- Zandvliet Canine lymphoma: a review. Vet Q 2016; 36(2): 76–104.
- Chun R, Garrett L, Vail D. Evaluation of a high-dose chemotherapy protocol with no maintenance therapy for dogs with J Vet Intern Med. 2000;14:120-124.
- Zandvliet M, Teske E, Schrickx J, Mol J. A longitudinal study of ABC transporter expression in canine multicentric Vet J. 2015; 205(2):263-271.
- Brodsky E, Maudlin G, Lachowicz J, Post Asparaginase and MOPP treatment of dogs with lymphoma. J Vet Intern Med. 2009;23(3):578-584.
- Goodman I, Moore A, Frimberger Treatment of canine non-indolent T cell lymphoma using the VELCAP-TSC protocol: a retrospective evaluation of 70 dogs (2003-2013). Vet J. 2016;211:39-44.
- Brown PM, Tzannes S, Nguyen S, White J, Langova V. LOPP chemo- therapy as a first-line treatment for dogs with T-cell lymphoma. Vet Comp Oncol.2018;16(1):108-113.
- Rebhun RB, Kent MS, Borrofka SA, Frazier S, Skorupski K, Rodriguez CHOP chemotherapy for the treatment of canine mul- ticentric T-cell lymphoma. Vet CompOncol. 2011;9(1):38-44.
- Vail D, Michels G, Khanna C, et Response evaluation criteria for periph- eral nodal lymphoma in dogs (v1.0): a Veterinary Cooperative Oncology Group (VCOG) consensusdocument. Vet Comp Oncol. 2010;8(1):28-37.
- Veterinary cooperative oncology group – common terminol- ogy criteria for adverse events (VCOG-CTCAE) following chemother- apy or biological antineoplastic therapy in dogs and cats v1.1. Vet Comp Oncol. 2016;14(4):417-446.
- Garrett L, Thamm D, Chun R, Dudley R, Vail D. Evaluation of a 6-month chemotherapy protocol with no maintenance therapy for dogs with J Vet InternMed. 2002;16:704-709.
- LeBlanc A, Mauldin G, Milner R, et al. Efficacy and toxicity of BOPP and LOPP chemotherapy for the treatment of relapsed canine lym- Vet Comp Oncol.2006;4(1):21-32.
- Heading K, Brockley L, Bennett CCNU (lomustine) toxicity in dogs: a retrospective study (2002–07). Aust Vet J. 2011;89(4):109-116.
- Fahey C, Milner R, Barabas K, et al. Evaluation of the University of Florida lomustine, vincristine, procarbazine, and prednisone chemo- therapy protocol for the treatment of relapsed lymphoma in dogs: 33 cases (2003–2009). J Am Vet Med Assoc. 2011;239(2):209-215.
- Mealey K, Fidel J. P-glycoprotein mediated drug interactions in ani- mals and humans with J Vet Intern Med. 2015;29(1):1-6.
- Mealey K. Canine ABCB1 and macrocyclic lactones: heartworm pre- vention and Vet Parasitol. 2008;158(3):215-222.
- Pastor M, Chalvet-Monfray K, Marchal T, et al. Genetic and environ- mental risk indicators in canine non-Hodgkin’s lymphomas: breed associations and geographic distribution of 608 cases diagnosed throughout France over 1 J Vet Intern Med. 2009;23(2):301-310.
- Lurie D, Lucroy M, Griffey S, Simonson E, Madewell B. T-cell-derived
malignant lymphoma in the boxer breed. Vet Comp Oncol. 2004;2(3): 171-175.
- Jankowska U, Jagielski D, Czopowicz M, Sapierzyn´ski The animal-dependent risk factors in canine T-cell lymphomas. Vet Comp Oncol. 2015;5(2):307-314.
- Sayag D, Fournel-Fleury C, Ponce F. Prognostic significance of mor- photypes in caninelymphomas: a systematic review of Vet Comp Oncol. 2018;16(1):12-19.
- Bu makaleye atıfta bulunmak için: Morgan E, O’Connell K, Thomson M, Griffin A. Canine T cell lymphoma treated with lomustine, vin- cristine,procarbazine, and prednisolone chemotherapy in 35 dogs. Vet Comp Oncol. 2018;1–8. https://doi.org/10.1111/ vco.12430