| 1Ohio Eyalet Üniversitesi Veteriner Hekimliği Fakültesi, Klinik Bilimler Bölümü, Columbus, Ohio, ABD 2Nashville Uzman Veteriner Hekimliği, Nashville, Tennessee, ABD İletişim Güncel adresler Bu makale, orijinal çalışmaya uygun şekilde atıfta bulunulması ve ticari amaçlarla kullanılmaması koşuluyla, herhangi bir ortamda kullanım, dağıtım ve çoğaltmaya izin veren Creative Commons Attribution-NonCommercial License koşulları altında açık erişimli bir makaledir. |
| Özet Ön bilgi: Kemoterapi ilaçlarının vücut yüzey alanına göre geleneksel olarak dozlanması, küçük köpeklerde aşırı doza neden olarak yan etkilerin (AE) sıklığında artışa yol açabilir. Hipotez/Amaçlar: Vinkristin ile tedavi edilen ≤15 kg ağırlığındaki yeni tanı konmuş lenfomalı köpeklerde hematolojik ve gastrointestinal AE’lerin sıklığını >15 kg ağırlığındaki köpeklere kıyasla değerlendirmek. Hipotezimiz, ≤15 kg ağırlığındaki köpeklerin daha yüksek AE sıklığı yaşayacağıdır. Hayvanlar: Yeni tanı konmuş lenfomalı yüz otuz sekiz köpek vinkristin ile tedavi edildi. Yöntemler: Hematolojik verileri ve tıbbi kayıt bilgilerini gözden geçiren çok merkezli retrospektif bir çalışma yapıldı. Tam kan sayımları vinkristin uygulamasından en fazla 24 saat önce ve daha sonra uygulama sonrası 4 ila 8 gün arasında yapıldı. Veriler lojistik regresyon veya ordinal lojistik regresyon kullanılarak değerlendirildi. Sonuçlar: Çalışmaya ≤15 kg ağırlığında 38 köpek ve >15 kg ağırlığında 100 köpek dahil edilmiştir. Her iki grup için medyan vinkristin dozu 0.6 mg/m2 idi. On yedi (%12,3) nötropeni vakası meydana gelmiştir ve gruplar arasında genel sıklık veya derece açısından anlamlı bir fark görülmemiştir. Başlangıçta asemptomatik olan otuz alt evre A köpekte (%29,4) gastrointestinal AE’ler görülmüştür. Gastrointestinal destekleyici bakım ilaçlarının yaygın kullanımı nedeniyle gruplar arasında istatistiksel karşılaştırma yapılamamıştır. Yedi kez hastaneye yatış gerçekleşmiş (%5.0) ve hastaneye yatış riski gruplar arasında istatistiksel olarak anlamlı farklılık göstermemiştir (P = .37). Sonuçlar ve Klinik Önem: ≤0,6 mg/m2 dozunda uygulanan vinkristin, ≤15 kg ağırlığındaki köpeklerde hematolojik AE riskini artırmamaktadır. ANAHTAR KELİMELER Kısaltmalar: AE, yan etki; BSA, vücut yüzey alanı; CHOP, siklofosfamid, doksorubisin, vinkristin ve prednizon; MDR, çoklu ilaç direnci. |
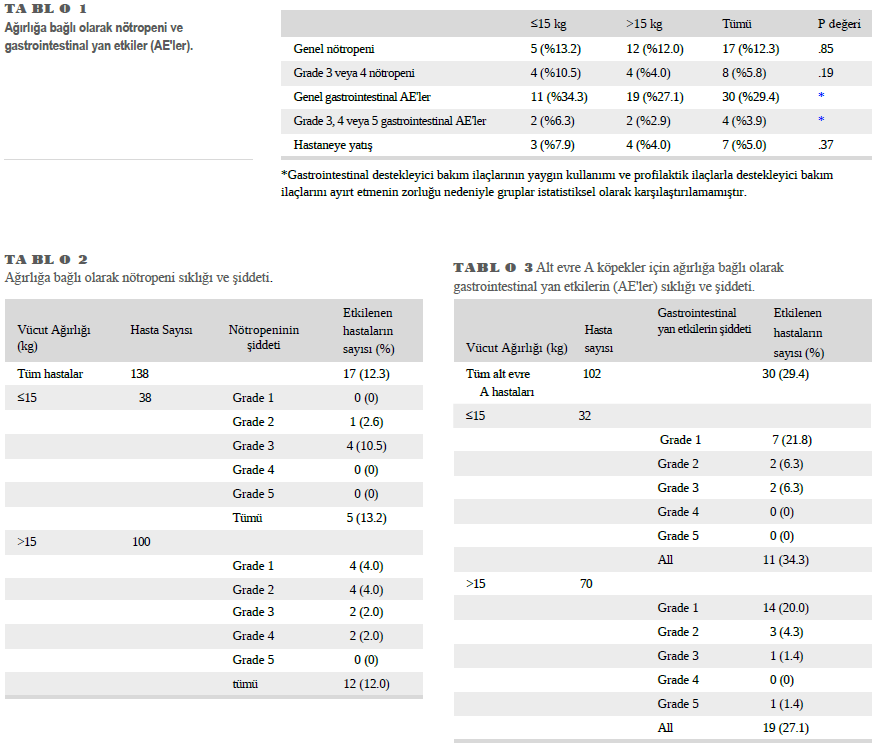
| GİRİŞ Vinkristin, tubulin bağlanması yoluyla mitozu inhibe eder, böylece bölünen hücrelerin mitotik ölümüne neden olur.2,3 Siklofosfamid, doksorubisin, vinkristin ve prednizon (CHOP) bazlı protokollerin bir parçası olarak köpeklerde lenfoma tedavisinde yaygın olarak kullanılır.1 Genellikle kemoterapide yaygın olarak kullanılan diğer ilaçlardan daha az miyelosupresif olduğu düşünülse de, vinkristin aldıktan sonra köpeklerde nötropeni nedeniyle doz azaltılması nadir görülen bir durum değildir.4–6 İki yayında, vinkristinin doksorubisinden sonra nötropeni ve ateşle ilişkili en olası kemoterapi ajanlarından biri olduğu gösterilmiştir.7,8 Bu nötropenik olayların çoğu hastanın ilk kemoterapi protokolü (indüksiyon fazı)7,8 sırasında ve yaklaşık %50’si ilacı ilk kez aldıktan sonra meydana gelmiştir.8 Geleneksel olarak, vücut yüzey alanı (BSA), vücut ağırlığına kıyasla ilaç dağılımı, metabolizması ve atılımının daha doğru bir şekilde tahmin edilmesini sağladığı varsayımıyla kemoterapi ajanlarının dozajlanmasında kullanılmaktadır.9 Bununla birlikte, köpeklerde vücut ağırlığını kullanarak BSA’yı belirlemeye yönelik formüller, küçük örneklem boyutları ve sınırlı ağırlık dağılımları olan çalışmalardan elde edilmiştir.10 Küçük köpeklerin büyük köpeklere kıyasla daha yüksek bir metabolik hıza sahip olduğu ve muhtemelen BSA’dan bağımsız faktörlerin de kemoterapi ajanlarının farmakokinetiğinde önemli rol oynadığı varsayılmaktadır.11 Bu varsayım, küçük köpeklerin doksorubisin, karboplatin, mitoksantron, vinblastin ve melfalan gibi ilaçlar da dahil olmak üzere BSA’ya göre dozlandığında kemoterapiye bağlı miyelosupresyon ve gastrointestinal toksisite riskinin arttığını gösteren birkaç çalışma ile desteklenmektedir.12–17 Bu artan miyelosupresyon riskinin önemli klinik sonuçları olabilir çünkü küçük köpeklerin kemoterapi sonrası nötropeni ve ateş geçirme olasılığı daha yüksektir.8 Küçük köpeklerde, özellikle vinkristin içeren protokollerde kemoterapiye bağlı yan etki (AE) riskinin arttığı tespit edilmiş olsa da,7,8 yakın zamanda yapılan retrospektif bir çalışmada, Japonya’dan ortalama ağırlığı 9,6 kg olan bir grup köpekte vinkristine bağlı genel nötropeni riskinin düşük olduğu sonucuna varılmıştır.18 Ancak, bu çalışma kiloya bağlı AE’lerin analizini içermemektedir.18 Buna ek olarak, insanlarda kemoterapinin toleransı, AE’lerin sıklığı ve etkinliği açısından popülasyonlar arasında coğrafi farklılıklar olduğu görülmüştür.19–21 Konakçı ve tümör farklılıkları, tıbbi bakımın mevcudiyeti ve sosyoekonomik faktörler arasında karmaşık bir etkileşim olması muhtemeldir.19–21 Birincil amacımız, vinkristin ile tedavi edilen yeni tanı konmuş lenfomalı köpeklerde miyelosupresyon sıklığını kiloya göre karşılaştırmaktı. İkincil amacımız ise gastrointestinal AE’lerin sıklığını kiloya bağlı olarak değerlendirmekti. Hipotezimiz, ≤15 kg köpeklerin tek doz vinkristin uygulamasından sonra hem nötropeni hem de gastrointestinal AE’lerin sıklığında ve şiddetinde artış yaşayacağı yönündeydi. MATERYAL VE METOT Vaka Seçimi Vinkristin ile tedavi edilen köpekleri tespit etmek için 2008 ve 2022 yılları arasında Ohio Eyalet Üniversitesi Veteriner Tıp Merkezi ve 2021 ve 2022 yılları arasında Nashville Veteriner Uzmanları tıbbi kayıtlarında bir arama yapılmıştır. Çalışmaya dahil edilme kriterleri arasında sitolojik veya histolojik olarak orta ila büyük hücreli lenfoma tanısı; vinkristin uygulamasından en fazla 24 saat önce ve uygulamadan sonraki 4 ila 9 gün içinde tamamlanan bir CBC,2 vinkristin uygulamasından önceki 21 gün içinde bir serum biyokimya paneli ve IV olarak uygulanan 0,5 ila 0,7 mg/m2 arasında vinkristin dozu yer aldı. Lenfoma için çoklu ajan protokollerinde kortikosteroidlerin yaygın kullanımı göz önüne alındığında, eşzamanlı kortikosteroid kullanımına (vinkristin uygulamasından önce veya uygulama sırasında başlayarak) izin verilmiştir. Çalışmadan çıkarılma kriterleri arasında orta ila büyük hücreli lenfoma dışında bir tanı, vinkristin uygulaması sırasında nötropeni, (Ohio Eyalet Üniversitesi vakaları için 2,60 ila 10,80 × 109/L ve Nashville Veterinerlik Uzmanları vakaları için 2,30 ila 10,29 × 109/L olarak bildirilen referans aralığının altında nötrofil sayısı ile tanımlandığı şekilde), önceden veya eşzamanlı kemoterapi (L-asparaginaz dahil), profilaktik antibiyotik kullanımı, belgelenmiş çoklu ilaç direnci (MDR-1) mutasyonu olan köpekler veya MDR-1 mutasyonu açısından yüksek riskli kabul edilen ırklar (≥%10 riske sahip ırklar22 olarak tanımlanmıştır) ve laboratuvar verilerinin veya tıbbi kayıt bilgilerinin eksik olması yer almıştır. Melez köpekler için genetik soy değerlendirmesi yapılmamıştır ve bu köpekler MDR-1 mutasyonu açısından düşük riskli olarak kabul edilmiştir.22 Vinkristin esas olarak karaciğer tarafından metabolize edildiğinden ve safra yoluyla atıldığından,23 biliyer atılım bozukluğu (hiperbilirubinemi > 1,5 mg/ dL) kanıtı olan köpekler de hariç tutulmuştur. Tıbbi kayıtlardan alınan bilgiler arasında cins, yaş, ağırlık, vinkristin uygulaması ve kontrol muayenesi sırasındaki rektal veya kulaktan ateş, başlangıçtaki evreleme tanı testleri ve ilgili klinisyen tarafından atanan evre, immünofenotip (yapıldığında), vinkristin dozu, prednizon dozu ve prednizon başlama tarihi, vinkristin ile eş zamanlı olarak ve ilk takip vizitinden önceki süre boyunca uygulanan ilaçlar, kemoterapi ile ilişkili AE’ler nedeniyle hastaneye yatış ihtiyacı ve sonuçları ve ilk vinkristin uygulaması ile kontrol muayenesi arasında meydana gelen gastrointestinal AE’ler yer almıştır. Lenfomanın evrelendirilmesinde Dünya Sağlık Örgütü’nün (WHO) evcil hayvanlarda lenfoma için klinik evrelendirme sistemi esas alınmıştır.24 Evre V lenfoma tanımlaması, kan yaymasında şüpheli dolaşan neoplastik hücreler görüldüğünde (klinik patolog veya ilgili klinisyen tarafından) veya lenf nodu, karaciğer veya dalak dışındaki organların tutulumundan şüphelenildiğinde ilgili klinisyen tarafından yapılmıştır. Vinkristin tedavisi ve yan etkiler (AE) Vinkristin 0,5 ila 0,7 mg/m2 dozunda IV bolus olarak uygulanmıştır. Toksisite verileri tek bir vinkristin dozundan sonra toplanmıştır. Tam kan sayımları vinkristin uygulamasından önceki 24 saat içinde ve uygulamadan sonraki 4 ila 8 gün arasında gerçekleştirilmiştir. Tam kan sayımları Cell-Dyn (Abbott Laboratories, Abbott Park, Illinois, ABD), ADVIA 2120 (Siemens Medical Solutions, Malvern, Pennsylvania, ABD) veya Pro-Cyte (Idexx Laboratories, Westbrook, Maine, ABD) hematoloji sistemleri kullanılarak gerçekleştirilmiştir. Her bir CBC analizörü belirli bölgesel popülasyona göre standardize edilmiştir. Hematolojik AE’ler Veteriner Kooperatif Onkoloji Grubu AE kriterleri (VCOG-CTCAE) versiyon 2 kullanılarak puanlanmıştır.25 Gastrointestinal AE’lere ilişkin bilgiler, vinkristin uygulaması sırasında alt evre A olarak kabul edilen köpekler için tıbbi kayıt bilgileri ve VCOG-CTCAE versiyon 2 kılavuzları kullanılarak retrospektif olarak toplanmıştır.23 Birden fazla gastrointestinal AE türü belgelenen vakalarda, analiz için en yüksek grade kullanılmıştır. Gastrointestinal destekleyici bakım ilaçları hem profilaktik hem de semptomatik olarak ilgili klinisyenin takdirine bağlı olarak kullanılmıştır. İstatistiksel analiz Toplam 138 köpek dahil edilme kriterlerini karşılamıştır. Köpeklerin 68’i kısırlaştırılmış dişi, 2’si kısırlaştırılmamış dişi, 64’ü kısırlaştırılmış erkek ve 4’ü kısırlaştırılmamış erkekti. Kırk iki farklı ırk temsil edilmiş olup en yaygın ırklar melez köpekler, Labrador retrieverlar ve Golden retrieverlardır. Hiçbir MDR genetik testi rapor edilmemiştir ve MDR mutasyonu açısından yüksek riskli olduğu düşünülen hiçbir ırk dahil edilmemiştir. Ortalama yaş 9,1 idi ( yaş aralığı, 0,9-15,7). Ortalama vücut ağırlığı 25,9 kg (aralık, 3,8-58,2 kg) idi. Otuz sekiz köpek ≤15 kg ( ortalama 8,9 kg) ve 100 köpek >15 kg (ortalama 30,8 kg) ağırlığındaydı. SONUÇLAR Çoğu köpeğe akış sitometrisi ile veya akış sitometrisi olmadan sitoloji ile çok merkezli orta ila büyük hücreli lenfoma (n = 134) tanısı kondu. Bu köpeklerden ikisine akış sitometrisi kullanılarak eş zamanlı T bölgesi lenfoma ve orta ila büyük hücreli lenfoma teşhisi konmuştur. Bir köpekte akış sitometrisi kullanılarak nodal T bölgesi lenfoması tespit edilmiştir. Multisentrik olmayan vakalardan 1’er tanesinde mediastinal, kolorektal ve hepatosplenik lenfoma tespit edilmiştir. İmmünofenotip 104 vaka için mevcuttu: 91 köpekte (%87,5) B hücreli lenfoma (2’sinde T bölgesi mevcut) ve 13’ünde (%12,5) T hücreli lenfoma vardı. Torasik radyografiler ve abdominal ultrasonografi 80 köpeğe uygulandı. Köpeklerde lenfoma için DSÖ evreleme sistemine göre,24 3 köpek (%3,8) II. evre, 14 köpek (%17,5) III. evre, 31 köpek (%38,8) IV. evre ve 32 köpek (%40,0) şüpheli V. evre idi. Yüz iki köpek (%73,9) tanı sırasında alt evre A olarak kabul edildi ve kemoterapi sonrası gastrointestinal AE’lerin değerlendirilmesi için yalnızca bu köpekler dikkate alındı. Ağırlığı ≤15 kg olan 38 köpeğin 32’si alt evre A idi (%84,2). Ağırlığı >15 kg olan 100 köpeğin 70’i alt evre A idi (%70,0). Ağırlığı ≤15 kg olan köpekler için ortalama vinkristin dozu 0,60 mg/m2 (aralık, 0,5-0,7 mg/m2) idi. Bu grup için doz dağılımı şu şekildeydi: 0,5 mg/m2 (13 köpek), 0,55 mg/m2 (3 köpek), 0,6 mg/m2 (19 köpek) ve 0,7 mg/m2 (3 köpek). Ağırlığı >15 kg olan köpekler için ortalama vinkristin dozu da 0,6 mg/m2 (aralık, 0,5-0,7 mg/m2) olmuştur. Bu grup için doz dağılımı şu şekildeydi: 0,5 mg/m2 (43 köpek), 0,55 mg/m2 (5 köpek), 0,6 mg/m2 (36 köpek), 0,65 mg/m2 (2 köpek) ve 0,7 mg/m2 (14 köpek). Hiçbir köpek önceden veya eşzamanlı kemoterapi almamıştır. Üç köpek dışında tüm köpekler eş zamanlı olarak prednizon ile tedavi edilmiştir. Kırk bir köpek vinkristin uygulamasından önce prednizon almaktaydı ve ortalama süre kemoterapiden 8,1 gün önceydi (aralık, 1-30 gün). Doksan üç köpeğe vinkristin tedavisi sırasında prednizon başlanmıştır. Bir köpeğe vinkristinden 3 gün sonra prednizon başlandı. Ortalama prednizon dozu 1,3 mg/kg/gün (aralık, 0,4-3,3 mg/kg/gün) idi. Altı köpek ortalama 2,3 mg/kg (aralık, 2,1-3,26 mg/kg) olmak üzere >2,0 mg/kg prednizon dozu almıştır. Bu köpeklerden dördü tanı sırasında alt evre A idi ve ikisinde gaz-bağırsak AE’leri (evre 5 ileus ve evre 1 kusma) görüldü. Vinkristin uygulamasından ilk takip CBC’sine kadar geçen ortalama gün sayısı 7 gündü (aralık, 6-9 gün). On dokuz köpek vinkristinden 6 gün sonra, 89’u 7 gün sonra, 24’ü 8 gün sonra ve 6’sı 9 gün sonra değerlendirilmiştir. Genel olarak, 17 köpekte (%12,3) nötropeni görülmüş olup, 8 vaka (%5,8) grade 3 veya grade 4′ tü. Beş köpek ≤15 kg (%13,2) ve 12 köpek >15 kg (%12,0) nötropeni yaşamıştır. Gruplar arasında genel nötropeni sıklığı açısından anlamlı bir fark bulunmamıştır (P = .85; Tablo 1). Nötropeni yaşayan ≤15 kg 5 köpekte, bir vaka (%2,6) grade 2 nötropeni ve 4 vaka (%10,5) grade 3 nötropeni idi. Nötropeni görülen >15 kg 12 köpeğin her birinde 4 vaka (%4,0) grade 1 ve 2 nötropeni ve her birinde 2 vaka (%2,0) grade 3 ve 4 nötropeniydi (Tablo 2). İki köpekte ateş ve nötropeni vardı ve her ikisi de >15 kg idi. Evre 3 ve 4 nötropeni sıklığı açısından gruplar arasında istatistiksel olarak anlamlı bir fark bulunmamıştır (P = .19; Tablo 1). 0,6 mg/m2 her iki grupta da kullanılan ortalama doz olduğundan, bu dozu alan köpeklerdeki nötropeni sıklığı ayrı olarak analiz edilmiştir. 0,6 mg/m2 alan ≤15 kg ağırlığındaki 19 köpekte 3 nötropeni vakası (%15,8) meydana gelmiştir. 0,6 mg/m2 alan >15 kg ağırlığındaki 36 köpekte 4 nötropeni vakası (%11,1) meydana gelmiştir. Vinkristin dozu 0,6 mg/m2 olan gruplar arasında nötropeni sıklığı açısından istatistiksel olarak anlamlı bir fark bulunmamıştır (P = .65). Alt evre A köpeklerin 30’unda (%29,4) çoğunluğu (%70) grade 1 olmak üzere gastrointestinal AE’ler görülmüştür. On bir köpekte aynı anda birden fazla gastrointestinal AE görülmüştür. Kaydedilen 43 gastrointestinal AE’den en yaygın olanı diyare (%44,2) olup, bunu kusma (%23,1), hiporeksi (%17,3), anoreksi (%3,8), kabızlık (%3,8), letarji (%3,8), ileus (%1,9) ve bulantı (%1,9) takip etmiştir. Altmış alt evre A köpeğe (%58,8) çalışma süresi boyunca gastrointestinal destekleyici bakım ilaçları verilmiştir; bunların 26’sında (%43,3) gastrointestinal belirti rapor edilmemiştir. Bu tedaviler arasında maropitant, metronidazol, ondansetron, famotidin, loperamid, omeprazol, sukralfat ve psyllium husk yer almaktadır. Gastrointestinal AE’leri olan Alt Aşama A köpeklerinin gastrointestinal destekleyici bakım ilacı almış olma olasılığı önemli ölçüde daha yüksektir (P = .001). On bir alt evre A köpek ≤15 kg (%34,3) gastrointestinal toksisite yaşamıştır ve 2 vaka (%6,3) grade 3 veya daha yüksek olmuştur. On dokuz köpek >15 kg (%27,1) gastrointestinal toksisite yaşamıştır ve 2 vaka (%2,3) derece 3 veya daha yüksektir (Tablo 3). Bu gruptaki bir köpek, 0,7 mg/m2 vinkristin uygulamasından 15 gün sonra tıbbi tedaviye yanıt vermeyen şiddetli ileus nedeniyle ötenazi edilmiştir. Ancak bu köpekte de grade 3 nötropeni görüldü ve ateşi vardı. Klinik düşüşün nedeni olarak sepsis tam olarak ekarte edilememiştir. Her iki ağırlık grubundaki beklenmedik sayıda köpek, gastrointestinal belirti riskini artırdığı gösterilen ilaçlar da dahil olmak üzere gastrointestinal destekleyici bakım ilaçlarıyla tedavi edilmiştir.26-28 Gastrointestinal ilaçların kullanımında ağırlık grupları arasında anlamlı bir fark bulunmamasına rağmen (P = .79), çalışmanın retrospektif doğası göz önüne alındığında ilaçların profilaktik olarak mı yoksa semptomatik olarak mı verildiğini belirlemek zordu. Bu ilaçların önemli bir karıştırıcı faktör olma potansiyeli nedeniyle, gruplar arasında gastrointestinal AE’lerin istatistiksel bir karşılaştırmasını yapmamayı tercih ettik. Yedi köpeğin (%5,0) AE’ler nedeniyle hastaneye yatırılması gerekmiştir. Üçü (%7,9) ≤15 kg ve 4’ü (%4,0) >15 kg olan köpeklerdi. Gruplar arasında hastaneye yatış sıklığı açısından istatistiksel olarak anlamlı bir fark bulunmamıştır (P = .37; Tablo 1). Dört köpek sadece gastrointestinal bulgular nedeniyle hastaneye yatırılmıştır. İki köpekte gastrointestinal bulgulara ek olarak nötropeni (her biri grade 3) vardı. Bu köpeklerden biri ateşlendi ve sonuçta şiddetli ileus nedeniyle ötenazi uygulandı, diğeri ise ateşsizdi ve gastrointestinal destekleyici bakımın ardından taburcu edildi. Bir köpek ise gastrointestinal bulgular olmaksızın ateş ve nötropeni (grade 4) nedeniyle hastaneye yatırılmış ve iyileştikten sonra taburcu edilmiştir. Her iki febril nötropeni vakası da 15 kg’ın üzerindeki köpeklerde görülmüş olup çalışma popülasyonundaki genel sıklık %1,4’tür. Grade 3 veya 4 nötropenisi olan 8 köpekten üçünün (%37,5) hastaneye yatırılması gerekmiştir. Hastaneye yatırılan köpekler için ortalama vinkristin dozu 0,6 mg/m2 (aralık, 0,5-0,7 mg/m2) olmuştur. Sonuçlarımız, BSA ile dozlandığında daha küçük köpeklerin vinkristin tedavisinden sonra artmış nötropeni riski altında olmadığını göstermektedir. >15 kg köpeklerle karşılaştırıldığında ≤15 kg köpeklerin sayısal olarak daha yüksek oranda grade 3 ve 4 nötropeni yaşamasına rağmen (%10,5’e karşı %4,0), bu fark istatistiksel olarak anlamlı değildir. Ayrıca, küçük köpeklerin AE’ler nedeniyle hastaneye yatma riski büyük köpeklere göre daha yüksek çıkmamıştır. Çalışmamızda periferik nöropati ve ekstravazasyon gibi vinkristine ikincil diğer potansiyel AE’lerin sıklığını değerlendiren veriler toplanmamıştır. Kemoterapi ilaçlarının BSA’ya göre dozlanması, yüzey alanının metabolik hızın ve dolayısıyla ilaç metabolizması ve dağılımı için daha doğru bir gösterge olduğu varsayımıyla yapılmaktadır.9 Bu varsayım, daha küçük köpeklerde bazı ajanlar için kemoterapiyle ilişkili toksisitelerin daha yüksek olduğunu gösteren birçok çalışmada sorgulanmıştır.12–17 Daha küçük köpekler, daha yüksek yüzey alanı / vücut ağırlığı oranı nedeniyle kaçınılmaz olarak kilogram başına daha yüksek vinkristin dozu alacak olsalar da, bu ilacın ≤0,6 mg / m2 dozlarda BSA’dan bağımsız olarak aynı hematolojik AE sıklığına neden olduğu görülmektedir. Kemoterapötik ilaçların metabolizması, atılımı ve toksikozu, çoğu boyuttan bağımsız olan çeşitli konak faktörlerine bağlıdır.13 Vinkristinin farmakodinamiği, genel boyuttan ziyade ırk, yaş, hastalığın evresi ve komorbiditelerin varlığı gibi faktörlere bağlı olabilir. Ayrıca, burada bildirilenden daha yüksek dozlarda kiloya bağlı olarak AE sıklığında bir fark görülmesi de mümkündür. Vinkristin genellikle daha az miyelosupresif bir kemoterapötik ajan olarak kabul edilmesine rağmen, CHOP tabanlı kemoterapi süresince vakaların %14,3 ila %57,5’inde vinkristine ikincil nötropeni bildirilmiştir.6,18,29 Ayrıca, vinkristin ateş ve nötropeniye yol açan en yaygın ilaçlardan biri olarak gösterilmiştir.7,8 Genel olarak, çalışmamızdaki kohortun %12,3’ü nötropeni yaşamış ve bu köpeklerin yalnızca %5,8’i grade 3 veya 4 nötropeni yaşamıştır. Toksisite riskini artırabilecek karıştırıcı faktörleri sınırlamak için, burada değerlendirilen popülasyon kemoterapiye maruz kalmamıştı (L-asparaginaz dahil), klinik olarak ilgili hiperbilirubinemi yoktu ve MDR-1 mutasyonu riski daha düşük bir ırk olarak kabul edildi. Diğer çalışmalar, yakın zamanda L-asparaginaz uygulaması,30 ilacın kümülatif dozları veya kombine bir protokolün parçası olarak diğer ilaçlarla etkileşimler nedeniyle daha yüksek nötropeni sıklığı bildirebilir. Buna ek olarak, bizim çalışmamız sadece tek bir dozdan sonraki sıklığı bildirirken, çoğu çalışma bir protokol boyunca sıklığı bildirmektedir. Sonuçlarımız daha önce bildirilenleri doğrulamaktadır18 ve farklı bir coğrafyadan daha büyük bir kohortu temsil etmektedir. Önceki çalışmada, köpeklerin çoğu küçüktü ve ortalama ağırlıkları 9,6 kg idi. Vinkristine ikincil hematolojik (%14,3) ve gastrointestinal (%42,9) AE’lerin sıklığı, küçük köpeklerden oluşan kohortumuzda bulunan sayılara benzerdi (sırasıyla %12,3 ve %29,4).18 İnsanlarda çeşitli kemoterapi protokolleri ve malignitelerde kemoterapinin toleransı ve AE’lerin oranı ile ilgili coğrafi farklılıklar bildirilmiştir,19–21 ve bu nedenle Kuzey Amerika popülasyonunu incelemenin değerli olduğunu düşündük. Çalışmamıza 2 farklı kurum vaka sağlamış olsa da, lokasyonlar arasında ağırlık (P = .45), vinkristin dozu (P = .68) ve nötropeni sıklığı (P = .07) arasında istatistiksel olarak anlamlı bir fark bulunmamıştır. Bildiğimiz kadarıyla, veteriner hekimlikte AE’ler için bir risk faktörü olarak coğrafyayı değerlendiren çalışmalar eksiktir. Önceki bir çalışmada, CHOP tabanlı protokoller kullanılarak tedavi edilen lenfomalı köpeklerde sağkalım süresinde coğrafi bir fark bulunmasına rağmen, gruplar arasındaki AE sıklığı değerlendirilmemiştir.31 Çalışmamızın bazı kısıtlamaları bulunmaktadır. İlk olarak, retrospektif tasarımı, özellikle gastrointestinal etkiler için AE raporunun detaylarında büyük bir varyasyona neden olmuştur. Birçok alt evre A köpeğe (%43,3), belgelenmiş gastrointestinal bulguları olmamasına rağmen vinkristinden sonra gastrointestinal destekleyici bakım ilaçları verilmiştir. Gastrointestinal bulguların gelişimine katkıda bulunmuş olabilecek ilaçların kullanımına ek olarak bu faktör,26–28 bu popülasyonda vinkristine sekonder gastrointestinal AE’lerin gerçek sıklığının bilinmediği anlamına gelmektedir. Çalışmamızın retrospektif doğası, ilaçların profilaktik olarak mı yoksa semptomatik olarak mı verildiğini doğru bir şekilde belirlemeyi imkansız kılmıştır ve gastrointestinal AE’lerin sıklığını karıştırma potansiyeli nedeniyle ağırlık grupları arasında bir karşılaştırma yapılamamıştır. Retrospektif tasarım aynı zamanda beklenen nadir nötrofil sayısının standardizasyonuna izin vermemiştir ve bu nedenle farklı takip süreleri kullanılmıştır. Çoğu köpeğin (%64,4) vinkristin sonrası CBC’si 7. günde yapılmış olsa da, kemoterapinin farmakokinetik ve farmakodinamik özellikleri arasında farklılıklar vardır32 ve bir köpeğin en düşük nokta (nadir) sayısının gözden kaçmış olması mümkündür. Lenfoma tedavisinin indüksiyon fazında yaygın kullanımı göz önünde bulundurularak, vin-kristin ile aynı anda ya da öncesinde prednizon kullanımına izin verilmiştir. Çalışmamıza dahil edilen sadece 3 köpek halihazırda prednizon ile tedavi edilmemiştir. Bu popülasyonda gözlenen gastrointestinal AE’lerin eş zamanlı prednizon kullanımından kaynaklanmış (veya kötüleşmiş) olması mümkündür. Ayrıca, eş zamanlı prednizon kullanımının nötrofil sayısı üzerinde bir etkisi olması da mümkündür.33 Çalışmamızın bir diğer önemli kısıtlaması da ortalama vinkristin dozunun 0,6 mg/m2 olmasıdır. Vinkristin dozu için bildirilen aralık 0,5 ila 0,75 mg/m2 olmasına rağmen,1 CHOP tabanlı kemoterapi protokolünün bir parçası olarak vinkristin kullanan çoğu çalışma 0,7 mg/m2 başlangıç dozu bildirmektedir.4–6 Sonuç olarak, çalışmamızda bildirilen AE’lerin sıklığı, daha yüksek vinkristin başlangıç dozu kullanılmış olsaydı daha düşük olabilirdi. Çalışmamızdaki vakaları tedarik edenler gibi bazı kurumlar için, tarihsel olarak 0,6 mg/m2 ile başlamak ve tolere edildikçe 0,7 mg/m2’ye yükseltmek gelenekseldi. Ancak, burada bildirilen ciddi hematolojik AE’lerin genel olarak düşük riski göz önüne alındığında, 0,6 mg/m2’den daha yüksek başlangıç dozunun kullanılmasının, aksi takdirde toksisite riski artmayan köpeklerde muhtemelen iyi tolere edileceğini düşünüyoruz. Çalışmamızdaki köpeklerin çoğu (%55) aynı vinkristin dozunu (0,6 mg/m2) almış olsa da, gruplar arasındaki AE sıklığını etkilemiş olabilecek bir dizi doz dahil edilmiştir. Sadece 0,6 mg/m2 alan köpekler dikkate alındığında, nötropeni sıklığında anlamlı bir fark bulunmamıştır. Ancak, analizimizdeki köpek sayısının azlığı göz önüne alındığında, tip 2 hata olasılığı bulunmaktadır. Tüm köpekler dikkate alındığında bile, genel nötropeni sıklığı düşüktür (%12,3) ve tip 2 hata hala mümkündür. Sonuç olarak, ≤0,6 mg/m2 dozunda kullanılan vinkristin küçük köpeklerde miyelosupresyon riskinde artışa yol açmamaktadır. Profilaktik gastrointestinal ilaçlar kullanılmadan, yeni teşhis edilmiş çok merkezli lenfomalı köpek popülasyonunda daha yüksek vinkristin başlangıç dozunun AE’lerini değerlendiren prospektif bir çalışma, bulgularımızı doğrulamak ve ağırlık grupları arasında gastrointestinal AE’lerin sıklığını daha doğru bir şekilde bildirmek için yararlı olacaktır. TEŞEKKÜRLER ÇIKAR ÇATIŞMASI BEYANI ENDİKASYON DIŞI ANTİMİKROBİYAL BEYANI KURUMSAL HAYVAN BAKIM VE KULLANIM KOMİTESİ (IACUC) VEYA DİĞER ONAY BEYANI İNSAN ETİĞİ ONAY BEYANI ORCID |
KAYNAKÇA
|