1Veteriner Hekimliği ve Cerrahisi Bölümü, Missouri Üniversitesi Veteriner Hekimliği Fakültesi, Columbia, Missouri
2Veteriner Klinik Bilimleri Bölümü, Louisiana Eyalet Üniversitesi Veteriner Hekimliği Fakültesi, Baton Rouge, Louisiana
İletişim Dr. Brian K. Flesner, Missouri Üniversitesi Veteriner Hekimliği Fakültesi, Columbia, MO 65211. E-posta: flesnerb@missouri.edu
Güncel adres Kim Menard, 503 E Sonterra Boulevard Suite 102, San Antonio, TX 78258.
5-Fluorourasil (5-FU) insan baş ve boyun kanseri ve diğer epitelyal neoplazmların tedavisinde kombinasyon kemoterapi protokolleri ile birlikte kullanılmaktadır. Fakat, bu ilacın veteriner onkolojide kullanımını ele alan literatürün azlığı, muhtemelen hem köpeklerde hem de kedilerde, ağırlıklı olarak insan kremlerinin yutulmasından kaynaklanan ölümcül nörotoksisite raporlarından dolayıdır. Bu retrospektif çalışmanın birincil amacı, köpek karsinomlarında eş zamanlı 5-FU ve karboplatinin güvenli olup olmadığını incelemektir. İkincil olarak, tedavi edilen köpeklerde genel yanıt oranını dikkate alarak kombinasyonun etkinliğini araştırmaktır. Her iki ajanla tedavi edilen köpeklerin tıbbi kayıtları 2007’den 2017’ye kadar tarandı; 24 köpek dahil edilme kriterlerini karşıladı. Karboplatin dozajları 180 ila 250 mg/m2 (ortalama 200 mg/m2) arasında değişmekteydi; 5- FU dozajı 150 mg/m2 idi. On dört köpekte Grade I’den asemptomatik Grade IV’e kadar değişen miyelosupresyon görüldü; trombositopeni nötropeniden daha yaygındı. Gastrointestinal rahatsızlıklar nadirdi; sadece yedi köpekte Grade I veya II bulantı, kusma veya ishal görüldü. Hiçbir vaka yukarıdaki toksisitelerden herhangi biri nedeniyle hastaneye yatırılmamıştır. Bir köpekte otit ve 5-FU nörotoksisitesi arasında ayrım yapılamayan bir ataksi vakası görülmüştür. Bu protokol iyi tolere edilmiştir. Ağır hastalık ortamında yanıt oranı %43’tür (üç tam yanıt, üç kısmi yanıt). Köpek karsinomlarının tedavisinde hem bu kombinasyon protokolünün hem de potansiyel olarak 5-FU’nun diğer platin ajanlarla prospektif şekilde analiz edilmesi gerekmektedir.
ANAHTAR KELİMELER
karboplatin, karsinom, köpekler, florourasil
1 | GİRİŞ
5-Florourasil (5-FU), orijinal olarak 1950’lerde Heidelberger ve arkadaşları tarafından sentezlenen antimetabolit bir kemoterapi ajanıdır.1 Etki mekanizması timidilat sentaz inhibisyonudur, ancak ilacın metabolitleri aynı zamanda hem RNA hem de DNA’ya katılır. Bunun sonucunda DNA’ya dahil olması DNA iplikçik kırılmalarına ve potansiyel olarak apoptoza yol açar .1,2 5-FU’nun %85 kadarı dihidropirimidin dehidrogenaz (DPD) tarafından enzimatik olarak inaktive edilir. Yetersiz DPD, insan hastalarda nörotoksisitenin artmasına neden olabilir1 ve bağırsak mukozasındaki yüksek DPD seviyeleri, kararsız biyoyararlanım nedeniyle oral yoldan uygulamayı engeller.2 5-FU, veteriner onkoloji hastalarında nadiren kullanılır.3 Bu durum, ilaçla ilgili deneyim eksikliği ile ilgili olabilir, ancak kullanımın az olması, daha önce kazara maruz kalmayla ilişkili ölümcül toksisite raporlarından ötürü olması daha muhtemeldir. 5-FU’nun yutulması hem kedi hem de köpeklerde ölümcül nörotoksisitelerle sonuçlanmıştır.4–6
Bu durum veteriner hastalarda DPD konsantrasyonlarının düşük olmasıyla ilişkilendirilebilir; kedilerin yaklaşık %25’inde ve köpeklerin %14’ünde urasil:dihidrourasil konsantrasyonları insanlarda düşük DPD ile ilişkilendirilen değerden daha yüksektir.7,8
5-FU’nun nörotoksisite potansiyeli veteriner onkolojide yaygın kullanımını muhtemelen engellemiş olsa da, bu tedavi küçük çaplı köpek anal kese adenokarsinomu hastalarında incelenmiştir.9 Ayrıca, 5-FU köpek karsinomlarında daktinomisin ve siklofosfamid ile kombinasyon protokolünde kullanılmıştır.10 5-FU 1 hafta içinde (8. ve 15. günlerde) iki kez tekrarlanmış ve köpeklerin %40’ında nörotoksisite görülmüştür. Başka bir karsinom alt tipinde, nazal adenokarsinomlu 15 köpek haftada bir kez 5-FU ve siklofosfamid ile tedavi edilmiştir. Toksisite rapor edilmemiştir.11 5-FU ayrıca tam olarak rezeke edilmemiş yumuşak doku sarkomlarında intralezyonel olarak kullanılmıştır; tedavi edilen altı köpekte nörotoksisite görülmemiştir.12 5-FU’nun tek bir ajan olarak kullanılması insan onkolojisinde pek de umut vaat edici olmamıştır.
Bununla birlikte, diğer kemoterapi ajanlarıyla, özellikle platin ajanlarla sinerjizm,13-15 tek ajan tedavisine kıyasla daha yüksek klinik etki göstermiştir ve günümüzde baş-boyun ve gastrointestinal epitelyal tümörler de dahil olmak üzere birçok insan karsinomunda standart tedavi yöntemidir.16-20 Bunun nedeni fluorourasilin timidilat sentaz inhibisyonu yoluyla DNA onarımını azaltması ve DNA hasarını artırması,21,22 ve timidilat sentazın platin ajanlar, özellikle de oksaliplatin tarafından down-regüle edilmesidir.23
Karboplatin, uygulama kolaylığı ve özellikle nefrotoksisite ve emezis olmak üzere düşük yan etki oranı nedeniyle veteriner onkolojide kullanılan ana platin ajandır.3 Köpek osteosarkomu için standart tedavi olarak kabul edilmektedir24 ve köpek tonsiller skuamöz hücreli karsinomunda (SCC) non-steroid anti-inflamatuarlar ve diğer kemoterapi ajanları ile birlikte kullanılmıştır.25,26 Kombinasyon tedavisi, direnç mekanizmalarının üstesinden gelerek ve toksisite şemalarını ikiye ayırarak tek ajan tedavisinden daha başarılı olma eğilimindedir.3 Kombinasyon şemaları diğer köpek neoplazmlarının, özellikle de lenfomanın tedavisinde doğal olarak önemli olsa da, karsinomlar hakkında çok az bilgi mevcuttur. Karsinomlu bazı köpeklerde (tiroid ve anal kese karsinomu) toceranib ile kombinasyon halinde karboplatin kullanılan yeni prospektif bir çalışmada, doz sınırlayıcı toksisite olarak miyelo supresyon ile klinik faydasağlanmıştır.27 İnsan karsinomlarında 5-FU ve platin kombinasyonlarının sıkça kullanılmasına rağmen, bu ajanların birlikte kullanımı veteriner onkolojisinde daha önce rapor edilmemiştir.
Bu çalışmanın birincil amacı, karsinomlu köpeklerde 5-FU ve karboplatinin birlikte uygulanmasının güvenli olup olmadığını göstermektir. Bu çalışmanın retrospektif doğası nedeniyle, tolere edilebilir maksimum doz birincil hedef değildi ve bu nedenle hasta popülasyonumuzda doz eskalasyonu takip edilmedi. Klinik fayda ve sağkalım avantajlarının değerlendirilmesi bu çalışmanın birincil hedefleri değildi, ancak kombinasyon yöntemi ile tedavi edilen köpeklerde yanıt oranı ve genel sağkalım temelinde değerlendirilmiştir.
2 | MATERYAL VE METOD
Missouri Üniversitesi Veteriner Hekimliği Fakültesi Veteriner Sağlık Merkezi (MU- VHC) ve Louisiana Eyalet Üniversitesi Veteriner Hekimliği Hastanesi’nde (LSU-VTH) aynı anda hem 5-FU hem de karboplatin alan köpeklerin tıbbi kayıtları incelenmiştir. Yirmi dört hasta, sitoloji veya histopatoloji yoluyla kurul sertifikalı patolog tarafından konulan epitelyal neoplazm tanısı ve eş zamanlı 5-FU ve karboplatin uygulaması için dahil edilme kriterlerini karşılamıştır. Vakalardan alınan veriler arasında tanı sırasındaki yaş ve ağırlık, cinsiyet, ırk ve epitelyal neoplazm türü yer almıştır. Mevcut olduğunda hastalığın evresi de belgelenmiştir.
Karboplatin ve 5-FU tarif edilen protokol uyarınca intravenöz olarak eş zamanlı uygulanmıştır (Tablo 1). Üç hastada karboplatinin bir veya daha fazla dozu intrakaviter olarak uygulanırken 5-FU eş zamanlı olarak intravenöz olarak uygulanmıştır. Karboplatin intrakaviter uygulama için seyreltilmemiştir. Malign efüzyon intrakaviter uygulamadan önce klinik bulgulara göre uygun şekilde boşaltılmıştır. Her iki ajanın uygulama yolu ve dozu kaydedilmiştir.
VCOG AE kriterlerine göre derecelendirilen toplam doz sayısı ve müteakip yan etkiler belgelenmiştir.28 Tam kan sayımları (CBC) tedaviden 7, 14 ve 21 gün sonra tekrarlanmıştır; müteakip CBC’ler hasta en düşük değere ulaştığında yapılmıştır. Böbrek profilleri ek 5-FU ve karboplatin dozlarından önce gerçekleştirilmiştir. Nörotoksisite de dahil olmak üzere benzersiz toksisiteler, tıbbi kayıtlar ve iletişim günlükleri incelendikten sonra kaydedilmiştir. Tedavi yanıtı verileri Veteriner Onkoloji Grubu’nun solid tümörler için RECIST kriterlerine veya karsinomatozis hastalarında efüzyonun rezolüsyonuna göre belirlenmiştir.
Bunu yaparken tümörün konumuna bağlı olarak fiziksel muayene ve kumpas veya görüntüleme kullanılarak yapılan ölçümler esas alınmıştır. Ameliyat yoluyla lokorejyonel kontrol (hastalık bulgusuna rastlanmadı, NED) uygulanan köpekler hastalık yanıtı açısından değil nüks açısından gözlem altında tutulmuştur. Ağır hastalık ortamında, tam yanıt (CR) tüm klinik ve görüntüleme temelli hastalık kanıtlarının ortadan kalkması, kısmi yanıt (PR) yeni lezyon olmaksızın tümör çapında en az %30 azalma, stabil hastalık (SD) yeni lezyon olmaksızın tümör çapında – %30 ile +%20 arasında fark ve progresif hastalık (PD) tümör çapında %20’den fazla artış veya yeni lezyonların gelişmesi şeklinde tanımlanmıştır. Genel yanıt oranı (ORR) CR + PR olarak tanımlanmıştır. Çalışmaya dahil edilen tüm hastalar için progresyona kadar geçen süre, ilk kombinasyon kemoterapi tedavisinden hastalığın progresyon tarihine kadar geçen gün şeklinde hesaplanmıştır . Sağkalım süresi, ilk kombinasyon kemoterapi tedavisinden karsinom nedeniyle ölüm tarihine kadar geçen süre olarak gün cinsinden hesaplanmıştır. Çalışma süresinin sonunda hayatta olan, takibi kaybedilen veya karsinomlarıyla ilgisi olmayan herhangi bir ölüm nedeni olan tüm hastalar analizden sansürlenmiştir. Hastalık progresyonuna kadar geçen ortalama süre ve ortalama sağkalım süresi Kaplan- Meier çarpım sınırı hesaplayıcısıyla hesaplanmıştır. Hiçbir grup karşılaştırılmadığı için bu çalışmadaki istatistikler tamamen açıklayıcıdır.
3 | SONUÇLAR
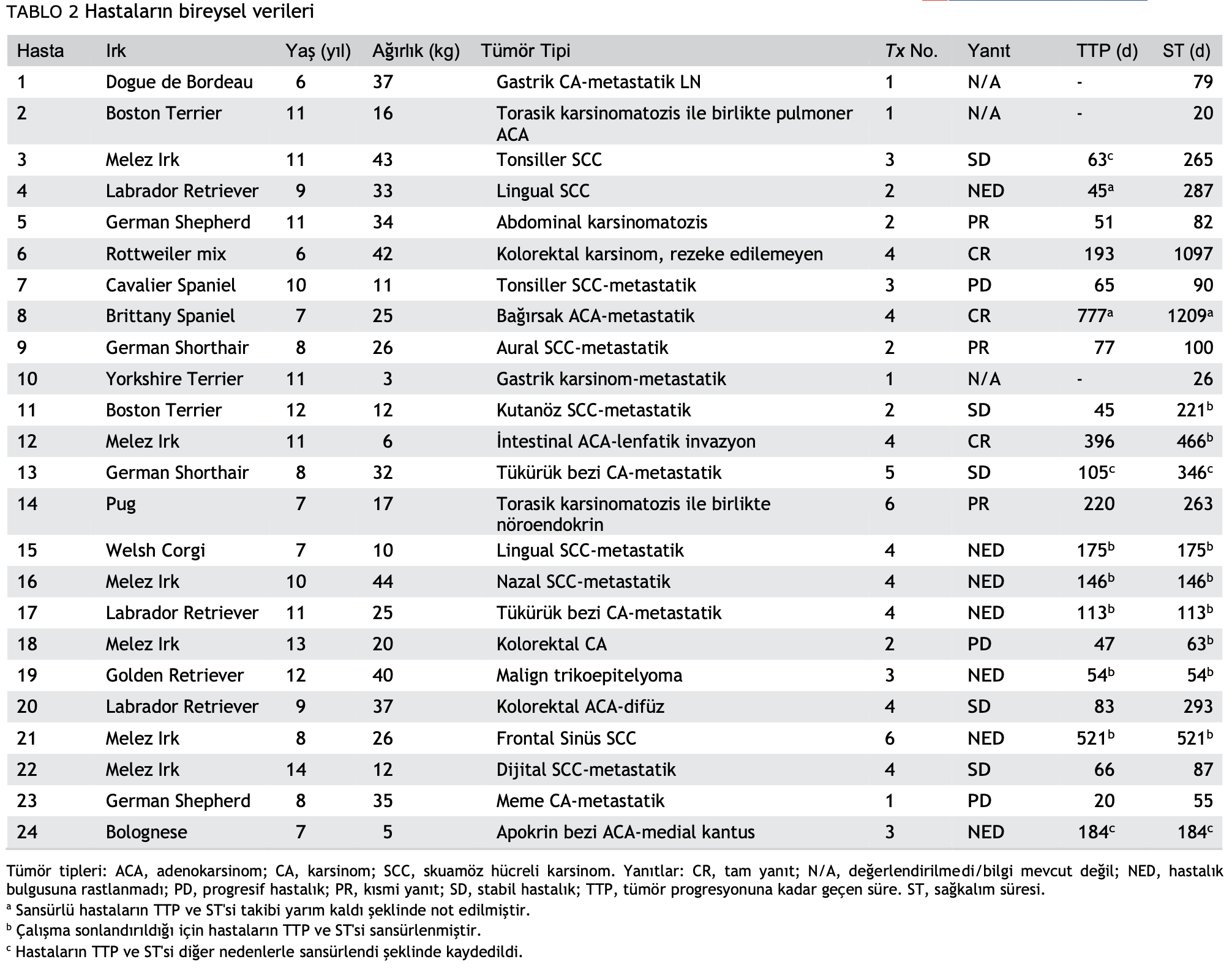
Yirmi dört köpek çalışmaya dahil edilme kriterlerini karşılamıştır (Tablo 2). Tüm hastaların ortalama yaşı 9,5 idi (dağılım: 6-14 yaş) ve ortalama vücut ağırlığı 25,5 kg (dağılım: 3-44 kg) idi. 14 erkek köpek (3 kısırlaştırlmamış ve 11 kısırlaştırılmış) ve 10 kısırlaştırılmış dişi köpek vardı. On dört farklı ırk mevcuttu ve en yaygın olanı melez ırktı (n = 6), bunu Labrador Retriever (n = 3), Boston Terrier (n = 2), German Shorthair (n = 2) ve German Shepherd (n = 2) izledi. Tüm köpeklere karsinom teşhisi konulmuştur: yedi köpekte gastrointestinal karsinom ve dokuz köpekte farklı lokalizasyonlarda SCC vardı. Üç köpeğe karsinomatozis teşhisi konmuştur. On beş köpekte bölgesel veya uzak lenf düğümlerine metastaz vardı.
Kombinasyon tedavisinden önce, altı köpek kemoterapi ve/veya NSAİİ ile ön tedaviye tabi tutulmuştur. İkisi tek ajan karboplatin, biri mitoksantron ve karboplatin içeren elektrokemoterapi, biri toceranib ve ardından karboplatin ve ikisi NSAİİ (karprofen ve piroksikam) ile tedavi edilmiştir.
Başlangıç karboplatin dozları bir köpek hariç hepsinde 200 mg/m2 idi; bir köpek 250 mg/m2 karboplatin IV ile tedavi edildi. Bu köpekte doz azaltımı yapılmasına gerek kalmamıştır. 5-FU dozu tüm köpekler için 150 mg/m2 idi. Protokolde alınan toplam dozların ortalama sayısı 3’tü (aralık: 1-6 doz). Sadece iki köpek eşlik eden ilaçlar (gastroprotektanlar ve destekleyici ilaçlar haricinde) almıştır. Her iki köpek de piroksikam almıştır.
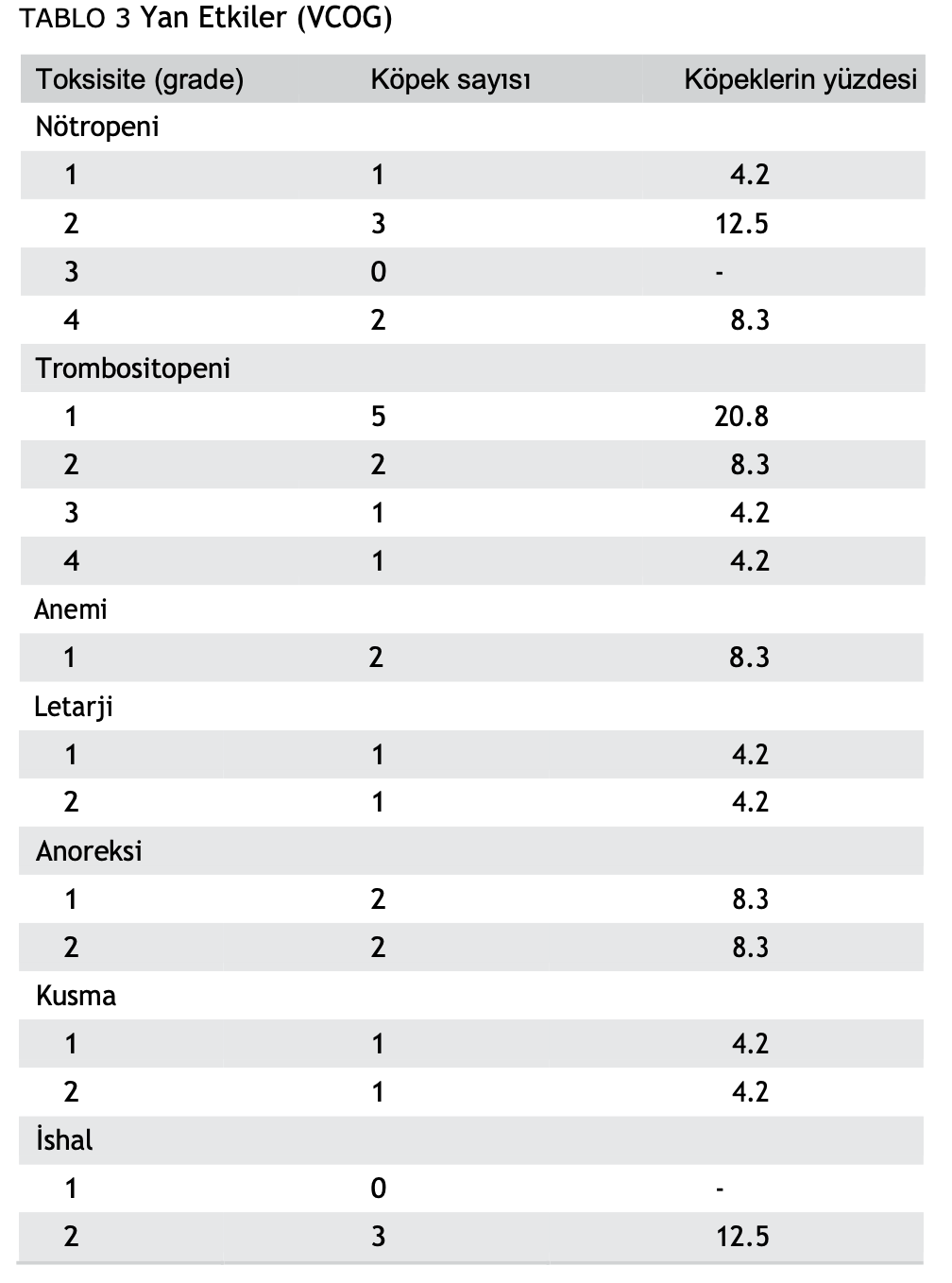
En sık görülen yan etki 14 köpekte görülen miyelosupresyon olmuştur (Tablo 3). Dokuz köpekte (%37,5) trombositopeni görülmüş olup çoğunluğu VCOG Grade I veya II’dir. Nötropeni altı köpekte (%25,0) görülmüş olup çoğunluğu VCOG Grade II’dir. İki köpekte anemi (%8,3) gelişmiştir ve her ikisi de VCOG Grade I’dir. İki köpekte eş zamanlı nötropeni ve trombositopeni, bir köpekte ise eş zamanlı anemi ve trombositopeni görülmüştür. Hiçbir hastada hastaneye yatış gerekmemiştir. Bir hastada tedaviden 14 gün sonra gecikmeli şekilde en düşük seviye görüldü; diğer tüm nötropeni atakları tedaviden 7 gün sonraydı. Sadece bir hastada doz azaltımı gerekmiştir.
Bu hastada asemptomatik Grade IV nötropeni görüldü, ancak karboplatin dozunun %20 azaltılmasıyla başka atak olmadı. Hiçbir hastada planlı doz geciktirme gerekmemiştir.
Yedi köpekte (%29,2) hafif gastrointestinal rahatsızlık meydana gelmiş, bu köpeklerde iştah azalması, kusma ve/veya VCOG Grade I veya II ishal görülmüştür. İki köpekte ishalle eş zamanlı kusma veya anoreksi görülmüştür. Köpeklerin hiçbirinde gastrointestinal yan etkiler nedeniyle hastaneye yatış gerekmemiştir. Kolorektal karsinomu olan bir hastada alanin aminotransferaz ve azotemi artışı görüldü; PD nedeniyle kemoterapi kesildi. ALT ve böbrek değerlerindeki artışın altında yatan neden, büyük olasılıkla hastalığın ilerlemesiyle ilgili olabileceğinden şüphelenildiği için araştırılmamıştır. Medial kantusta apokrin bez adenokarsinomu olan bir hastada kombinasyon tedavisi sırasında aralıklı olarak Grade II kusma, diyare ve letarji görülmüştür. Gastrointestinal rahatsızlık sırasında bir pre-renal azotemi de gelişti, ancak destekleyici tedaviyle 1 hafta içinde düzeldi. Köpek, üç doz 5-FU ve karboplatin kombinasyonundan sonra tek ajan karboplatin protokolüne geçirilmiştir. Köpekte üçüncü tek ajan karboplatin dozundan sonra (toplam altı doz karboplatin) pankreatit gelişti ve kemoterapi almayı bıraktı. Aural SCC’li bir hastada iki dozdan sonra ataksi atağı görülmüştür; ancak altta yatan etkenin sekonder otit mi yoksa nörotoksisite mi olduğu ayırt edilememiştir.kop
Bu çalışmanın birincil amacı tolere edilebilirlik olsa da, birkaç köpekte tümör yanıtı elde edilmiştir. Ağır hastalığı olan köpekler (n = 14) değerlendirildiğinde, %42,8’lik bir ORR için üç köpekte CR ve üç köpekte PR görülmüştür. Altı köpeğin stabil hastalığa sahip olduğu ve ikisinde PD olduğu bildirilmiştir. Yedi köpek mikroskobik olduğu varsayılan ortamda tedavi edilmiştir; ameliyattan sonra NED görülmüş ancak önceden metastatik yayılım veya lenfatik invazyon olduğu belgelenmiştir.
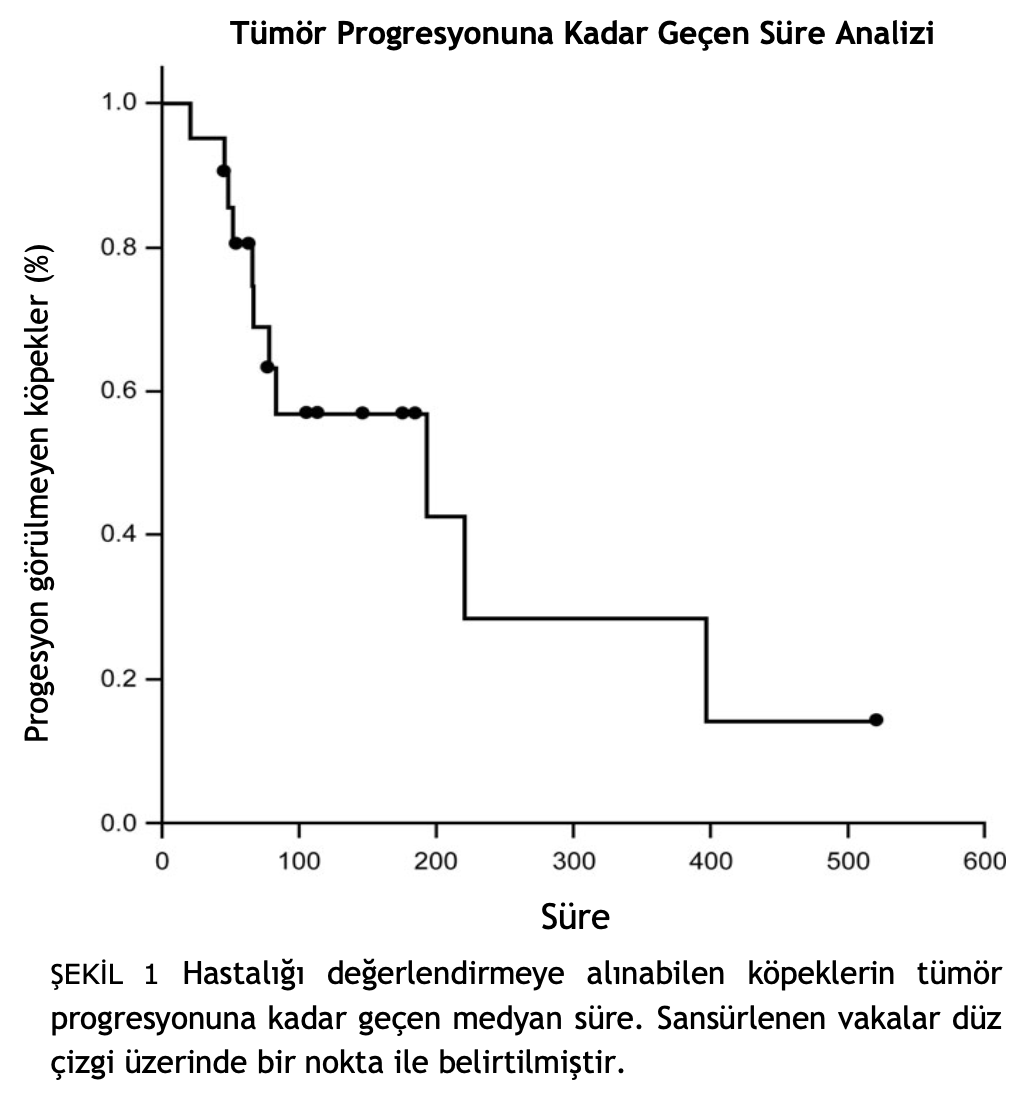
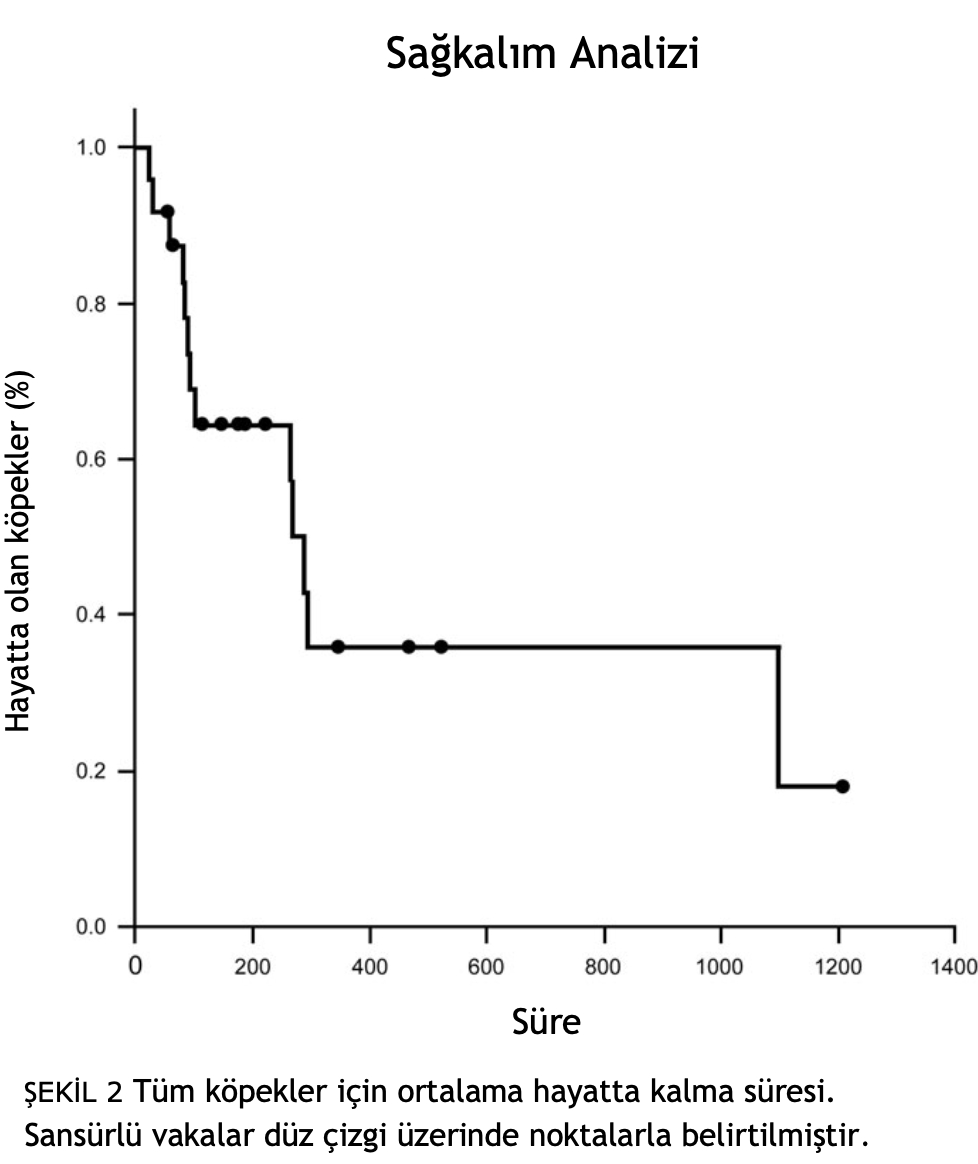
CR olan üç köpeğe kolorektal (n = 1) ve intestinal adeno-karsinom (n = 2) tanısı konmuştur; bu yanıtlar sırasıyla 193, 396 ve 777 gün sürmüştür. PR’ler 51, 77 ve 220 gün sürmüştür. Değerlendirmeye alınabilen köpekler için progresyona kadar geçen ortalama süre (Şekil 1) 193 gündü (aralık: 20-777 gün). Değerlendirmeye alınabilen 21 köpekten 10’u analizden sansürlendi: 4’ü tedaviye alındığında hastalıksızdı, 2’sinin takibi kaybedildi, 3’ü sahiplerinin isteği üzerine çalışmadan çıkarıldı ve 1’inde metastatik melanom olduğu doğrulandı. Diğer üç köpek hastalık yanıtı açısından değerlendirilememiştir. Tedavi edilen tüm köpekler için ortalama sağkalım süresi (Şekil 2) 287 gündü (aralık: 20-1209 gün). On bir köpek analizden sansürlenmiştir: altısı başvuru sırasında hala hayattaydı, dördü NED sonucu takipten çıkmıştı ve biri de doğrulanmış metastatik melanom nedeniyle ölmüştü.
4 | TARTIŞMA
Bu çalışmanın birincil amacı, karsinomlu köpeklerde eş zamanlı 5- FU ve karboplatin kemoterapisinin uygulanmasının tolere edilebilirliğini değerlendirmekti. Klinik fayda ve sağkalım avantajının değerlendirilmesi çalışmanın birincil amacı olmamakla birlikte, bu kombinasyon yaklaşımıyla tedavi edilen hastaların birçoğunda yanıtlar kaydedilmiştir.
Platin ajanlar veteriner hastalarda yaygın olarak kullanılırken, muhtemelen rapor edilen nörotoksisitesiyle ilgili endişeler nedeniyle 5-FU kullanımına ilişkin az sayıda rapor bulunmaktadır.4-6 Köpeklerde ölümcül nörolojik toksisite en sık ilacın topikal formu tüketildikten sonra rapor edilmiştir.6 Köpeklerde tek tip ölümcül nörotoksisiteye yol açtığı bildirilen dozajlar >40 mg/kg’dır; ancak 5 mg/kg kadar az bir miktar bile bazı hastalarda klinik semptomlara neden olmuştur.4
Bu hastalardaki nörotoksisite mekanizması tam olarak anlaşılamamış olsa da, düşük DPD seviyelerinin insanlarda yüksek 5-FU toksisitesine katkıda bulunduğu düşünülmektedir.1 Daha önce belirtildiği gibi, köpek ve kedilerin %25’inden az bir kısmında urasil:dihidrourasil konsantrasyonları insanlarda düşük DPD ile ilişkili değerden daha yüksektir.7,8 Bu çalışmada, köpeklere intravenöz olarak 150 mg/m2 5- FU uygulanmıştır; bu doz, nörotoksisite yaşayan köpeklerin aldığı toksik seviyelerle karşılaştırılabilir ve köpeklerde nörotoksisite görülen önceki raporlarla karşılaştırılabilir .10 Ancak, doz aralığımız daha önce bahsedilen çalışmalardan farklıydı. Çalışma popülasyonumuzda kesin olarak 5-FU’ya atfedilebilecek herhangi bir nörotoksisite kaydedilmemiştir; ancak, aural karsinomu olan bir köpekte tümöre sekonder otitis media veya 5-FU toksisitesi ile ilişkili olabilecek ataksi olduğu rapor edilmiştir. Bu hastada ataksinin altında yatan nedeni araştırmak için ileri tanı yöntemleri uygulanmamış ve köpeğin nörolojik bulguları oral antimikrobiyal tedavi ile düzelmiştir. 5-FU tedavisine tekrar başlanmadı; köpekte PH gelişmeye devam etti ve ötenazi uygulandı.
Sağkalım açısından faydaları araştırmak çalışmamızın birincil amacı olmasa da, birkaç köpekte bazı yanıtlar elde edilmiştir. Ağır hastalığı olan 14 köpekte %43 oranında ORR görülmüştür. Yedi köpekte daha NED vardı; bu nedenle yanıt değerlendirmesine dahil edilmediler . İnsanlarda, 5-FU ve platin ilaçlarla kombinasyon protokolleri baş ve boyun, nazofarengeal ve kolorektal karsinomlu hastalar için standart tedavi haline gelmiştir.16-20 Ancak, bu protokoller veteriner hekimlikte yaygın olarak kullanılmamaktadır. Bu yaklaşımla, timidilat sentazın florourasil tarafından inhibe edilmesi ve bunun sonucunda DNAonarımının bozulması ve müteakip DNA hasarı nedeniyle sinerjizm görülmektedir .21 Timidilat sentazın platin ajanlar tarafından downregülasyonu bu iki ajanın sinerjisine muhtemelen katkıda bulunmaktadır.23 Dozaj şemamız, sisplatine dirençli insan SCC’sinin florourasil tedavisinden sonra sisplatine yeniden duyarlı hale geldiği bir in vitro çalışmadan destek almaktadır.22 Çalışma popülasyonumuzda bu protokolle kaydedilen tolere edilebilirlik nedeniyle, veteriner hastalarda yanıt oranını ve sağkalım faydasını daha fazla araştırmak için ek çalışmalar yapılması gerekebilir.
Bu retrospektif çalışmanın birincil amacı 5-FU ve karboplatinin birlikte uygulanmasının tolere edilebilirliğini araştırmak olduğundan, tolere edilebilir maksimum dozun belirlenmesi çalışmanın son noktası değildi. Köpekler 5-FU ve karboplatin kombinasyonunu yönetilebilir yan etkilerle iyi tolere etmiştir. Bildirilen VCOG yan etkilerinin çoğu Grade 1 ve 2’dir ve hiçbir köpeğin hastaneye yatırılması gerekmemiştir. Bulgularımıza dayanarak, doz artışını araştırmak ve köpek hastalarımız için tolere edilebilir maksimum dozu belirlemek için ek çalışmalar yapılması gerekebilir.
Üçüncü nesil platin olan oksaliplatin, insanlarda kolorektal kanser tedavisinde kullanılmak üzere FDA onaylıdır.1 Özellikle 5-FU ile birlikte kullanıldığında diğer platin ilaçlara dirençli kolorektal kanser tedavisinde daha etkili olduğu bildirilmektedir.17,23 Oksaliplatin, klinik öncesi değerlendirme sırasında kardiyo-toksik ölüm nedeniyle daha önce veteriner hekimlikte kullanılmamıştır. Bununla birlikte, maligniteleri doğrulanmış köpeklerde yapılan yeni bir Faz I klinik çalışma, oksaliplatinin 140 mg/m2’lik dozlara kadar güvenle uygulanabileceğini göstermiştir.*
*Klahn S, Dervisis N, Gustafson D, Fagan E, Abbott J, Borgarelli M. Köpek kanser hastalarında oksaliplatinin Faz I klinik çalışması. 26-28 Ekim 2017 Veteriner Kanser Derneği Yıllık Konferansı’nda sunulan özet.
Oksaliplatinin insanlarda diğer platin ajanlara karşı kanıtlanmış üstünlüğü nedeniyle, oksaliplatin ve 5-FU kombinasyonu köpek karsinomları için umut verici bir tedavi seçeneği olabilir.
Bu çalışmanın kısıtlamaları temel olarak retrospektif doğası ve küçük örneklem büyüklüğünden kaynaklanmaktadır . Hastaların çoğu aynı dozları ve tedavi programını alırken, birkaç köpeğe bir kemoterapi ajanı intrakaviter , diğerleri intravenöz olarak uygulanmıştır . Malign efüzyonlar için karboplatin veya mitoksantron kullanılan küçük bir retrospektif çalışmada, tedavi edilen köpeklerde sağkalımın arttığı kaydedilmiştir.30 Yazarlar, tümör kapiller maruziyetini gösteren farmakolojik çalışmalara atıfta bulunarak, intra venöz dozlama ile eşdeğer doza ulaştıklarını belirtmişlerdir .30 Bizim çalışmamızda, efüzyonlu köpek sayısının az olması nedeniyle, intrakaviter ve intravenöz tedavi edilen köpekler arasında yanıt karşılaştırması yapamadık. İntrakaviter kemoterapi ile tedavi edilen üç köpek tedaviyi iyi tolere etti; ancak iki köpek ikinci tur kemoterapiden önce hastalıklarına yenik düştü. Üçüncü köpekte, tekrarlanan hızlı torasik taramaya göre efüzyonda en azından kısmi rezolüsyon ve solunum karakterinde iyileşme ile belirtilen yaşam kalitesinde iyileşme vardı; protokolün başlamasından 220 gün sonra hastalık ilerledi.
İki köpek tipik dört doz yerine altı doz eş zamanlı tedavi almıştır. Bu durum, ilgili klinisyenin takdirine bağlıydı. T edavi aralıkları standardize edilmiş olsa da takip süreci gözlemlenmemiştir. Hastalarda tek tip yeniden kontroller veya tekrar evreleme yapılmamıştır; bu durum yanıt oranlarında yanlışlıklara yol açabilir. Genel örneklem büyüklüğü küçüktü ve tedavi edilen tüm hastalar karsinom tanısıyla sınırlıyken, birkaç farklı karsinom türü vardı, bu da istatistiksel karşılaştırmaları zorlaştırıyordu. İdeal olarak, spesifik karsinom tanıları olan vakaları içeren ve mevcut bakım standardına kıyasla yanıtı değerlendiren prospektif bir çalışma yapılmalıdır.
Özet olarak, çalışmamız hem 5-FU hem de karboplatin kullanan kombinasyon protokolünün köpeklerde iyi tolere edildiğini ve özellikle gastrointestinal formlar olmak üzere çeşitli karsinomlar için yeniden uygulanabilir bir tedavi protokolü olduğunu göstermiştir. Bu sonuçlara dayanarak, 5-FU ve karboplatin kombinasyonunun doz artışını değerlendirmek için ek çalışmalar yapılması gerekmektedir. Kombinatoryal 5-FU köpek karsinomlarında diğer platin ajanlarla, özellikle sisplatin ve oksaliplatin ile birlikte de kullanılabilir. Eşzamanlı olarak uygulanan bu ilaçların biyolojik etkinliği, burada sunulan verilere dayanarak açıktır. Bununla birlikte, daha geniş bir köpek kohortunda tedaviye yanıtı ve potansiyel toksisiteyi daha fazla değerlendirmek için prospektif çalışmalara ihtiyaç vardır.
TEŞEKKÜRLER
Yazarlar, MU ve LSU’daki destek veren onkoloji ekiplerine bu
projedeki tüm yardımları için teşekkür eder.
Çıkar Çatışması Beyanı
Yazarlar herhangi bir çıkar çatışması beyan etmemiştir.
ORCID
Brian K. Flesner
http://orcid.org/0000-0002-2459-705
KAYNAKÇA
- Chabner B, Longo DL. Cancer Chemotherapy and Biotherapy: Principles and Practice. 5th ed. Philadelphia, PA: Wolters Kluwer/Lippincott Wil- liams & Wilkins Health;2011.
- DeVitaVT,LawrenceTS,RosenbergSA.DeVita,Hellman,andRosen- berg’s Cancer: Principles & Practice of Oncology. 9th ed. Philadelphia, PA: Wolters Kluwer Health/Lippincott Williams & Wilkins; 2011.
- Withrow SJ, Vail DM, Page RL. Withrow & MacEwen’s Small Animal Clinical Oncology. 5th ed. St. Louis, MO: Elsevier Saunders; 2013.
- SayreRS,BarrJW,BaileyEM.Accidentalandexperimentallyinduced 5-fluorouracil toxicity in dogs. J Vet Emerg Crit Care. 2012;22: 545- 549.
- Dorman DC, Coddington KA, Richardson RC. 5-Fluorouracil toxicosis in the dog. J Vet Intern Med. 1990;4:254-257.
- Snavely NR, Snavely DA, Wilson BB. Toxic effects of fluorouracil cream ingestion on dogs and cats. Arch Dermatol. 2010;146: 1195- 1196.
- Saba CF, Schmiedt CW, Freeman KG, Edwards GL. Indirect assess- ment of dihydropyrimidine dehydrogenase activity in cats. Vet Comp Oncol. 2013;11:265-271.
- Schmiedt CW, Saba CF, Freeman KG, Edwards GL. Assessment of plasma uracil-to-dihydrouracil concentration ratio as an indicator of dihydropyrimidine dehydrogenase activity in clinically normal dogs and dogs with neoplasia or renal insufficiency. Am J Vet Res. 2012;73: 119-124.
- Bennett PF, DeNicola DB, Bonney P, Glickman NW, Knapp DW. Canine anal sac adenocarcinomas: clinical presentation and response to therapy. J Vet Intern Med. 2002;16:100-104.
- HammerAS,CarothersMA,HarrisCL,etal.Unexpectedneurotoxicity in dogs receiving a cyclophosphamide, dactinomycin, and 5- fluorouracil chemotherapy protocol. J Vet Intern Med. 1994;8: 240- 243.
- Henry CJ, Brewer WG Jr, Tyler JW, et al. Survival in dogs with nasal adenocarcinoma: 64 cases (1981-1995). J Vet Intern Med. 1998;12: 436-439.
- MarconatoL,ComastriS,LorenzoMR,AbramoF,BettiniG.Postsurgi- cal intra-incisional 5-fluorouracil in dogs with incompletely resected, extremity malignant spindle cell tumours: a pilot study. Vet Comp Oncol. 2007;5:239-249.
- JohnstonPG,GeoffreyF,DrakeJ,VoellerD,GremJL,AllegraCJ.The cellular interaction of 5-fluorouracil and cisplatin in a human colon car- cinoma cell line. Eur J Cancer. 1996;32a:2148-2154.
- Forastiere AA, Natale RB, Takasugi BJ, Goren MP, Vogel WC, Kudla- Hatch V. A phase I-II trial of carboplatin and 5-fluorouracil com- bination chemotherapy in advanced carcinoma of the head and neck. J Clin Oncol. 1987;5:190-196.
- ForastiereAA,MetchB,SchullerDE,etal.Randomizedcomparisonof cisplatin plus fluorouracil and carboplatin plus fluorouracil versus methotrexate in advanced squamous-cell carcinoma of the head and neck: a Southwest Oncology Group Study. J Clin Oncol. 1992;10: 1245-1251.
- IqbalA,GeorgeTJ.Randomizedclinicaltrialsincolonandrectalcan- cer. Surg Oncol Clin N Am. 2017;26:689-704.
- AndreT,BoniC,NavarroM,etal.Improvedoverallsurvivalwithoxali- platin, fluorouracil, and leucovorin as adjuvant treatment in stage II or III colon cancer in the MOSAIC trial. J Clin Oncol. 2009;27:3109-3116.
- Meyers BM, Cosby R, Quereshy F, Jonker D. Adjuvant chemotherapy for stage II and III colon cancer following complete resection: a cancer care Ontario systematic review. Clin Oncol (R Coll Radiol). 2017;29: 459-465.
ShapiroLQ,ShermanEJ,RiazN,etal.Efficacyofconcurrentcetuxi- mab vs. 5-fluorouracil/carboplatin or high-dose cisplatin with intensity-modulated radiation therapy (IMRT) for locally-advanced head and neck cancer (LAHNSCC). Oral Oncol. 2014;50:947-955.
20. Kua VF, Ismail F, Chee Ee Phua V, Aslan NM. Carboplatin/5- fluorouracil as an alternative to cisplatin/5-fluorouracil for metastatic and recurrent head and neck squamous cell carcinoma and nasopha- ryngeal carcinoma. Asian Pac J Cancer Prev. 2013;14:1121-1126.
21.Wilson PM, Danenberg PV, Johnston PG, Lenz HJ, Ladner RD. Stand- ing the test of time: targeting thymidylate biosynthesis in cancer ther- apy. Nat Rev Clin Oncol. 2014;11:282-298.
22.Esaki T, Nakano S, Masumoto N, Fujishima H, Niho Y. Schedule- dependent reversion of acquired cisplatin resistance by 5- fluorouracil in a newly established cisplatin-resistant HST-1 human squamous carcinoma cell line. Int J Cancer. 1996;65:479-484.
23.Yeh KH, Cheng AL, Wan JP, Lin CS, Liu CC. Down-regulation of thy- midylate synthase expression and its steady-state mRNA by oxalipla- tin in colon cancer cells. Anticancer Drugs. 2004;15:371-376.
24.Skorupski KA, Uhl JM, Szivek A, Allstadt Frazier SD, Rebhun RB, Rodriguez Jr CO. Carboplatin versus alternating carboplatin and doxo- rubicin for the adjuvant treatment of canine appendicular osteosar- coma: a randomized, phase III trial. Vet Comp Oncol. 2016;14:81-87.
25.de Vos JP, Burm AG, Focker AP, Boschloo H, Karsijns M, van der Waal I. Piroxicam and carboplatin as a combination treatment of canine oral non-tonsillar squamous cell carcinoma: a pilot study and a literature review of a canine model of human head and neck squa- mous cell carcinoma. Vet Comp Oncol. 2005;3:16-24.
26.MurphyS,HayesA,AdamsV,etal.Roleofcarboplatininmulti-modality treatment of canine tonsillar squamous cell carcinoma—a case series of five dogs. J Small Anim Pract. 2006;47:216-220.
27.Wouda RM, Hocker SE, Higginbotham ML. Safety evaluation of combination carboplatin and toceranib phosphate (Palladia) in tumour-bearing dogs: a phase I dose finding study. Vet Comp Oncol. 2018 Mar;16(1):E52-E60.
28.Veterinary Cooperative Oncology Group. Veterinary Cooperative Oncology Group—common terminology criteria for adverse events (VCOG-CTCAE) following chemotherapy or biological antineoplastic therapy in dogs and cats v1.1. Vet Comp Oncol. 2016;14:417-446.
29.Nguyen SM, Thamm DH, Vail DM, London CA. Response evaluation criteria for solid tumours in dogs (v1.0): a Veterinary Cooperative Oncology Group (VCOG) consensus document. Vet Comp Oncol. 2015;13:176-183.
30.CharneySC,BergmanPJ,McKnightJA,etal.Evaluationofintracavi- tary mitoxantrone and carboplatin for treatment of carcinomatosis, sarcomatosis and mesothelioma, with or without malignant effusions: a retrospective analysis of 12 cases (1997-2002). Vet Comp Oncol. 2005;3:171-181.
Bu makaleye atıfta bulunmak için: Menard K, Flesner BK, Glahn A, Boudreaux B, Bryan JN. Concurrent 5-fluorouracil and carbo- platin for the treatment of canine carcinomas. Vet Comp Oncol. 2018;1–6. https://doi.org/10.1111/vco.12426