| *İletişim: bonkobara@nvlu.ac.jp 3 Hayvan Yaşam Bilimleri Araştırma Merkezi, Nippon Veteriner Hekimlik ve Yaşam Bilimleri Üniversitesi, Tokyo, Japonya Yazar(lar) 2022. Açık Erişim Bu makale, asıl yazar(lar)a ve kaynağa uygun şekilde atıfta bulunduğunuz, Creative Commons lisansına link verdiğiniz ve değişiklik yapılıp yapılmadığını belirttiğiniz sürece, herhangi bir ortam veya formatta kullanım, paylaşım, uyarlama, dağıtım ve çoğaltmaya izin veren Creative Commons Attribution 4.0 Uluslararası Lisansı ile lisanslanmıştır. Bu makalede yer alan görseller veya diğer üçüncü taraf materyalleri, aksi belirtilmedikçe, makalenin Creative Commons lisansına dahildir. Materyal, makalenin Creative Commons lisansına dahil değilse ve kullanım amacınıza yasal düzenlemeler tarafından izin verilmiyorsa veya izin verilen kullanımı aşıyorsa, doğrudan telif hakkı sahibinden izin almanız gerekir. Bu lisansın bir kopyasını görüntülemek için şu adresi ziyaret edebilirsiniz: http://creativecommons.org/licenses/by/4.0/. Creative Commons Public Domain Tahsis feragati (http://creativeco mmons.org/publicdomain/zero/1.0/), verilere ilişkin referans satırında aksi belirtilmedikçe, bu makalede kullanıma sunulan veriler için geçerlidir Makalenin İngilizce versiyonu için: https://doi.org/10.1186/s12917-022-03484-1 |
| Özet Giriş: Multipl miyelom (MM) kedilerde nadir görülen bir neoplazmdır. Bu hastalığın kedilerde nadir görülmesi nedeniyle henüz belirlenmiş bir tedavi standardı bulunmamaktadır. Bortezomib, insanlarda MM için ilk basamak ilaç olarak kullanılan bir proteozom inhibitörüdür, ancak şu anda kedi MM’sindeki etkinliği bilinmemektedir. Biz bu çalışmada bortezomib tedavisine olumlu yanıt veren kedi MM vakasını sunmaktayız. Vaka sunumu: Bu vaka, klinik semptomlar (anoreksi, halsizlik ve kusma), hafif azotemi ve pansitopeni ile başvuran hafif zincir MM’li 11 yaşında kısır olmayan erkek evcil bir kedinindi. Kedi prednizolonlu melfalan (MP) tedavisinde başarısız olmuş ve 88. günde bortezomib (Velcade) tedavisine başlanmıştır. Her tedavi döngüsü 2 hafta boyunca haftada iki kez subkutan uygulamadan ve ardından 1 haftalık dinlenmeden oluşacak şekilde toplam 6 tedavi döngüsü şeklinde uygulanmıştır. İlk döngüde bortezomib dozu ilk hafta için 0,7 mg/m2 ve ikinci hafta için 1,0 mg/m2 idi. Sonraki döngüler için 0.7 mg/m2 doz kullanıldı. Prednizolon ilk 2 döngüde eşzamanlı olarak uygulandı. Bortezomib tedavisini takiben, klinik semptomlar kayboldu ve serum globulininde azalma ve pansitopenide iyileşme kaydedildi. Tanı sırasında var olan monoklonal gammopati, serum immünoglobulin hafif zincirinin aşırı üretimi ve Bence-Jones proteinürisi 123. günde tespit edilemedi. Bortezomib tedavisinin sonunda da (213. Gün) monoklonal gammopati tespit edilememiştir. Bortezomib 1,0 mg/m2 dozunda uygulandığında anoreksi, halsizlik ve belirgin kemik iliği toksisitesi görülürken, tedavi süresi boyunca 0,7 mg/m2 dozunda fark edilebilir bir toksisite gözlenmemiştir. Vaka takibe alınmıştır ve 243. Gün itibariyle nüks olduğuna dair herhangi bir kanıt görülmemiştir. Sonuç: Bortezomib, MP ile başarısızlığın ardından bu kedi MM vakasının tedavisinde etkili ve kalıcı olmuştur. Bortezomib bu kedide 0,7 mg/m2 dozunda iyi tolere edilmiş, ancak 1,0 mg/m2 dozunda tolere edilememiştir. Bortezomib, kedi MM’sinin tedavisi için daha fazla araştırılmaya elverişli bir ilaç gibi durmaktadır. Anahtar Kelimeler: Kedi, Multipl miyelom, Bortezomib |
GirişMultipl miyelom (MM) kedilerde nadir görülen bir neoplazmdır. Bu hastalığın kedilerde nadir görülmesi nedeniyle, bu tür için belirlenmiş herhangi bir tedavi standardı bulunmamaktadır. Köpek MM’sinin tedavisinde sıklıkla kullanılan [1] ve eskiden insan MM’sinde ilk basamak tedavi olarak kullanılan prednizolon/prednizon (MP) ile kombine melfalan kullanılarak yapılan kemoterapi, bazı kedi MM vakalarında rapor edilmiştir [2, 3]. Bu raporlarda, söz konusu tedaviye olumlu yanıtlar gözlenmiştir; sekiz hastadan üçü 6 aydan fazla [2] ve yedi hastadan biri 6 aylık sağkalım elde etmiştir [3]. Bununla birlikte, yanıt vermeyen veya yanıt veren ancak birkaç hafta veya daha az sağkalım elde eden vakalar da vardı. Bir proteozom inhibitörü olan bortezomib, şu anda insanlarda MM tedavisi için ilk basamak ilaç olarak hizmet vermektedir. Bu bileşik, daha önce uzun bir süre boyunca ilk basamak tedavi olarak MP ile tedavi edilen insan MM’si için çığır açan bir ilaçtır. Bortezomib 26S proteazoma tersine bağlanarak çeşitli pro-apoptotik faktörlerin proteazom tarafından parçalanmasını önler ve neoplastik hücrelerde programlanmış hücre ölümünün aktivasyonuyla sonuçlanarak MM’li insan hastalarda terapötik etkiler oluşturur [4]. Günümüzde bortezomib insanlarda MM tedavisi için yaygın olarak kullanılmasına rağmen, bu bileşiğin kedi MM’sindeki terapötik faydası şu anda bilinmemektedir. Bu makalede, MP ile tedavinin başarısız olmasının ardından bortezomibe iyi yanıt veren bir kedi MM vakası sunulmaktadır. |
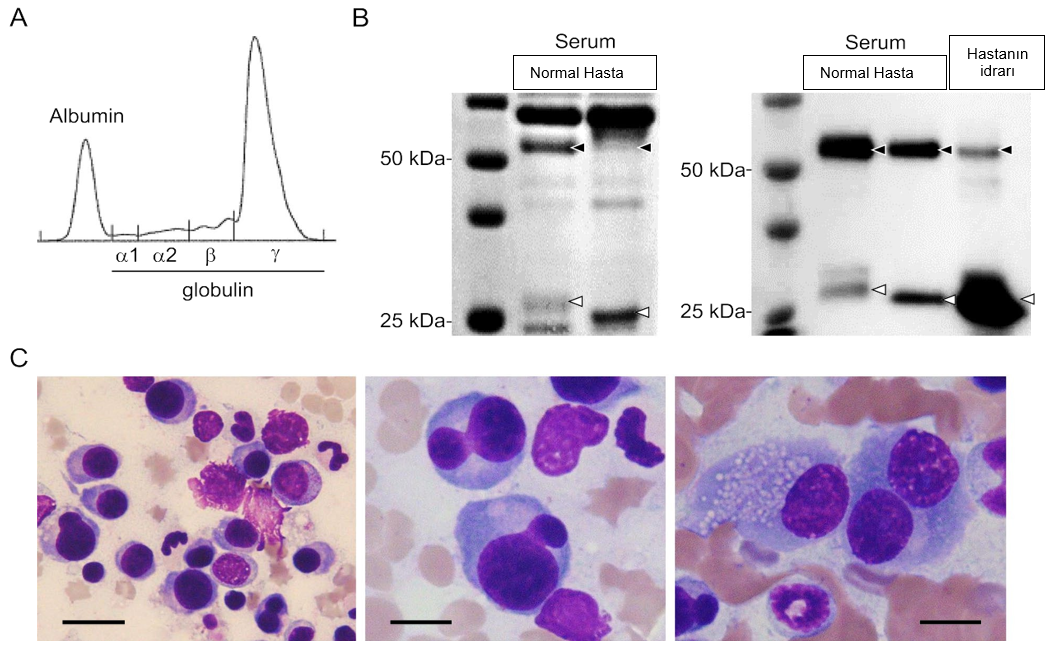
Vaka sunumuVaka, iki haftalık anoreksi, halsizlik ve kusma öyküsü ile başvuran 11 yaşında kısır olmayan erkek evcil bir kediydi. Kedi, nonrejeneratif anemi ile karakterize pansitopeni sergilemiştir (hematokrit, %22 [referans aralığı, %30,3-52,3]; kırmızı kan hücresi sayısı, 4,33 × 106/μL [referans aralığı, 6,54-12,2 × 106/μL]; hemoglobin, 7,3 g/dL [referans aralığı, 9,8-16,2 g/dL]; retikülosit sayısı, 3,9 × 103/μL), lökopeni (2750/μL; referans aralığı, 2870-17.020/μL) ile nötropeni (1320/μL, referans aralığı 2300-10.290/μL) ve trombositopeni (39 × 103/μL; referans aralığı, 151-600 × 103/μL). Serum kimyasında azotemi (kan üre nitrojeni, 35,1 mg/dL [referans aralığı, 17,6-32,8 mg/dL]; kreatinin, 2,5 mg/dL [referans aralığı 0,9-2,1 mg/dL]) ve proteinüri saptandı. Karaciğer ve elektrolit panellerinde herhangi bir anormallik kaydedilmemiştir. Kedi, agaroz jel serum protein elektroforez testi ile monoklonal gammopati ile birlikte hiperproteinemi (10,9 g/dL; referans aralığı, 5,7-7,8 g/ dL) ve hiperglobulinemi (7,5 g/dL; referans aralığı, 2,7-5,2 g/dL) sergilemiştir (Şekil 1A). Coomassie brilliant blue boyamalı sodyum dodesil sülfat-poliakrilamid jel elektroforezi (SDS-PAGE) (Şekil 1B, sol panel) ve western blotlama (Şekil 1B, sağ panel) ile yapılan serum protein analizi immünoglobulin hafif zincirin aşırı üretildiğini göstermiştir. İdrarda immünoglobulin hafif zincir (Bence-Jones proteinürisi) ve bir miktar immünoglobulin ağır zincir varlığı (hafif zincir nefrotoksisitesine bağlı glomerülopati varlığına işaret edebilir) aynı western blot ile tespit edilmiştir (Şekil 1B, sağ panel). Coomassie brilliant blue boyama ve western blotlama ile SDS-PAGE’in ayrıntıları Ek dosya 1’de verilmiştir (Şekil 1B’nin orijinal görüntüleri Ek dosya 2’de verilmiştir). Torasik ve abdominal radyografilerde veya abdominal ultrason taramasında herhangi bir anormallik görülmedi. Kemik iliği aspirasyon biyopsisinde, plazma hücrelerinin dağıldığı veya fokal kümeler oluşturduğu kemik iliği plazmasitozu (kemik iliği hücrelerinin >%20’si) saptandı. Plazma hücreleri anizositoz ve anizokaryoz sergilemiş (Şekil 1C, sol panel) ve bazılarında tuhaf şekilli çekirdekler görülmüştür (Şekil 1C, orta panel). Çift çekirdekli plazma hücreleri, görünür tek veya çok sayıda nükleol içeren plazma hücreleri ve Russell cisimciği benzeri inklüzyonlar içeren plazma hücreleri zaman zaman görülmüştür (Şekil 1C, sağ panel). Kemik iliği aspiratı kullanılarak yapılan PCR klonalite testi ile immünoglobulin lambda hafif zincirde monoklonalite tespit edilmiştir. İmmünoglobulin hafif zincirinin aşırı üretiminden kaynaklanan monoklonal gammopati, Bence-Jones proteinürisi ve kemik iliğinde monoklonal neoplastik plazma hücresi genişlemesi gibi bulgulara dayanarak bu vakaya MM, özellikle de varyant hafif zincir MM tanısı konmuştur. Tanı günü 1. Gün kabul edilmiştir. Kediye, prednizolon (2 mg/kg, günde bir kez 1 mg/kg’a düşürülerek; 1. Günde başlandı) ile birlikte melfalan (0,1 mg/kg, oral, günde bir kez [4-10. Gün ve 60-81. Gün] veya gün aşırı [11-59. Gün]; 4. Günde başlandı) içeren MP (Şekil 2A) tedavisi uygulandı. Yaklaşık 30. Günde serum globülininde azalma (Şekil 2A) ve klinik semptomlarda iyileşme dahil olmak üzere tedaviye bazı yanıtlar gözlense de, bu yanıtlar kalıcı olmadı ve melfalan 81. Günde kesildi. 88. Günde kedinin bortezomib (Velcade, Janssen Pharmaceutical K.K., Tokyo, Japonya) ile tedavisine başlanmıştır (Şekil 2A). Tedavi döngüsü, 2 hafta boyunca haftada iki kez subkutan bortezomib (0,7 veya 1,0 mg/m2) uygulamasının ardından 1 haftalık aradan oluşmuştur. Prednizolon (1 mg/kg, oral, günde bir kez) ilk iki döngü boyunca eşzamanlı olarak kullanıldı. İlk üç döngüde her bortezomib dozu uygulamasından önce ve sonraki döngülerde verilen haftanın ilk bortezomib dozundan önce tam kan hücresi sayımı (CBC) ve serum kimyası testleri yapılmıştır. Tedavi aralığı boyunca gerektiğinde ek CBC ve serum kimyası testleri ve görüntüleme testleri (radyografi ve/veya ultrason taraması) yapılmıştır. Toksisiteler Veteriner Onkoloji Grubu – Yan Etkiler için Ortak Terminoloji Kriterleri versiyon 2’ye göre derecelendirilmiştir [5]. Bortezomib doz aralığının başlangıcında, kedide orta ila şiddetli klinik semptomlar (anoreksi ve yorgunluk) ve rejeneratif olmayan anemi (hematokrit, %26,8; kırmızı kan hücresi sayısı, 4,81 × 106/μL; hemoglobin, 8,4 g/dL; retikülo-sit sayısı, 1,9 × 103/μL) ve nötropeni (1320/μL) ile lökopeni (1580/μL) görülmüştür. Trombosit sayısı referans aralığın alt sınırına yakındı (157 × 103/μL). Serum kimyası analizinde hiperproteinemi (8,8 g/dL) gözlenmesine rağmen karaciğer, böbrek ve elektrolit panellerinin belirtilen referans aralıkta olduğu görülmüştür. Serum globulin (5,4 g/dL) referans aralığın üst sınırının biraz üzerindeydi ancak monoklonal gammopati açıkça mevcuttu (Şekil 2B, sol panel). |
| Bortezomib dozunun ilk döngüsünde, bileşik ilk hafta boyunca 0,7 mg/m2 olarak uygulanmıştır. İlk haftanın sonunda klinik semptomların kaybolması, nötrofil sayısının normal aralığa (4800/μL) geri dönmesi ve serum globülininin azalması (4,2 g/ dL) (Şekil 2A) gibi olumlu yanıtlar gözlenmiştir. Daha sonra bortezomib dozu ikinci haftada 1,0 mg/m2’ye yükseltilmiştir (94. ve 98. günlerde uygulanmıştır). Kedide daha sonra grade 2 anoreksi ve grade 2 halsizlik ile ikinci 1.0 mg/m2 dozdan sonraki gün grade 4 nötropeni (140/μL, febril olmayan) ve grade 3 trombositopeni (34 × 103/μL) görülmüştür. Kedi daha sonra antibiyotik ve destekleyici bakım ile tedavi altına alınmıştır. Bir haftalık dinlenme döneminden sonra klinik semptomlar kayboldu ve nötrofil ve trombosit değerleri düzeldi (sırasıyla 6300/μL ve 196 × 103/μL). Bu nedenle bortezomib dozu sonraki döngüler için 0,7 mg/m2 olarak belirlendi. Kediye toplam altı döngü bortezomib tedavisi uygulandı (Gün 88-213). Tedavinin ikinci ila altıncı döngüleri sırasında kedinin durumu iyiydi ve serum globulin değerleri sürekli olarak referans aralığın üst sınırının altındaydı (Şekil 2A). Bu dönemde kan üre nitrojeni ve kreatininin bazen belirtilen referans aralıklarının üst sınırının biraz üzerinde olması dışında nötropeni, trombositopeni, gaz trointestinal semptomlar, proteinüri veya serum kimyasında anormallik kaydedilmemiştir. |
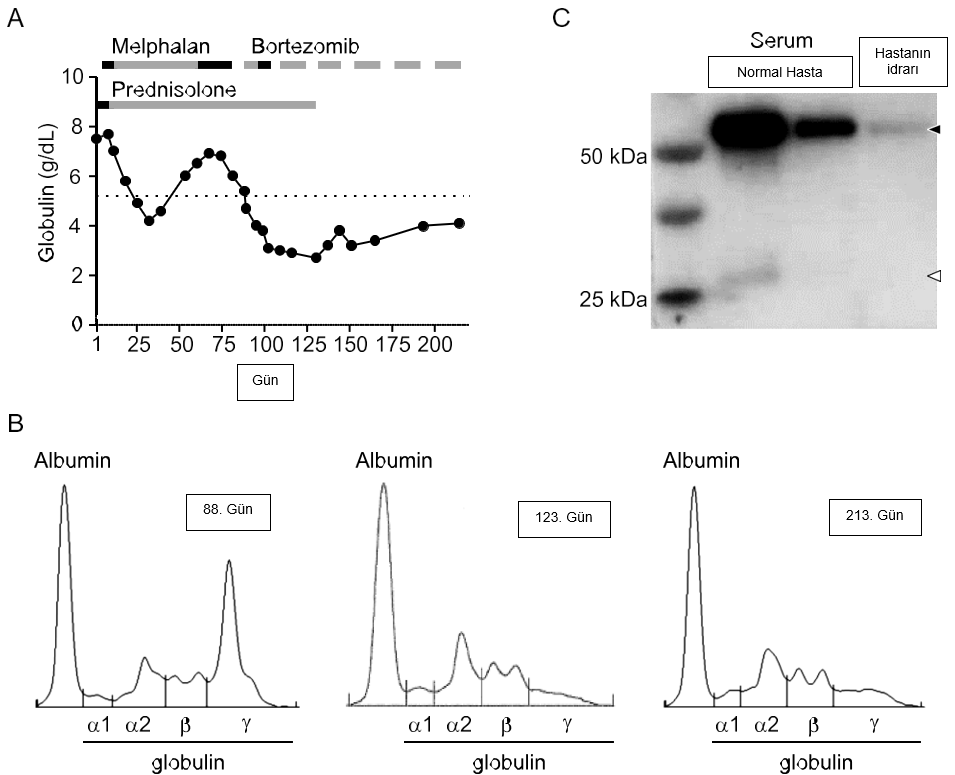
| Monoklonal gammopati, serum immünoglobulin hafif zincir ve Bence-Jones proteinürisi 123. Günde tespit edilememiştir (Şekil 2B, orta panel ve Şekil 2C [Şekil 2C’nin orijinal görüntüsü Ek dosya 2’de verilmiştir]). Monoklonal gammopati 213. Günde tespit edilememiştir (Şekil 2B, sağ panel). Hematokrit ve kırmızı kan hücresi değerleri 193. Günde normal aralıklara yükselmiş ve bortezomib tedavi aralığının sonuna kadar normal aralıkta kalmıştır. İnsan MM’sinde bildirilen ortalama tedavi döngüsü sayısı 6 döngü olduğundan [6] ve bu kedi 6 tedavi döngüsünün sonunda iyi durumda olduğundan, bortezomib tedavisi 6 döngüden sonra kesilmiştir. Tedaviyi takiben, vaka 2 haftada bir fizik muayene ve kan testleri ile takibe alınmıştır. Kedinin durumu iyi olup 243. Gün itibariyle herhangi bir nüks belirtisi göstermemiştir. |
Tartışma ve sonuçBu çalışma, bortezomib ile başarılı bir şekilde tedavi edilen ilk kedi MM vaka raporunu (bildiğimiz kadarıyla) temsil etmektedir. MP ile tedavi, önceki raporlarda [2, 3] ve mevcut vakada belirtilmiş olduğu gibi, kedi MM vakaları için etkili olabilir. Bununla birlikte, MP ile tedavi başarısız olduktan sonra kedi MM’si için tavsiye edilen herhangi bir terapötik ilaç bilinmemektedir, ancak siklofosfamid ve kortikoidlerin kullanımı faydalı olabilir çünkü bu ilaçların kombinasyonunun miyelomla ilişkili bozukluğu olan kedilerde klinik etkinliği olduğu görülmüştür [7]. Mevcut vakada MP başarısızlığını takiben bortezomibe olumlu yanıt kaydedildiği ve bortezomibin MP dahil ön basamak tedaviden sonra nüks eden MM’li insan hastalarda terapötik aktiviteye sahip olduğu göz önüne alındığında [8], bortezomibin MP ile başarısızlıktan sonra kedi MM’sinde kurtarma ilacı olarak kullanım potansiyeli olabilir. Ayrıca, daha önce tedavi edilmemiş MM’li insan hastalarda, tek ajan bortezomib tedavisinin etkili olduğu görülmüştür [9] ve bortezomib artı MP’nin tek başına MP’ye kıyasla daha iyi sonuçlar sağladığı görülmüştür [10]. Bu raporlar ve bortezomibin şu anda insanlarda MM için ilk basamak ilaç olarak kullanıldığı gerçeği göz önüne alındığında, bortezomibin kedi MM tedavisi için ilk basamak tek ajan veya MP ile kombinasyon halinde kullanılabilecek potansiyel bir ajan olabileceği düşünülmektedir, ancak bu konunun daha kapsamlı araştırmalarla incelenmesi gerekmektedir. Kedilerde MM’nin davranışı hakkında çok az şey bilinmesine rağmen, MM’li dokuz kedi üzerinde yapılan bir çalışmada [2] anemi, hiperkalsemi, patolojik kırıklar, Bence-Jones proteinüri, azotemi ve tedaviden 8 hafta sonra serum proteininde kalıcı yükselme ve klinik iyileşmenin çok az olması/hiç olmaması olumsuz prognostik faktörler olup MM’nin daha agresif bir türünü yansıtmaktadır. Bu çalışmada, agresif MM’li dört kedinin hayatta kalma süresi 14 günü geçmezken (ortalama 5 gün), daha az agresif MM’li beş kedinin ortalama hayatta kalma süresi 387 gündü (aralık 120 ila 720 gün). İnsan MM’sinde, anizositoz ve neoplastik plazma hücrelerinin atipik morfolojisi, pansitopeni ve hafif zincir MM görülmesinin daha kısa sağkalım ile ilişkili olduğu belirtilmiştir [11-13]. Bu raporda, sunulan vakada pansitopeni, Bence Jones proteinürisi ve azotemi vardı ve MP’ye sadece geçici yanıtlar verdi. Ayrıca, bu vaka hafif zincir MM idi ve neoplastik plazma hücreleri atipik morfoloji ile anizositoz sergiliyordu. Bu noktalar göz önüne alındığında, bu vakadaki MM agresif bir MM formu gibi görünmektedir; bortezomib bu vakadaki nispeten uzun sağkalıma katkıda bulunduğu düşünülmektedir. Kedinin bortezomib ile tedavisi için ilk iki döngüde eşzamanlı olarak prednizolon kullanılmıştır. Prednizolonun kedi MM’sindeki anti-neoplastik etkileri bilinmemekle birlikte, bu ajan bu hastalık için potansiyel fayda sağlamış ve böylece çalışmamızda gözlenen tümör yanıtına katkıda bulunmuş olabilir. Bununla birlikte, tümörün MP tedavisi altında nüksettiği ancak prednizolon tedavisinin sonlandırılmasından 100 günden fazla bir süre sonra iyi bir şekilde kontrol altında kaldığı göz önüne İnsanlarda standart bortezomib dozu 1,3 mg/m2’dir. Standart doz uygulanan hastalarda ciddi toksik etkiler gözlendiğinde, insan MM’sinde bortezomibin faz 2 çalışmasında azaltılmış doz (1.0 mg/m2) veya minimal doz (0.7 mg/m2) ile de kullanılmıştır [14]. Bortezomibin kedilerdeki toksisitesi bilinmediğinden, bu çalışmada insan minimal dozu olan 0,7 mg/m2’den başlanmış ve 1,0 mg/m2’ye yükseltilmiştir. Bu vakada 0,7 mg/m2 dozundaki bortezomib iyi tolere edilmiş, tedavi süresi boyunca bu doz seviyesinde fark edilebilir herhangi bir toksik etki gözlenmemiştir. Bortezomib tedavisi sırasında bazen hafif azotemi görülse de, bu semptom bu vakada zaten mevcuttu ve bortezomib ile daha da kötüye gitmedi. Aynı zamanda, bu kedide bortezomibin 1.0 mg/m2 dozunda verilmesiyle birlikte klinik semptomlarla (anoreksi ve yorgunluk) birlikte geçici ancak belirgin kemik iliği toksisitesi kaydedilmiştir. Bu dozun insanlarda kullanılan standart dozdan (1,3 mg/m2) daha düşük olması dikkat çekicidir. Kedilerde bort-ezomibin tolere edilebilir maksimum dozu (MTD) bilinmemekle birlikte, MTD’nin türler arasında değiştiği görülmüş, intravenöz tek doz MTD’ler farelerde 3,0 mg/m2; sıçanda 0,6 mg/m2; köpekte 3,6 mg/m2 ve maymunda 1,2 mg/m2 şeklinde bildirilmiştir [15]. Dolayısıyla kedi, insanlara kıyasla bortezomibe karşı daha yüksek duyarlılığa sahip bir tür olabilir. Alternatif olarak, bu kedideki böbrek yetmezliği, bortezomibin insan MM’sinde böbrek yetmezliği olan klinik hastalarda daha sık ve ciddi advers olaylara neden olduğu göz önüne alındığında, bortezomibin 1.0 mg/m2’de görülen toksik etkilerine yol açmış olabilir [16]. Sonuç olarak, bortezomib, MP tedavisi başarısız olan bir kedi MM vakasının tedavisinde etkili ve kalıcı olmuştur. Bortezomib bu kedide 0,7 mg/m2 dozunda iyi tolere edilmiş, ancak 1,0 mg/m2 dozunda tolere edilememiştir; daha yüksek doz anoreksi, yorgunluk ve kemik iliği toksisitesi ile ilişkilendirilmiştir. Kedi MM’si için bortezomibin toksisitesi ve etkinliği üzerine daha fazla araştırma yapılması önerilmektedir. |
| Kısaltmalar MM: Multipl miyelom; MP: Prednisolone/ prednisone ile kombine edilmiş melfalan; SDS-PAGE: Sodyum dodesil sülfat-poliakrilamid jel elektroforezi. |
Ek Bilgi |
| Teşekkürler Bu konuya ilişkin herhangi bir bilgi verilmemiştir. Katkıda bulunan yazarlar Finansman Veri ve materyallere erişim BeyanlarEtik kurul onayı ve katılım izni Yayın izni Çıkar çatışması Sunum tarihi: 14 Nisan 2022 Yayıncının Notu |
Kaynakça
|




