Özet: Rezeke edilemeyen nodüler ve diffüz tip hepatosellüler karsinom (HCC), tedavi seçeneklerinin sınırlı olması nedeniyle prognozu kötüdür. Sistemik geleneksel kemoterapi, tatmin edici sonuçlar vermemekle birlikte nadiren rapor edilmiştir. Bu prospektif, randomize edilmemiş, kör olmayan, tek merkezli klinik çalışmanın amacı, ilerlemiş, rezeke edilemeyen HCC’li köpeklerde talidomid, piroksikam ve siklofosfamidden oluşan metronomik kemoterapi (MC) ile karşılaştırmalı olarak sorafenibin güvenilirliğini, objektif yanıt oranını, progresyona kadar geçen süreyi ve genel sağkalımı araştırmaktır. Aralık 2011 ve Haziran 2017 tarihleri arasında 13 köpek çalışmaya dahil edilmiştir: yedisine sorafenib, altısına ise MC uygulanmıştır. Progresyona kadar geçen ortalama süre sorafenib ile tedavi edilen köpeklerde 363 gün (%95 GA, 191-535) iken MC ile tedavi edilen köpeklerde 27 gün (%95 GA, 0-68) olmuştur (p = 0,044). Ortalama genel sağkalım sorafenib alan köpeklerde 361 gün (%95 GA, 0-909) iken MC alanlarda 32 gün (%95 GA, 0-235) olmuştur (p = 0.079). Sorafenib, hastalığın kontrolündeki faydası ve kabul edilebilir düzeydeki güvenilirliği nedeniyle ileri evre HCC’li köpeklerin tedavisinde başarılı bir yöntem gibi görünmektedir. MC veya geleneksel kemoterapiye kıyasla sorafenibin etkinliğini ve dezavantajlarını karşılaştırmak üzere yeni randomize prospektif klinik çalışmaların yapılması için ideal zemini sağlamaktadır.
Anahtar kelimeler: köpek; hepatosellüler karsinom; metronomik tedavi; sonuç; sorafenib; toksisite; spontan model
1. Giriş
Köpeklerde hepatosellüler karsinom (HCC) en sık görülen primer karaciğer tümörüdür [1,2] ve prognozu morfolojik tipine bağlıdır. Masif form tipik olarak bir karaciğer lobu ile sınırlıdır ve cerrahi rezeksiyona uygun olabilmektedir [3]. Ayrıca, metastaz riski genellikle düşük ila orta düzeydedir. Ancak, HCC’nin nodüler ve diffüz formları tipik olarak birden fazla karaciğer lobunu etkiler ve cerrahi rezeksiyona uygun değildir [1-3]. Ayrıca, metastaz oranı her iki form için de %90’ı aşmaktadır [1-3]. Bu nedenle, rezeke edilemeyen nodüler veya diffüz HCC, cerrahi olmayan vakalarda tedavi seçenekleri sınırlı olduğu için genellikle kötü bir prognoza sahiptir.
Lokal tümör ablasyonu, Transarteryel Kemoembolizasyon ve radyoterapi gibi disiplinler arası yaklaşımlar veteriner hekimlikte henüz araştırılmamıştır. Sistemik geleneksel kemoterapi,
Kanserler 2020, 12, 1272; doi:10.3390/cancers12051272 www.mdpi.com/journal/cancers
tatmin edici olmayan sonuçlar vermekle birlikte nadiren rapor edilmiştir. Tümör hücrelerinin kemoterapötik ilaçlara direnci, HCC’li hastalarda klinik tedavinin başarısız olmasının ve nükslerin ortaya çıkmasında kilit rol oynamaktadır [4]. Yapılan bir çalışmada, rezeke edilemeyen HCC’li yedi köpek intravenöz gemsitabin ile tedavi edilmiştir [5]. Ortalama progresyonsuz geçen süre 150 gün ve ortalama sağkalım süresi 197 gün olmuştur [5]. Başka bir çalışmada, rezeke edilemeyen ve metastatik HCC’li iki köpek gemsitabin ve karboplatin tedavisine yanıt vermemiştir [6]. Bu nedenle, yeni tedavi yaklaşımlarına acilen ihtiyaç duyulmaktadır.
Metronomik kemoterapi (MC), geleneksel kemoterapiye kıyasla toksisitesi ve uygulama kolaylığı sayesinde son zamanlarda dikkat çeken bir tedavi yöntemi haline gelmiştir. MC, hem anti-anjiyojenik hem de immün-modülatör etkili terapötik hedef doğrultusunda, sitotoksik ilaçların uzun süreli aralar vermeden ve yüksek doz kemoterapiden çok daha düşük dozlarda uygulanması anlamına gelmektedir [7]. Veteriner onkolojide, MC çoğunlukla palyatif amaçlı kullanılmaktadır. Metronomik rejimlerde yaygın olarak kullanılan ilaçlar arasında siklofosfamid ve piroksikam bulunmaktadır [8-10]. Tek ajan olarak veya siklofosfamid ve piroksikam ile kombinasyon halinde metronomik rejimin bir parçası olarak köpeklerde talidomid kullanımına ilişkin çok az sayıda rapor bulunmaktadır. Bu raporlarda toksisite yönünden olumlu bir profil görülmüş ve belli bir seviyede de antitümör etki tespit edilmiştir [11-15].
İleri veya orta evre HCC’si olan hastalarda, refrakter kanseri olanlarda veya lokorejyonel tedavilere artık uygun olmayan ve karaciğer fonksiyonu iyi korunmuş hastalarda (child pugh skoru A), multi-kinaz inhibitörü sorafenib, sistemik tedavi için FDA onaylı yegane birinci basamak tedavi seçeneği olmaya devam etmektedir [16]. Sorafenib, Raf kinazı, vasküler endotelyal büyüme faktörü reseptörleri 1, 2 ve 3’ü ve anti-proliferatif ve anti-anjiyojenik aktivitelere sahip trombosit türevli büyüme faktörü reseptörü β’yı hedef alan multi-kinaz inhibitörüdür. Ne yazık ki, insan hastaların önemli bir yüzdesinde, kazanılmış sorafenib direnci, tedavinin başarısız olmasına yol açan önemli klinik engellerden biri olmaya devam etmektedir. Metabolik yeniden yapılandırma da dahil olmak üzere tümör hücresinin sorafenibe duyarlılığının azalmasında çeşitli mekanizmalar devreye girmektedir [17-22].
İlaca bağlı en sık görülen yan etkiler bitkinlik, hipertansiyon, anoreksi, ishal, deride döküntü/deskuamasyon ve ön-arka bacakta deri reaksiyonudur [16,23].
Köpeklerde, sorafenib in vitro olarak köpek osteosarkom ve hemanjiosarkom hücrelerine karşı güçlü antitümör etki göstermiştir [24,25]. Sağlıklı dişi beagle köpeklerde yapılan preklinik toksikoloji çalışmalarına göre, 30 mg/kg/gün dozunda oral olarak uygulanan sorafenib, uzun süreli uygulamadan sonra (3-12 ay) ciddi gastrointestinal, kutanöz, renal, adrenal, kemik ve hematolojik toksisiteye neden olurken, 10 mg/kg/gün dozunda herhangi bir ciddi yan etki gözlenmemiştir [26,27]. Ayrıca sorafenib, HCC’li olan başka bir hayvan da dahil olmak üzere çeşitli kanser hastası köpekler üzerinde yapılan ilk faz tolerabilite çalışmasında klinik olarak da değerlendirilmiştir [28]. Tek oral sorafenib dozları haftada bir kez verildiğinde 3 mg/kg’a kadar tolere edilebilmiştir [28]. Bu nedenle, doz daha da arttırılabilir.
Bu prospektif, randomize edilmemiş, kör olmayan, tek merkezli klinik çalışmanın amacı, ilerlemiş, rezeke edilemeyen HCC’li köpeklerde talidomid, piroksikam ve siklofosfamid ile birlikte uygulanan MC’ye kıyasla sorafenibin güvenilirliğini, objektif yanıt oranını (RR), progresyona kadar geçen süreyi (TTP) ve genel sağkalımı (OS) araştırmaktır. Sorafenibin MC’den daha iyi sonuçlar vereceği varsayılmıştır.
2. Sonuçlar
- Köpekler ve tümörlerin özellikleri
Aralık 2011 ile Haziran 2017 arasında, sahipli 13 köpek tek bir merkeze (Centro Oncologico Veterinario) kaydedilmiştir: yedisine sorafenib uygulanmış ve altısı MC ile tedavi edilmiştir.
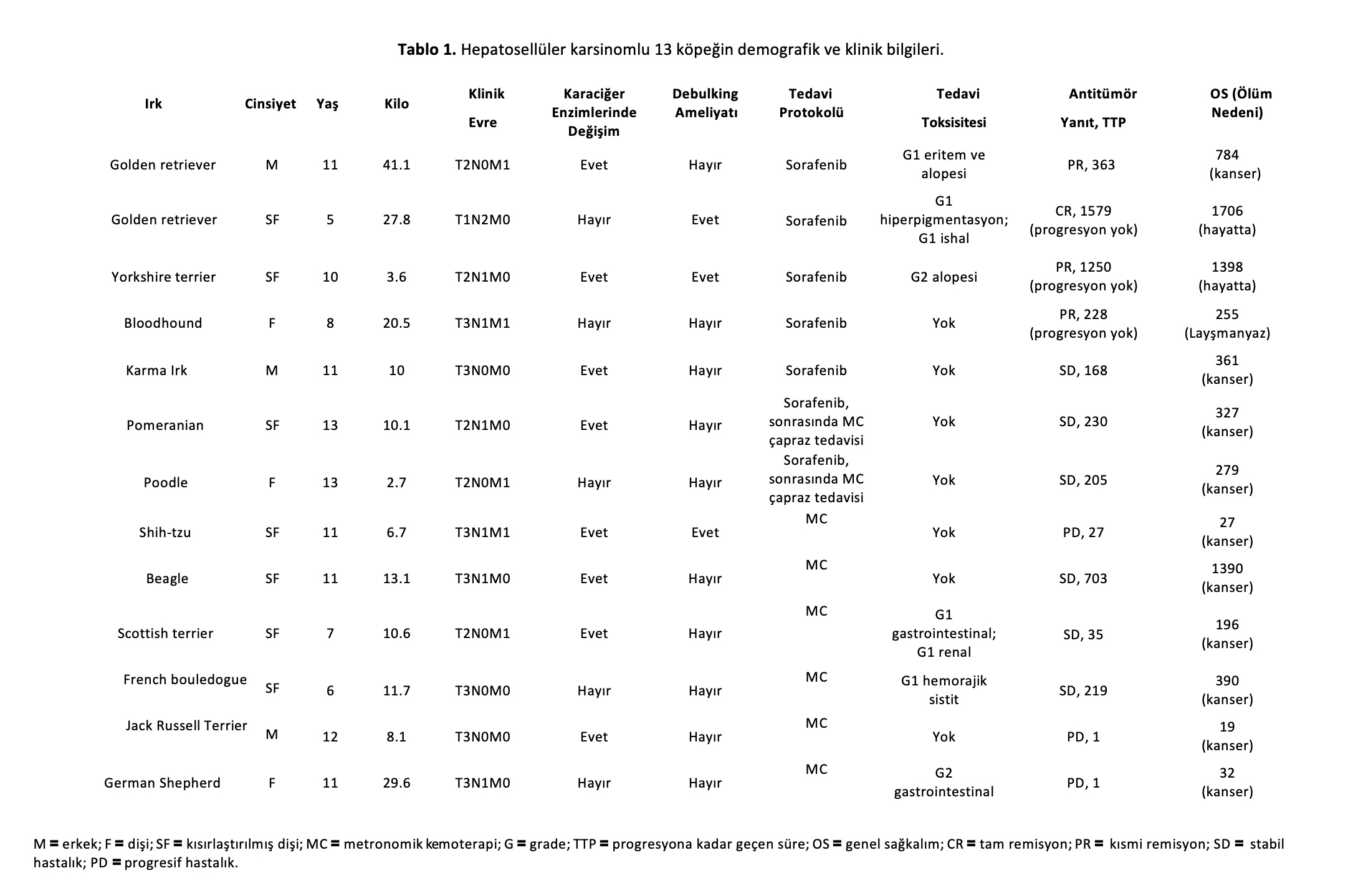
Söz konusu ırklar Tablo1’de listelenmiştir. 10 dişi (yedisi kısırlaştırılmış) ve üç kısırlaştırılmamış erkek vardı. Ortalama yaş 11 (yaş aralığı: 5 ila 13 yıl) ve ortalama ağırlık 10,6 kg (kilo aralığı: 2,7 ila 41,1 kg) idi.
Her vakaya ilk muayene gününde tam kapsamlı evreleme amaçlı tanı testleri yapılmıştır: dokuz köpeğe TBCT uygulanmış, dört köpeğin hastalığı ise batın ultrasonu ve toraks röntgeni ile evrelenmiştir.
Görüntüleme incelemesinde ortalama maksimum çapı 6,4 cm (dağılım, 3 ila 10 cm) olan karaciğerde yuvarlak bir kitle tespit edilmiştir. TBCT çekilen köpeklerde HCC heterojen şekilde büyürken, batın ultrasonu çekilenlerde tümör sonografik olarak heterojen solid görünümdeydi.
Dokuz köpekte HCC’ler kuadrat lob (n = 3), sol lateral ve medial (n = 4), sağ lateral (n = 1) ve sağ medial lob (n = 1) yerleşimli tek bir büyük kitle olarak ortaya çıkmıştır. Bu dokuz vakanın üçünde, intrahepatik metastazlarla uyumlu olarak primer lezyona bitişik ikincil nodüller gözlenmiştir.
Diğer dört vakada, tüm karaciğer loblarına yayılmış, benzer büyüklükte, çapları 0,4 ile 9 cm arasında değişen çoklu hepatik nodüller bulunmuştur. Ek bulgular arasında bölgesel lenf nodu büyümesi (n = 5), peritoneal nodüller ve assit (n = 2), sternal lenfadenopati (n = 1), torasik nodüller (n = 1) ve 2 cm’lik sağ adrenal nodül (n = 1) vardı.
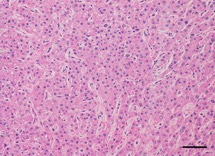
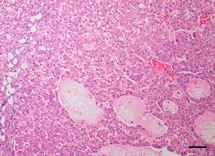
HCC’nin histopatolojik tanısı tüm köpeklerde görüntüleme eşliğinde tru-cut biyopsi (n = 10) veya cerrahi biyopsi (n = 3) yoluyla elde edilmiştir. Histolojik olarak, tüm tümörler baskın şekilde trabeküler patern ile karakterize olup, neoplastik hücreler 20 hücre kalınlığına kadar düzensiz trabeküller halinde dizilmiş, sıklıkla dilate sinüzoidlerle ayrılmış ve bazen kavernöz boşluklar oluşturmuştur (Şekil1ve2). Kollikatif nekroz sık rastlanılan bulgulardan biriydi (Şekil3). Nadiren, tümörlerin bir alt kümesinde psödoglandüler veya solid farklılaşma alanları gözlenmiştir.
Şekil 1. Köpek, karaciğer. Hepatoselüler karsinomun histolojik örneği. Tümör iyi diferansiye ve neoplastik hepatositlerin oluşturduğu değişken kalınlıkta trabeküllerden meydana gelmiş (trabeküler patern).
Hematoksilen ve eozin. Bar, 100 µm
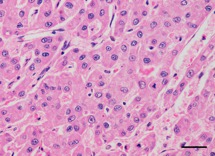
Hematoksilen ve eozin. Bar, 50 µm.
Hasta kayıt sırasında tüm köpeklerde ölçülebilir HCC vardı: 3 köpekte T2N0M1 hastalığı (IV. evre), 3 köpekte T3N0M0 hastalığı (III. evre), 2 köpekte T2N1M0 hastalığı (IV. evre), 2 köpekte T3N1M1 hastalığı (IV. evre), 2 köpekte T3N1M0 hastalığı (IV. evre) ve bir köpekte T1N2M0 hastalığı (IV. evre) vardı. Tüm N1 veya M1 vakalarında ultrason eşliğinde ince iğne aspirasyonu ile genişlemiş bölgesel lenf düğümleri ve diğer şüpheli metastatik lezyonlardan örnek alınmış ve metastatik hastalık olduğu doğrulanmıştır.
Beş köpeğin tedavi öncesi kan tahlillerinde görüldüğü üzere CBC, böbrek ve karaciğer fonksiyonları normaldi. Sekiz köpekte yüksek ALP (üst referans limitinin 4-53 katı), üç köpekte yüksek GGT (üst referans limitinin 2,2-569 katı), iki köpekte yüksek bilirubin (sırasıyla üst referans limitinin 2 ve 3 katı) ve bir köpekte yüksek AST (üst referans limitinin 2,5 katı) tespit edilmiştir.
Sorafenib alan yedi köpekten ikisine, kayıttan sırasıyla 38 ve 42 gün önce en büyük hepatik lezyona cerrahi debulking uygulanmıştır. Her iki köpekte de histopatolojik değerlendirmeye göre tam olmayan sınırlar ve kayıt sırasında ölçülebilir bölgesel metastatik lenf nodları vardı. Bu köpekler en uzun TTP’ye sahipti (sırasıyla 1250 ve 1579 gün) ve her ikisi de 1398 ve 1706 gün sonra veri analizi kapanışında hala hayattaydı.
MC alan altı köpekten birine MC başlamadan 31 gün önce en büyük hepatik lezyona cerrahi debulking uygulanmıştır; kayıt sırasında iki hepatik lezyon ve bölgesel lenf nodları ve akciğerlere metastaz mevcuttu. Bu köpek MC’nin başlatılmasından sadece 27 gün kadar hayatta kalmıştır.
Demografik özellikler ve potansiyel prognostik değişkenler iki tedavi grubu arasında homojen olarak dağılmıştır (Tablo2).
Tablo 2. Sorafenib veya metronomik kemoterapi ile tedavi edilen hepatosellüler karsinomlu 13 köpeğin demografik bilgileri ve prognoza bağlı olabilecek değişkenlerin dağılımları.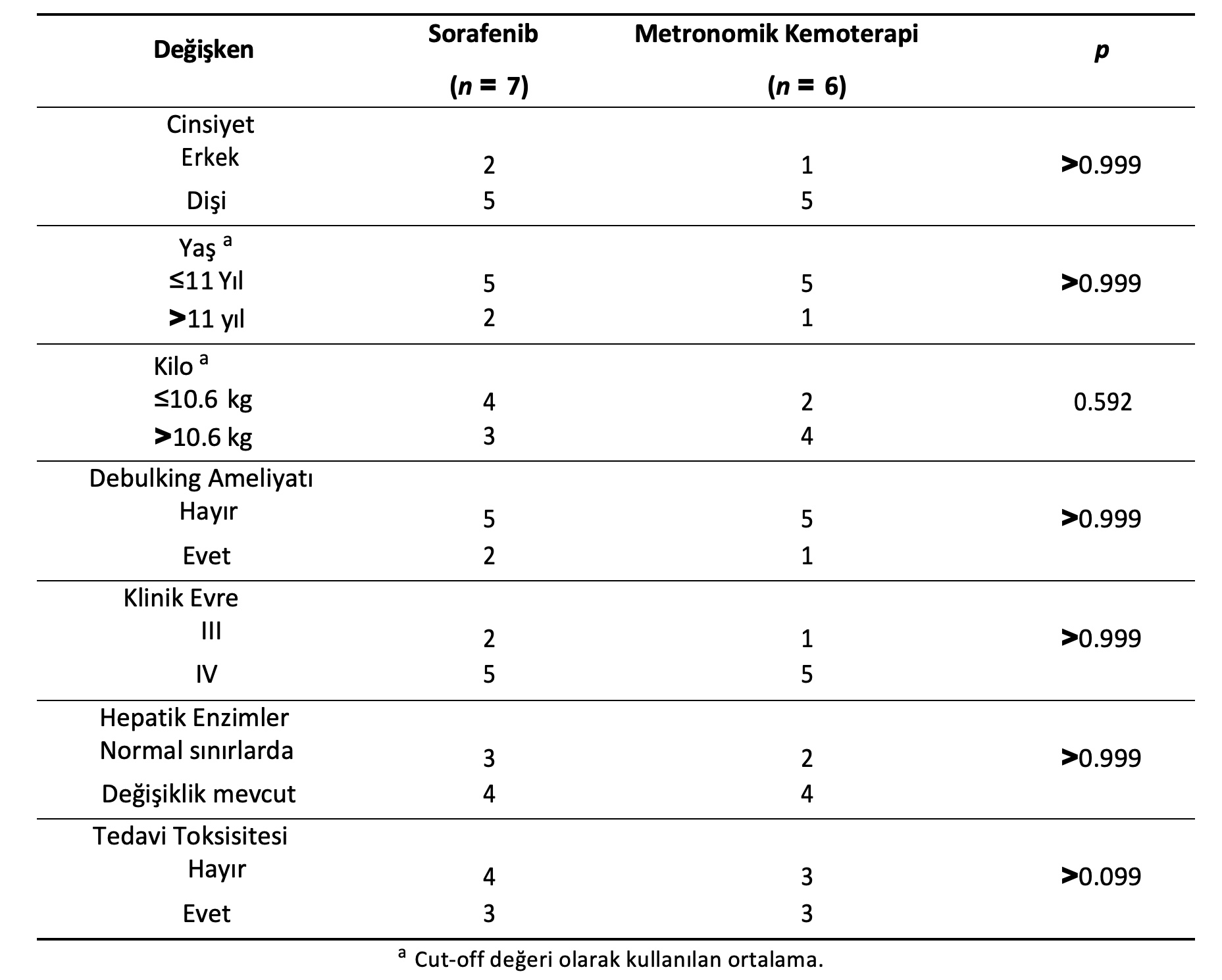
Şekil 3. Köpek, karaciğer. Hepatoselüler karsinomun histolojik örneği. Hepatositlerin trabekülleri çok sayıda düzensiz vasküler kanal ve kavernöz boşluklarla ayrılmıştır. Neoplastik hücrenin sitoplazması glikojen veya lipid dolumu nedeniyle genellikle soluk boyanır veya vakuolleşir. Multifokal olarak neoplastik doku kaybolur ve yerini granüler eozinofilik ve karyorektik debris alır (kollikatif nekroz).
Hematoksilen ve eozin. Bar, 100 µm.
- Tedavi ve toksisite
Yedi köpek oral sorafenib almıştır. Ortalama tedavi süresi 228 gündü (aralık, 168 ila 321 gün). Veri analizi tamamlandığında, beş köpeğin tedavisi ilacın bulunamaması nedeniyle, bir köpeğin tedavisi ise 168 gün sonra PD nedeniyle kesilmişti. Bir köpek tedavi altındayken tümöre bağlı olmayan nedenlerle (leishmaniasis) ölmüştür. PD görülen köpeğe sorafenib tedavisine ara verildikten sonra trans-arteriyel kemoembolizasyon uygulanmıştır. İlacın bulunamaması nedeniyle tedavisi kesilen beş köpekten ikisi MC’ye geçirilirken, kalan üçü hasta sahiplerinin tercihine bağlı olarak başka tedavi görmemiştir. İlginç bir şekilde, sonunculardan ikisi veri analizinin kapanışında sırasıyla CR ve PR’de hala hayattayken, MC’ye geçen diğer 2 köpeğin hastalığı ilerlemiş ve çapraz tedaviden 28 ve 34 gün sonra tümöre bağlı nedenlerle ölmüştür.
Altı köpek MC ile tedavi edilmiştir. Ortalama tedavi süresi 21 gündü (aralık, 4 ila 703 gün). Sadece bir köpeğin tedavisi 703 gün sonra PH nedeniyle kesilmiş ve kurtarma amaçlı toceranib ile tedavi edilmiştir.
Toksisite bakımından, sorafenib grubunda üç köpekte birer tane olmak üzere kutanöz toksisite gelişmiştir: grade 2 alopesi, grade 1 hiperpigmentasyon ve grade 1 lokalize eritem ve alopesi. Bir köpekte ayrıca semptomatik tedavi ile sorunsuz bir şekilde düzelen grade 1 ishal görülmüştür. Sorafenib tedavisi sırasında rutin karaciğer testleri yapılmıştır. Hiperbilirubinemi ve serum transaminaz yükselmesi görülmemiştir.
MC grubunda üç köpekte gastrointestinal toksisite (2’si grade 1, 1’i grade 2), bir köpekte grade 1 hemorajik sistit ve bir köpekte grade 1 renal toksisite görülmüştür.
Her iki grupta da tedaviye bağlı mortalite görülmemiştir.
Anket sonuçlarına göre, sorafenib alan 7 köpeğin 6’sında yaşam kalitesi iyileşirken, bir köpekte yaşam kalitesi sabit kalmıştır. MC alan 6 köpekten sadece 3’ü yaşam kalitesinin değerlendirilebileceği kadar uzun yaşamıştır. Bunlardan ikisinde yaşam kalitesi iyileşirken, son köpekte yaşam kalitesi sabit kalmıştır.
- Yanıt Oranları ve Bulgular
Sorafenib ile tedavi edilen yedi köpekten 1’inde CR, 3’ünde PR ve 3’ünde SD görülmüştür. CR, hepatik debulking uygulanan ve başvurduğunda hepatik, splenik ve sternal lenfadenopatisi belirgin olan, ilk görüntüleme kontrolünde ve 1706 güne kadar düzelen tek bir köpekte tespit edilmiştir. Üç köpekte PR gözlenmiş ve karaciğer lezyonlarının boyutunda azalma (n = 3), malign efüzyonun çözülmesi (n = 2) ve akciğer nodüllerinin küçülmesi (n = 1) şeklinde gerçekleşmiştir. Yanıt oranı %57,1 ve hastalığın kontrol oranı %100 idi.
MC uygulanan altı köpekten üçünde SD ve üçünde PD vardı. SD’li üç köpekte hepatik kitle boyutu sırasıyla 35, 219 ve 703 gün boyunca sabit kalmış ve daha sonra lezyon rüptürü ve sekonder hemoabdomen ile boyut artmıştır. Yanıt oranı %0 ve hastalık kontrol oranı %50 idi.
Çalışmanın sonunda, sorafenib alan beş köpek ölmüştür (4’ü PH ve 1’i layşmanyaz nedeniyle). Tümöre bağlı ölümler, yüksek ihtimalle hepatik ensefalopatiye bağlı olarak hemoabdomen (n = 2) ve konvülsif kriz (n = 2) ile birlikte HCC rüptüründen kaynaklanmıştır. Nekropsiye izin verilmediğinden, bu vakalarda serebral metastazlar tamamen ekarte edilememiştir. Ortalama TTP 363 gün (%95 GA, 191-535); ortalama OS 361 gün (%95 GA, 0-909) idi.
MC grubundaki tüm köpekler PD nedeniyle ölmüştür. Tümöre bağlı ölümler hemoabdomen (n = 4), peritoneal ve adrenal metastazlar (n = 1) ve dissemine intravasküler koagülopati (n = 1) ile birlikte HCC rüptürüne bağlıydı. Ortalama TTP 27 gün (%95 GA, 0-68); ortalama OS 32 gün (%95 GA, 0-235) idi.
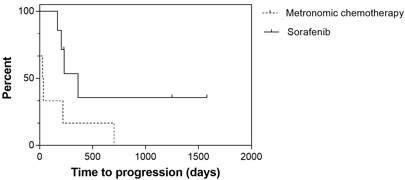
Sorafenib alan köpeklerde TTP istatistiksel olarak anlamlı derecede uzarken (p = 0,044), OS için anlamlı bir fark görülmemiştir (p = 0,079) (Şekil 4 ve 5).
Şekil 5. Sorafenib (düz çizgi) veya metronomik kemoterapi (kısa çizgi) ile tedavi edilen hepatosellüler karsinomlu 13 köpek için genel sağkalım. Ortalama genel sağkalım sorafenib grubu için 361 gün ve metronomik kemoterapi grubu için 32 gün sürmüştür; ancak aradaki fark istatistiksel olarak anlamlı değildir (p = 0,079).
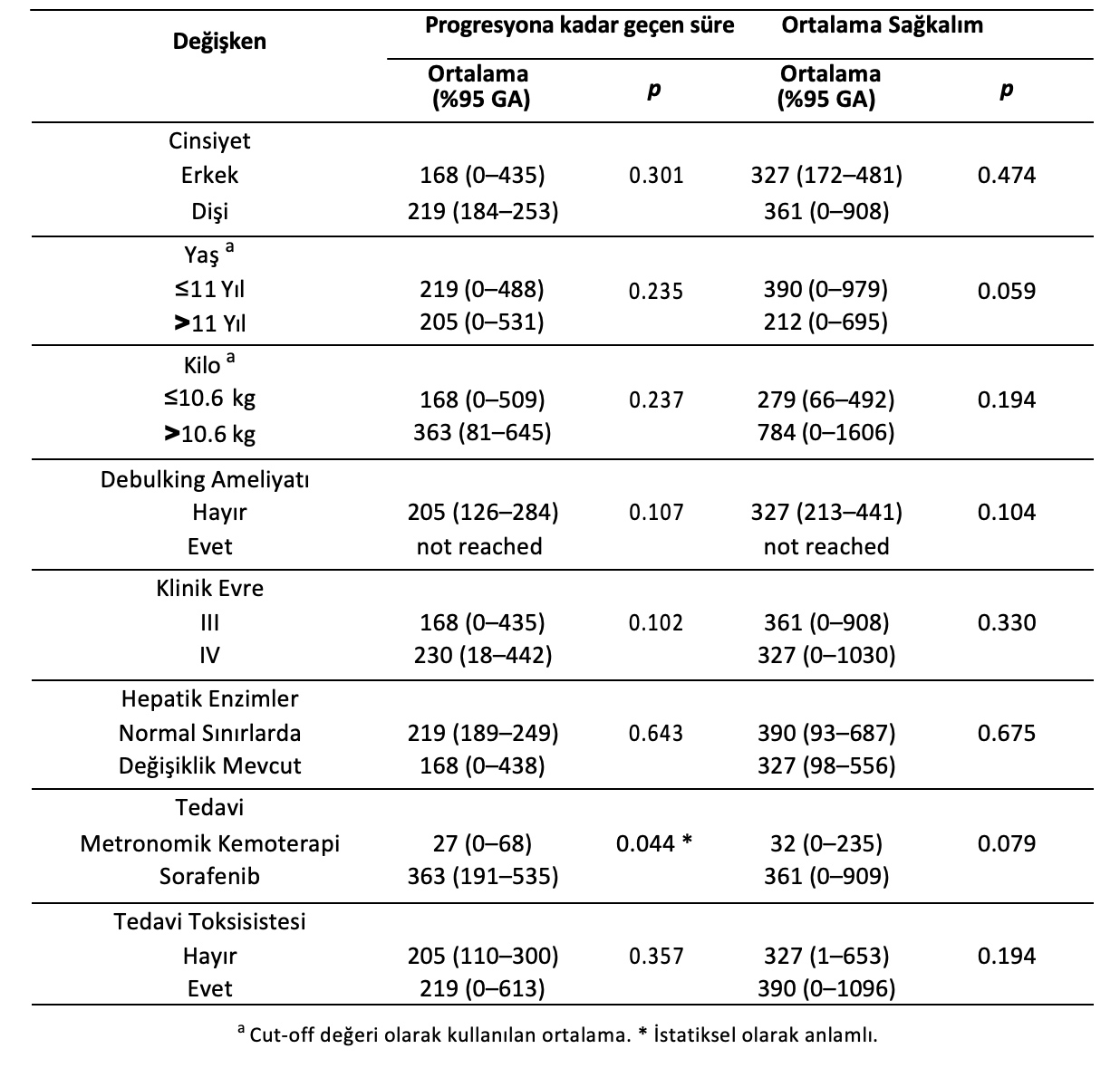
İncelenen diğer değişkenlerin hiçbiri TTP veya OS ile anlamlı derecede bağlantılı değildi (Tablo3).
Table 3. Hepatosellüler karsinomlu 13 köpekte tümör progresyonu ve genel sağkalım riskinde artış ile bağlantılı olabilecek değişkenler için log-rank testi.
1. Tartışma
Bu çalışmanın amacı sorafenibin rezeke edilemeyen HCC’li köpeklerde MC uygulananlara kıyasla güvenliliğini ve etkinliğini değerlendirmektir.
MC, düşük dozda kemoterapötik ilacın uzun süre sürekli olarak uygulanması prensibine dayanmaktadır; bu da neo-anjiyogenezin inhibisyonu yoluyla antitümör etkinin artmasına ve aynı zamanda her uygulamada azaltılan ilaç dozu ile düşük tosisite oranına imkan vermektedir. Merkezimiz tarafından çeşitli ilerlemiş kanserli köpeklerin tedavisinde bildirilen iyi sonuçlar [11,14,15] üzerine, MC’yi köpek HCC’sinde test ettik ve güvenilirliğinin pozitif yönde olduğunu teyit ettik.
HCC’li insanlarda, kapesitabinli MC’nin güvenilirliği ve antitümör etkisi oldukça yüksek bulunmuştur [29,30].
MC’nin toksisite profili gayet iyi belgelenmişken, sorafenib hakkında çok az şey bilinmektedir. Mevcut klinik çalışma başlatıldığında, köpeklerde tedavi toksisitesine ilişkin hiçbir veri yoktu, bu nedenle sağlıklı beagle’larda güvenli olduğu düşünülen doz uygulandı [26,27].
Bu çalışmada HCC tedavisinde kullanılan sorafenib programı ve dozu güvenli ve tolere edilebilir bulunmuştur. Üç (%42,9) kutanöz toksisite ve 1 (%14,3) ishal vakası yan etki olarak görülmüştür, ancak bunların hiçbiri doz sınırlayıcı toksisite değildir. Bununla birlikte, bu küçük ve doz artışı yapılmayan çalışma kapsamında, sonuçlarımızın başka çalışmalarla doğrulanması gerekmektedir. Özellikle, Yaşam Kalitesi analizi sorafenib alan 6/7 köpekte iyileşme görüldüğünü kanıtlamıştır.
Bununla birlikte, sorafenib insanlarda ciddi toksisiteye neden olmaktadır ve tedaviye bağlı en yaygın yan etkiler arasında el-ayak sendromu, hipertansiyon ve ishal yer almaktadır [16]. Bununla birlikte, çeşitli çalışmalara göre, bir veya daha fazla yan etki görülmesi ile daha uzun TTP, hastalık kontrol oranı ve OS arasında bağlantı kurulmuştur [16].
Rezeke edilemeyen HCC’li köpeklerde cerrahi olmayan herhangi bir etkin tedavi seçeneğinin bulunmadığı bildirilmiştir [1-3]. Şu anda, diffüz veya nodüler tipte HCC’li köpekler için sitotoksik ajanlarla standart sistemik kemoterapi tedavisi bulunmamaktadır. Gemsitabin ile tek ajan olarak veya karboplatin ile dönüşümlü geleneksel kemoterapi köpeklerde test edilmiş, ancak sağkalım bakımından fayda sağladığına dair herhangi bir kanıt bulunamamıştır [5,6].
Sorafenib, insan ileri evre HCC tedavisi için onaylanan ilk moleküler hedefli ilaçtır ve anti-proliferatif ve anti-anjiyojenik aktivitelere sahip çoklu kinazların güçlü ve küçük moleküllü inhibitörüdür.
İnsan ileri evre HCC’sinde sorafenib ile ilgili 10 yıllık araştırmanın ardından, tedaviye yanıt açısından hala doğrulanmış prognostik veya öngörücü hiçbir faktör bulunmamaktadır. Ayrıca, direncin gerçek moleküler mekanizmaları da tam olarak aydınlatılamamıştır [31,32].
Sorafenib ile tedavi edilen hasta popülasyonumuzun TTP’si MC ile tedavi edilen köpeklere kıyasla daha iyiydi. Benzer şekilde, resmi olarak karşılaştırılmamış olsa da, bu çalışmada gözlemlenen yanıt oranı, TTP ve OS, sitotoksik kemoterapiye odaklanan diğer çalışmalarda bildirilen sonuçlardan daha yüksektir [5,6].
Sorafenib alan köpeklerin MC (32 gün) alanlara göre ortalama OS (361 gün) 10 kat daha yüksek olmasına rağmen, örneklem boyutunun küçük olması bu gözlemin sağkalım açısından daha iyi sonuç verip vermediğinin belirlenmesine engel olmuştur. Sorafenib alan yedi köpekten beşinin ilacın temin edilememesi nedeniyle tedaviyi bıraktığı unutulmamalıdır. Bu nedenle, sorafenib ile sürekli tedavinin sağkalım süresini de uzatabileceği düşünülebilir.
Öte yandan, düşük bir ihtimal olsa da, sorafenib grubunda daha uzun yaşama eğiliminin nedeni MC’de başarısız olan rezeke edilemeyen HCC’li köpekler için herhangi bir etkili tedavinin olmaması olabilir. Nitekim, sorafenib alan köpeklerin ilerlemeleri halinde veya ilacın artık mevcut olmaması durumunda MC’ye veya diğer tedavilere geçmelerine izin verilirken, MC alan köpekler için ilerleme sonrası tedavi önerilmemiştir. Ayrıca, köpeklerini araştırma amaçlı kullanılacak ilaçlarla tedavi ettirmeyi kabul eden köpek sahipleri, hastalık ilerlediğinde, özellikle de yaşam kalitesi arttığında tedaviye devam etmeye istekli olabilirler. Bu durum, sorafenib alan köpek grubundaki sonuçların daha iyi olmasına yardımcı olmuş olabilir. Veteriner onkolojide, yaşam kalitesinin (nicelikten ziyade) uygulanacak herhangi bir antitümöral tedavinin birincil hedefi olduğu kabul edilmelidir. Sonuç olarak, sağkalım süresi yaşam kalitesiyle yakından ilişkilidir ve bu da muhtemelen sonuçları saptırmaktadır. Bununla birlikte, geçiş yapan köpeklerin kısa bir süre (sırasıyla 28 ve 34 gün) MC aldığını ve böylece tedavi değişikliği nedeniyle sağkalım bakımından ciddi faydalar elde etme olasılığını azalttığını belirtmek önemlidir.
Mevcut çalışmada, sorafenib tedavi grubundaki iki köpek, sistemik tedaviye başlamadan önce debulking ameliyatı ile ön tedaviye tabi tutulmuş ve rezidüel lokal ve metastatik hastalık olmasına rağmen tedaviye olağanüstü derecede yanıt vermiştir. Hematolojik olmayan kanserler için mevcut sistemik tedavilerle hacimli hastalığı tedavi etmek zor olduğundan bu bulgu beklenmedik bir durum değildi. Norton-Simon hipotezine göre, en yüksek kemosensitivite derecesi tümör hacimsiz olduğunda ortaya çıkmaktadır. Bu nedenle, debulking ameliyatı daha kemosensitif bir rezidüel tümör yükü ile sonuçlanabilir ve bu da lokal tedavi alma imkanının bu köpeklerde görülen olumlu sonuçlara katkıda bulunmuş olabileceğini düşündürmektedir.
Hasta popülasyonunun küçük olmasının yanı sıra, bu çalışmanın başka kısıtlamaları da bulunmaktadır. İlk olarak, randomize edilmemiş ve tedaviler klinisyen ve sahiplerinin takdirine bağlı olarak seçilmiştir. Bu durum, sorafenib ile tedavi edilen köpekler için seçim yanlılığına yol açmış olabilir, ancak iki grup arasında köpeklerin özelliklerinde herhangi bir anlamlı fark bulunmamıştır. İkinci olarak, her iki gruptaki bazı köpekler daha önce debulking ameliyatı geçirmiştir. Son olarak, sorafenibin bulunabilirliğinin az olması yedi köpekten beşinde sorafenib kullanımına devam edilmesini engellemiştir.
Bu sınırlamalar göz önünde bulundurulduğunda, sorafenib, hastalığın kontrolündeki faydası ve güvenirlilik profilinin kabul edilebilir olması nedeniyle, ilerlemiş HCC’li köpeklerin tedavisi için iyi bir aday gibi görünmektedir.
2. Materyal ve Method
- Çalışmaya dahil edilme ve edilmeme kriterleri
Herhangi bir klinik evrede histolojik olarak doğrulanmış HCC’si olan köpekler çalışmaya dahil edilmiştir (Tablo4). Köpekler, cerrahi eksizyon için uygun değillerse veya primer tümörün cerrahi olarak çıkarılmasından bağımsız olarak, kabul sırasında nodal veya uzak metastatik hastalık doğrulanmışsa çalışmaya dahil edilmeye uygun bulunmuştur.
Dahil edilme kriterleri şöyleydi: (1) köpek Solid Tümörlerinde Yanıt Değerlendirme Kriterleri versiyon 1.0’a göre ultrason veya bilgisayarlı tomografi (BT) ile ölçülebilen en az bir tek boyutlu lezyon; (2) klinik evre değerlendirmelerinin T3 veya N1 veya M1 şeklinde olması veya görüntülemede karaciğer lobektomisinin güvenli bir şekilde yapılabilmesi için yeterli normal karaciğer dokusunun bulunmaması durumunda cerrahi rezeksiyon kararı alınamaması; (3) önceden sistemik antitümöral tedavi uygulanmamış olması; (4) normal CBC, renal ve hepatik serum kimyası değerleri ile kanıtlanan verilere göre yeterli kemik iliği, kardiyak, renal ve hepatik fonksiyon. Özellikle, köpeklerin mutlak nötrofil sayısının ≥ 1500 hücre/µL, hematokritin ≥ %25, trombosit sayısının ≥ 100.000/µL, serum kreatinin konsantrasyonunun ve alanin transaminaz aktivitesinin normalin üst sınırının ≤ 3 katı, letarji/yorgunluk durumunun (VCOG-CTCAE versiyon 1.0) 0 veya 1 olması gerekmekteydi [24].
Çalışmaya dahil edilmeme kriterleri arasında hepatik ensefalopati, ikinci maligniteler, eş zamanlı ciddi sistemik hastalıklar veya daha önce sistemik kemoterapi veya moleküler tedavi uygulanmış olması vardı.
Kayıtlar Aralık 2011’de başlamış ve çalışma Haziran 2017’de sona ermiştir.
Bu çalışmaya katılmak için her hasta sahibinden yazılı, bilgilendirilmiş onam alınmıştır. Tüm hayvan sahipleri, tedavinin bilinmeyen sonuçları ve tedaviye bağlı morbiditeler de dahil olmak üzere tedavilerin avantaj ve dezavantajları konusunda bilgilendirilmiştir. Nihai tedavi kararı, katılımı reddetme seçeneğine tam saygı gösterilerek, her hasta sahibi ve ilgili klinisyen tarafından ortaklaşa alınmıştır.
- Tedavi protokolü
Sorafenib tedavisi tüm köpeklere önerilmiştir. Hasta sahiplerinin sorafenibi reddetmesi halinde köpeklere MC uygulanmıştır.
Sorafenib, aç karnına günde iki kez 5 mg/kg dozunda oral olarak uygulandı; doz en yakın 50 mg’a kadar uygulandı.
Hastalığın ilerlemesi, protokolde tanımlanan şekilde kabul edilemez seviyede toksisite, 30 günden uzun süreli doz kesintisi, hasta sahibinin tercihi, tedaviyi yürüten doktorun tavsiyesi veya ilacın bulunamaması üzerine ilaç kesilmiştir. Sorafenibin kesilmesi durumunda, nedeni ne olursa olsun, köpeklerin MC dahil olmak üzere alternatif tedavilere geçmesine izin verilmiştir.
MC ağızdan uygulanmış ve düşük doz siklofosfamid (10 mg/m2 q24 saat), piroksikam (0,3 mg/kg q24 saat) ve talidomidden (2 mg/kg q24 saat) meydana gelmiştir. Talidomid uygulaması yapan hasta sahipleri, ilacın bilinen teratojenik etkisi konusunda kapsamlı bir şekilde bilgilendirilmiştir.
- Güvenilirliğin Değerlendirilmesi ve Tedavinin Etkinliği
Güvenilirlik değerlendirmesi, tedavinin başlangıcından 14 gün sonra yapılmış ve hasta sahiplerinden alınan tıbbi öykü, fizik muayene, diferansiyel ve trombosit sayımı ile CBC, serum biyokimyasal analizi ve idrar sedimentinin mikroskobik incelemesi dahil olmak üzere idrar tahlili ile yapılmıştır. Köpeğin yaşamsal fonksiyonları, ateşi ve sistolik kan basıncı her muayenede kaydedilmiştir.
Takip sırasında, karaciğer fonksiyonunu değerlendirmek için her 4-6 haftada bir ALT, AST, γGTP, serum albümini, total bilirubin, üre ve kreatinin seviyeleri belirlendi. Toksik etkiler VCOG-CTCAE kılavuzlarına uygun olarak derecelendirilmiştir [33]. Kabul edilemez toksisite, herhangi bir doku veya organda grade 3 veya daha yüksek yan etki şeklinde tanımlanmıştır.
Yaşam kalitesi (QOL), araştırmacıların klinik uzmanlığına göre çalışma için tasarlanmış olan anket ile başlangıçta (tedaviye başlamadan önce) ve tedavi sırasında her muayenede değerlendirilmiştir (Anket S1).
Tümör ölçümleri, RECIST [34] temel alınarak, başlangıçta (tedaviye başlamadan önceki 14 gün içinde) batın ultrasonu veya tüm vücut bilgisayarlı tomografi (TBCT) ile yapılmıştır. Toraks röntgeni de başlangıçtaki çalışmaya dahil edilmiş ve klinik olarak endike olması halinde takipte tekrarlanmıştır. İlk takip görüntülemesi her iki tedavi kolunda da 4 hafta sonra ve daha sonra her 4-8 haftada bir yapılmıştır.
Terapötik etki RECIST tarafından şu şekilde tanımlanmıştır: tam yanıt (CR), ölçülebilir tüm lezyonların >4 hafta boyunca kaybolması; kısmi yanıt (PR), en büyük hedef lezyon çaplarının toplamında >%30 azalma ve >4 hafta boyunca yeni bir lezyon gelişmemesi; ilerleyici hastalık (PD), en büyük hedef lezyon çaplarının toplamında >%20 artış veya yeni bir lezyonun ortaya çıkması; ve stabil hastalık (SD), >4 hafta boyunca ne PR ne de PD görülmemesi.
İlk radyografik değerlendirmeden önce ölen köpekler PD olarak sınıflandırılmıştır. CR, PR, SD ve PD elde edilen köpeklerin sayısı analiz edilmiştir. Yanıt oranı, RECIST değerlendirmesi CR veya PR şeklinde en iyi yanıtı veren köpeklerin yüzdesi olarak tanımlanmış ve böyle bir derecelendirmenin ilk kez görülmesinden sonra en az dört hafta boyunca korunmuştur. Hastalık kontrol oranı, RECIST derecelendirmesine göre en iyi yanıtı CR, PR veya SD olan ve bu derecelendirmenin ilk kez gösterilmesinden sonra en az dört hafta boyunca korunan köpeklerin yüzdesi olarak tanımlanmıştır. SD veya objektif yanıtı olan köpekler için sağkalım için takip değerlendirmeleri PD ve/veya ölüme kadar her 4 haftada bir yapılmıştır.
- İstatiksel Analiz
İki protokolü alan köpekler arasındaki demografik ve klinik özellikler arasındaki farklar Mann-Whitney U-testi ve Fisher’in kesin testi ile değerlendirilmiştir.
Progresyona kadar geçen süre (TTP), tedavinin başlangıcından hastalığın progresyon tarihine kadar geçen süre olarak tanımlanmıştır. Genel sağkalım (OS), tedavinin başlangıcından ölüm tarihine veya köpeğin son takibine kadar geçen süre olarak tanımlanmıştır. Sağkalım analizi için, köpekler çalışma sona erdiğinde hayattaysa veya tümörle ilişkili olmayan nedenlerden ölmüşse sansürlenirken, TTP için köpekler son muayenede hastalık ilerlememişse sansürlenmiştir.
Sağkalım eğrileri Kaplan-Meier çarpım-limit yöntemine göre oluşturulmuştur. Sağkalım tahminleri, karşılık gelen %95 güven aralıkları (%95 GA) ile birlikte ortalama olarak verilmiştir. Potansiyel prognostik değişkenlerin (cinsiyet, yaş, kilo, lezyonların çokluğu, klinik evre, değişen karaciğer enzimleri, debulking ameliyatı, tedavi protokolü, tedavi toksisitesi) TTP ve OS üzerindeki etkisi log-rank testi ile araştırılmıştır.
Veriler ticari yazılım programları (SPSS Statistics v. 24, IBM, Somers, NY ve Prism v. 5.0, GraphPad, San Diego, CA, ABD) kullanılarak analiz edilmiştir. p değerleri ≤ 0.05 istatistiksel olarak anlamlı kabul edilmiştir.
- Sonuçlar
Bu çalışmanın sonuçları, ilerlemiş HCC’li köpeklerde MC veya geleneksel kemoterapiye karşı sorafenibin etkinliğini ve dezavantajını karşılaştırmak için yeni randomize prospektif klinik çalışmaların yapılması için sağlam bir temel sunmaktadır.
Ek Materyaller: Metronomik kemoterapi veya sorafenib alan ileri evre hepatosellüler karsinomlu 13 köpekte yaşam kalitesinin değerlendirilmesine yönelik S1 Anketi http://www.mdpi.com/2072-6694/12/5/1272/s1 adresinde çevrimiçi olarak mevcuttur.
Katkıda Bulunan Yazarlar: Kavramsallaştırma, L.M. ve A.C.-G.; Veri düzenleme, L.M. ve S.S.; Resmi analiz, S.S.; Araştırma, F.R. ve V.F.L.; Metodoloji, S.S., G.M. ve A.C.-G.; Proje yönetimi, L.M.; Yazım-Orijinal taslak, L.M. ve S.S.; Yazım-İnceleme ve düzenleme, A.C.-G. Tüm yazarlar makalenin yayınlanan versiyonunu okumuş ve kabul etmiştir.
Finansman: Bu araştırma herhangi bir dış finansman almamıştır.
Çıkar Çatışması Beyanı: Yazarlar herhangi bir çıkar çatışması beyan etmemektedir.
Kaynakça
- Patnaik, A.K.; Hurvitz, A.I.; Lieberman, H.;Johnson, G.F. Canine hepatocellular carcinoma. Vet. Pathol.
1981, 18, 427–438. [CrossRef] [PubMed]
- Liptak, J.M.; Dernell, S.; Monnet, E.; Powers, B.E.; Bachand, A.M.; Kenney, J.G.; Withrow, S.J. Massive hepatocellular carcinoma in dogs: 48 cases, (1992–2002). Am. Vet. Med. Assoc. 2004, 225, 1225–1230. [CrossRef] [PubMed]
- Kosovsky, E.; Matthiesen, D.T. Results of partial hepatectomy in 18 dogs with hepatocellular, carcinoma.
- Am. Anim. Hosp. Assoc. 1989, 25, 203–206.
- Marin, J.; Romero, M.R.; Briz, O. Molecular bases of liver cancer refractoriness to pharmacological, treatment.
Curr. Med. Chem. 2010, 17, 709–740. [CrossRef] [PubMed]
- Elpiner, K.; Brodsky, E.M.; Hazzah, T.N.; Post, G.S. Single-agent gemcitabine chemotherapy in dogs with hepatocellular carcinomas. Vet. Comp. Oncol. 2011, 9, 260–268. [CrossRef] [PubMed]
- Dominguez, A.; Dervisis, N.G.; Cadile, C.D.; Sarbu, L.; Kitchell, B.E. Combined gemcitabine carboplatin therapy for carcinomas in dogs. J. Vet. Intern. Med. 2009, 23, 130–137. [CrossRef] [PubMed]
- Kareva, ; Waxman, D.L.; Klement, G.L. Metronomic chemotherapy: An attractive alternative to maximum tolerated dose therapy that can activate anti-tumor immunity minimize therapeutic resistance. Cancer Lett. 2015, 358, 100–106. [CrossRef]
- Lana, S.; U’ren, L.; Plaza, S.; Elmslie, R.; Gustafson, D.; Morley, ; Dow, S. Continuous low-dose oral chemotherapy for adjuvant therapy of splenichemangiosarcoma in, dogs. Vet. Intern. Med. 2007, 21, 764–769. [CrossRef]
- Elmslie, E.; Glawe, P.; Dow, S.W. Metronomic therapy with cyclophosphamide piroxicam effectively
delays tumor recurrence in dogs with incompletely resected soft tissue sarcomas. J. Vet. Intern. Med.
2008, 22, 1373–1379. [CrossRef]
- London, A.; Gardner, H.L.; Mathie, T.; Stingle, N.; Portela, R.; Pennell, M.L.; Clifford, C.A.; Rosenberg, M.P.; Vail, D.M.; Williams, L.E.; et al. Impact of toceranib/piroxicam/cyclophosphamide maintenance therapy on outcome of dogs with appendicular osteosarcoma following amputation carboplatin chemotherapy: A multi-institutional, study. PLoS ONE 2015, 10, e0124889. [CrossRef]
- Finotello, R.; Henriques, J.; Sabattini, S.; Stefanello, D.; Felisberto, R.; Pizzoni, S.; Ferrari, R.; Marconato, L. A retrospective analysis of chemotherapy switch suggests improved outcome in surgically removed biologically aggressive canine Vet. Comp. Oncol. 2017, 15,493–503. [CrossRef] [PubMed]
- Bray, P.; Orbell, G.; Cave, N.; Munday, J.S. Does thalidomide prolong survival in dogs with splenic haemangiosarcoma? Small Anim. Pract. 2018, 59, 85–91. [CrossRef] [PubMed]
- de Campos, C.B.; Lavalle, G.E.; Fialho Ligório, S.; Camargo Nunes, ; Carneiro, R.A.; Amorim, R.L.; Cassali, G.D. Absence of significant adverse events following thalidomide administration in bitches diagnosed with mammary gland carcinomas. Vet. Rec. 2016, 179, 514. [CrossRef] [PubMed]
- Cancedda, ; Marconato, L.; Meier, V.; Laganga, P.; Roos, M.; Leone, V.F.; Rossi, F.; Bley, C.R. Hypofractionated radiotherapy for macroscopic canine softtissue sarcoma: A retrospective study of 50 cases treated with a 5×6 Gy protocol with or without metronomic chemotherapy. Vet. Radiol. Ultrasound 2016, 57, 75–83. [CrossRef] [PubMed]
- Polton, G.; Finotello, R.; Sabattini, S.; Rossi FLaganga, ; Vasconi, M.E.; Barbanera, A.; Stiborova, K.; Rohrer Bley, C.; Marconato, L. Survivalanalysis of dogs with advanced primary lung carcinoma treated by metronomic cyclophosphamide piroxicam thalidomide. Vet. Comp. Oncol. 2018, 16, 399–408. [CrossRef] [PubMed]
- Llovet, M.; Ricci, S.; Mazzaferro, V.; Hilgard, P.; Gane, E.; Blanc, J.F.; de Oliveira, A.C.; Santoro, A.; Raoul, J.L.; Forner, A.; et al. Sorafenib in advanced hepatocellular carcinoma. N. Engl. J. Med. 2008, 359, 378–390. [CrossRef]
- De Matteis, ; Ragusa, A.; Marisi, G.; De Domenico, S.; Gardini, A.C.; Bonafè, M.; Giudetti, A.M. Abberant
metabolism in hepatocellular carcinoma provides diagnostic therapeutic, opportunities. Oxid. Med. Cell Longev. 2018, 2018, 7512159. [CrossRef]
- Casadei-Gardini, A.; Del Coco, L.; Marisi, G.; Conti, ; Rovesti, G.; Ulivi, P.; Canale, M.; Frassineti, G.L.; Foschi, F.G.; Longo, S.; et al. 1H-NMR based serum metabolomics highlights different specific biomarkers between early advanced hepatocellular carcinoma, stages. Cancers (Basel) 2020, 12, 241. [CrossRef]
- De Matteis, S.; Scarpi, E.; Granato, A.M.; Vespasiani-Gentilucci, U.; La Barba, G.; Foschi, G.; Bandini, E.; Ghetti, M.; Marisi, G.; Cravero, P.; et al. Role of SIRT-3, p-mTOR and HIF-1α in Hepatocellular carcinoma patients affected by metabolic dysfunctions and in chronic treatment withmetformin. Int. J. Mol. Sci.
2019, 20, 1503. [CrossRef]
- Fiume, L.; Manerba, M.; Vettraino, M.; Di Stefano, G. Effect of sorafenib on the energy metabolism of hepatocellular carcinoma cells. J. Pharmacol. 2011, 670, 39–43. [CrossRef]
- Kim, J.; Choi, Y.K.; Park, S.Y.; Jang, S.Y.; Lee, J.Y.; Ham, H.J.; Kim, B.G.; Jeon, H.J.; Kim, J.H.; Kim, J.G.; et al. PPARδ reprograms glutaminemetabolism in sorafenib-resistant HCC. Mol. Cancer Res. 2017, 15, 1230–1242. [CrossRef] [PubMed]
- Cassim, ; Raymond, V.A.; Lacoste, B.; Lapierre, P.; Bilodeau, M. Metabolite profiling identifies a signature of tumorigenicity in hepatocellular carcinoma. Oncotarget 2018, 9, 26868–26883. [CrossRef] [PubMed]
- Strumberg, ; Clark, J.W.; Awada, A.; Moore, M.J.; Richly, H.; Hendlisz, A.; Hirte, H.W.; Eder, J.P.; Lenz, H.J.; Schwartz, B. Safety, pharmacokinetics, and preliminary antitumor activity of sorafenib: A review of four phase I trials in patients with advanced refractory solid tumors. Oncologist 2007, 12, 426–437. [CrossRef]
- Wolfesberger, ; Tonar, Z.; Gerner, W.; Skalicky, M.; Heiduschka, G.; Egerbacher, M.; Thalhammer, J.G.; Walter, I. Pharmacologic inhibition of MEKsignaling prevents growth of canine hemangiosarcoma. Mol. Cancer Ther. 2013, 12, 1701–1714.
- Wolfesberger, ; Tonar, Z.; Gerner, W.; Skalicky, M.; Heiduschka, G.; Egerbacher, M.; Thalhammer, J.G.; Walter, I. The tyrosine kinase inhibitor sorafenib decreases cell number and induces apoptosis in a canine osteosarcoma cell line. Res. Vet. Sci 2010, 88, 94–100. [CrossRef] [PubMed]
- Wilhelm, S.; Chien, D.S. BAY 43-9006: Preclinical data. Pharm. Des. 2002, 8, 2255–2257. [CrossRef] [PubMed]
- European Medical Agency [Webpage on the Internet]. Initial Marketing Authorization Study of Nexavar. 2007. Available online:http://ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/ 000690/human_med_000929.jsp&mid=WC0b01ac058001d124(accessed on 4 March 2017).
- Foskett, ; Manley, C.; Naramore, R.; Gordon, I.K.; Stewart, B.M.; Khanna, C. Tolerability of oral sorafenib in pet dogs with a diagnosis of cancer. Vet. Med. (Auckl.) 2017, 8, 97–102. [CrossRef]
- Casadei Gardini, ; Foca, F.; Scartozzi, M.; Silvestris, N.; Tamburini, E.; Faloppi, L.; Brunetti, O.; Rudnas, B.; Pisconti, S.; Valgiusti, M.; et al.Metronomic capecitabine versus best supportive care as second-line treatment in hepatocellular carcinoma: A retrospective study. Sci. Rep. 2017, 7, 42499.[CrossRef]
- Trevisani, ; Brandi, G.; Garuti, F.; Barbera, M.A.; Tortora, R.; Casadei Gardini, A.; Granito, A.; Tovoli, F.; De Lorenzo, S.; Inghilesi, A.L.; et al. Metronomic capecitabine as second-line treatment for hepatocellular carcinoma after sorafenib discontinuation. J. Cancer Res. Clin. Oncol. 2018, 144, 403–414. [CrossRef]
- Marisi, ; Cucchetti, A.; Ulivi, P.; Canale, M.; Cabibbo, G.; Solaini, L.; Foschi, F.G.; De Matteis, S.; Ercolani, G.; Valgiusti, M.; et al. Ten years of sorafenib in hepatocellular carcinoma: Are there any predictive and/or prognostic markers? World J. Gastroenterol. 2018, 24, 4152–4163. [CrossRef]
- Di Costanzo, G.G.; Casadei Gardini, A.; Marisi, G.; Foschi, G.; Scartozzi, M.; Granata, R.; Faloppi, L.; Cascinu, S.; Silvestris, N.; Brunetti, O.; et al. Validation of a simple scoring system to predict sorafenib effectiveness in patients with hepatocellular carcinoma. Target. Oncol. 2017, 12, 795–803. [CrossRef] [PubMed]
- Veterinary Co-operative Oncology Veterinary Co-operative oncology group- common terminology criteria for adverse events (VCOG-CTCAE)following chemotherapy or biological antineoplastic therapy in dogs and cats v1.0. Vet. Comp. Oncol. 2004, 2, 194–213.
- Nguyen, S.M.; Thamm, D.H.; Vail, M.; London, C.A. Response evaluation criteria for solid tumours in dogs (v1.0): A veterinary cooperative oncology group (VCOG) consensus document. Vet. Comp. Oncol. 2015, 13, 176–183. [CrossRef] [PubMed]
© 2020 yazarlar tarafından. Lisans sahibi MDPI, Basel, İsviçre. Bu makale Creative Commons Attribution (CC BY) lisansı (http://creativecommons.org/licenses/by/4.0/) hüküm ve koşulları altında dağıtılan açık erişimli bir makaledir.